Материал: Определение характеристик макета БПК-биосенсора на основе дрожжей Debaryamyces hansenii, иммобилизованных в модифицированный ПВС с использованием различных синтетических сточных вод
Определение концентрации растворенного кислорода
при анализе воды на БПК может выполняться различными методами.
1.4.1 Определение БПК5 методом разбавления
Определение БПК5 проводится в первоначальной или соответственно разбавленной пробе по разности между содержанием кислорода до и после инкубации в течение пяти суток без доступа кислорода и света. Инкубацию проводят в режиме постоянной температуры (20±1)°С, причем от точности поддержания значения температуры зависит точность выполнения анализа на БПК. Погрешность в определении БПК может внести также освещение пробы, влияющее на жизнедеятельность микроорганизмов и способное в некоторых случаях вызывать фотохимическое окисление. Поэтому инкубацию пробы проводят без доступа света (в темном месте).[23]
Содержание кислорода в первоначальной или разбавленной пробе должно оставаться в течение всего периода инкубации таким, чтобы были обеспечены нормальные условия протекания аэробных биохимических процессов. Эти условия будут соблюдены, если анализируемая проба перед началом определения будет насыщена кислородом воздуха (приблизительно до 8-9 мг/дм3 при 20°С) и если во время инкубации произойдет снижение концентрации кислорода на 2 мг/дм3 или больше, но так, чтобы спустя пять суток она составляла не менее 2 мг/дм3.
Исследуемую воду (при 20°С) аэририруют путем встряхивания или продувки воздуха. Далее определяют содержание кислорода в первоначальной или разбавленной пробе одним из следующих методов - йодометрическим определением по Винклеру, полярографическим пирофосфатным, или электрометрическим методами.
Определив содержание растворенного кислорода в
полученной смеси, ее оставляют в закрытой склянке на 5 суток при 20 °С без
доступа воздуха и света. Затем вновь определяют содержание растворенного
кислорода. Уменьшение количества кислорода в воде показывает, сколько его за
это время израсходовано на окисление органических веществ, находящихся в сточной
воде. Это количество, отнесенное к 1 дм3 сточной воды, и является биохимическим
потреблением кислорода сточной водой за данный промежуток времени (БПК5).
1.4.2 Определение БПК манометрическим методом
Данным метод основан на том, что в сосуде для
определения БПК над жидкостью находится воздух, объем которого четко
определяется объемом пробы воды. На биологическое разрушение органических
примесей воды расходуется кислород, содержащийся в воздухе над жидкостью.
Гранулы гидроксида натрия или калия предназначены для поглощения углекислого
газа, образующегося в результате биологического разрушения. Для интенсивного
массообмена между жидкой и газовой фазами предусмотрено непрерывное
перемешивание. В течение времени количество кислорода в объеме воздуха над пробой
воды уменьшается, в результате чего давление внутри сосуда снижается. Снижение
давления измеряется датчиком в крышке, которой закрывается сосуд. Диапазон
измерений БПК от 0 - 40 до 0 - 4000 мг/дм3, в зависимости от объема пробы и
ожидаемого значения.[27]


Рис. 9 - Манометрические датчики OxiTop для
определения БПК
Вычисление результатов анализа.
Снижение давления, зафиксированное датчиком,
пропорционально количеству поглощенного кислорода, которое пересчитывается в
значение БПК по формуле:
![]() , где
, где
(O2) - молекулярная масса кислорода, 32000мг/моль- универсальная газовая постоянная, 83,144 мбар/к∙моль
Т0 - исходная температура, к
Т1 - температура измерения, к- теоритический объем бутыли, см3- объем пробы, см3
α - коэффициент адсорбции Бунзена
Δр(О2) - парциальное давление кислорода
Преимущества манометрического метода
по сравнению с методом Винклера в том что воздействия на образец воды сведено к
минимуму. Использование OxiTop намного упрощает измерение БПК, так как он
автоматически запоминает измеренные значения. Все сохраненные в памяти прибора
значения можно считать в любой день. К разбавлениям приходиться прибегать
редко, что снижает трудо- и времяемкость анализа. Иными словами количество
рутинных операций при использовании OxiTop минимально. Однако метод не
избавляет от главного недостатка - 5-ти суточной инкубации.
1.4.3 Методы определения БПК с помощью биосенсоров
Большинство описанных в литературе БПК биосенсоров являются целоклеточными микробными сенсорами биокленочного типа, которые основаны на измерении скорости дыхания бактерий вблизи поверхности преобразователя. Первая работа, посвященная созданию подобного сенсора, была опубликована Karube et al. в 1977 г [28]; в качестве биоматериала были использованы микроорганизмы, взятые из активного ила очистных сооружений. К настоящему времени известно значительное количество лабораторных моделей и несколько промышленно выпускаемых биосенсорных анализаторов БПК. Такие анализаторы позволяют производить определение БПК в среднем диапазоне 5-300 мг/дм3 за время порядка нескольких минут; в качестве модельного соединения для калибровки прибора обычно используется смесь растворов глюкозы и глутаминовой кислоты или другие смеси органических соединений (так называемые синтетические сточные воды).
Разрабатываемые БПК-биосенсоры описанные в литературе разлчаются выбранными штаммами микроорганизмов или аасоциаций [29-38], способами иммобилизации [38], способами фиксации аналитического сигнала [39-42], а также применяемыми стандартами для калибровки датчиков [40], что позволяет повысить точность определения БПК.
Например, использование смешанных культур дает возможность расширения спектра биодеградируемых соединений (и, следовательно, обеспечивает более полное определение БПК), оборотной стороной этого подхода в большинстве случаев является сниженная стабильность и воспроизводимость результатов, что бывает связано с динамикой соотношения различных культур в биорецепторе. Поэтому, наряду с использованием активного ила и других смесей микроорганизмов, при конструировании БПК-сенсоров используют и чистые культуры бактерий и грибов, характеризующихся расширенным спектром метаболизируемых субстратов (т.е. широкой субстратной специфичностью). Примерами подобных приборов могут являться сенсоры, описанные в работах [29-37] и др.
Одним из микроорганизмов, наиболее часто используемых в составе БПК-сенсоров, является Trichosporon cutaneum [36-37]. Разными авторами опубликовано не менее десяти работ, посвященных созданию БПК-сенсоров на его основе; кроме того, он используется в ряде коммерческих анализаторов БПК. Пример подобного сенсора описан в работе [37]. Созданный прибор позволял определять БПК в диапазоне 0,2-18 мг/дм3. Время жизни биорецептора составляло 3 сут. Разброс показаний при измерении идентичных образцов не превышал 8%. Сенсор был использован для анализа промышленных и муниципальных сточных вод.
В некоторых разработанных БПК - биосенсорах для повышения корреляции со стандартным методом проводится предварительная пробоподготовка. Так, например, разработана система для определения низкого биохимическое потребление кислорода в реках с предварительным озонированием [44]. Реки содержат много бионедоступных органических веществ, таких как гуминовые кислоты и лигнин. Свободные радикалы, образованные саморазложением озона, использовались как мощный оксидант, чтобы расколоть органические вещества. При значении БПК 1 мг/дм3, ответ датчика после озонирования был в 1,6 раз выше, чем до озонирования. Время ответа БПК - биосенсора составляло 5 минут и не зависело от значения БПК, нижний предел обнаружения составлял 0,5 мг/дм3 БПК. Разработанная система была применена для определения БПК в реках. Была показана хорошая корреляция между ответом биосенсора и стандартным методом определения БПК5 (R = 0,989).
Описанные выше сенсоры основаны на использовании амперометрических кислородных преобразователей, как правило, электродов Кларка, однако это - не единственный возможный подход к созданию БПК-сенсоров. Следует отметить, что на значение БПК, определяемого с помощью микробного дыхания, влияют количество растворенного кислорода в образце. Известно, что некоторые синтетические соединения (искусственные акцепторы электронов) способны восстанавливаться определенными микроорганизмами, т.е. конкурируют за электроны с кислородом (естественным акцептором электронов). Если эти соединения обладают обратимыми окислительно-восстановительными свойствами, то они могут служить переносчиками электронов от биокаталитических систем микроорганизмов на электрод (медиаторами электронного транспорта). Преимущество использования медиаторов заключается в том что: результаты измерений становятся практически независимыми от парциального давления кислорода в среде и, если в процессе окисления восстановленного медиатора не участвуют протоны, то медиаторный электрод может быть относительно нечувствителен к изменениям рН. Таким образом, одним из наиболее перспективным направлением является разработка БПК-биосенсоров с применением медиаторов электронного транспорта [39-42].
В последнее время большое количество работ посвящено разработке БПК-биосенсоров оптического типа [45-48].
Это связано с тем, что оптические биосенсоры обладают высокой чувствительностью и, соответственно, позволяют определять низкие значения БПК.
Еще один подход к детекции БПК основан на регистрации изменений температуры, вызванных микробиологической деструкцией органических соединений. Этот подход основан на использовании калориметрических преобразователей; биосенсор на основе такого преобразователя описан в работе [49].
В зарубежной статье [50] на базе амперометрического датчика кислорода с ограниченной диффузией (кислородный электрод Кларка) был создан микробный БПК-датчик и исследована зависимость его выходного сигнала от биохимической потребности в кислороде сточных вод. Калибровка датчика БПК была выполнена в стационарном и динамическом режимах измерений с использованием растворах синтетических сточных вод (OECD). Результаты показали широкий диапазон определяемых концентраций (до 230 мг/дм3 БПК7), а также быстрый ответ и время регенерация раз в динамическом режиме анализа. Данные, полученные на стационарном метод показали лучшую воспроизводимость, особенно в оценке БПК7 реальных сточных вод. После калибровки датчика БПК был использован для быстрой оценки БПК городских сточных вод.
В сточных водах с высоким
содержанием жира был использован Aeromonas hydrophila P69.1 (А. hydrophila)
штамм для создания полуспецифичного биосенсора для оценки биохимического
потребления кислорода(БПК). В данной статье сравнивались биосенсоры на основе
клеток А. hydrophila и P. fluorescens. Клетки А. hydrophila выращивали в среде,
содержащей жир, чтобы вызвать образование необходимые ферменты для транспорта и
деградации жирных веществ. Универсальный биосенсор на основе неспецифических
specific Pseudomonas fluorescens P75 (P. fluorescens) был использован для
проведения экспериментов сравнения. Биосенсоры были откалиброваны с помощью
синтетических сточных вод (OECD) и стационарного метода. Линейный диапазон
биосенсорова на основе А. hydrophila составил до 45 мг/дм3 БПК7, по сравнению с
40 мг/дм3 БПК7 полученных с помощью биосенсора на основе P. fluorescens. Нижний
предел обнаружения обоих биосенсоров составил 5 мг/дм3 БПК7. Срок службы
биосенсоров на основе A. hydrophila и P. fluorescens составил 110 и 115 дней
соответственно. Время отклика биосенсоров зависело от БПК7 и составляло до 20
мин при анализе различных сточных вод. Оба биосенсора занижали БПК в сточных
водах мясоперерабатывающих предприятий с 43% до 71%, но более точные результаты
могут быть получены с помощью биосенсора на основе A. hydrophila.
Полу-специфичным биосенсором на основе A. hydrophila удалось измерить долю жира
в образцах сточных вод, в то время как другие трудноокисляемые соединения не
поддавались обнаружению обоих биосенсоров.
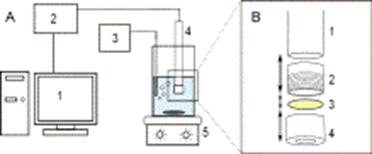
Рис. 10 - (А) Схематическое
представление биосенсорной измерительной системы: 1 компьютер, 2: измерительный
модуль, 3 блок аэрации, 4: биосенсор, 5 магнитная мешалка. (B) устройство
биосенсора: 1: датчик растворенного кислорода, 2: вставочное кольцо, 3:
мембрана, 4 держатель
В данной работе [52] предложен метод, использующий совместно иммобилизованные клетки Escherichia coli (E.coli), в качестве биокатализатора и нейтральный красный (NR), в качестве искусственного акцептора электронов, для модификации стеклоуглеродного электрода (GCE) для измерения биохимического потребления кислорода (БПК). Два разных подхода модификации GCE были использованы и сравнены. В одном подходе, нейтральный красный был элктрополимеризован на поверхности GCE, и клетки E.coli были смешаны с сополимером PVA-g-PVP (кратко gPVP) и нанесены на пленку NR для получения комплекса (gPVP/E. coli)/PNR/GCE. Во втором подходе, как клетки E.coli так и NR были смешаны с сополимером gPVP и нанесены на GCE, образуя комплекс (gPVP/E. coli/NR)p/GCE. На основе оценки электрохимических свойств, производительность последнего модифицированного электрода была лучше, что может быть обусловлено тем, что NR осаждается на поверхности E.coli вызывая хороший электронный транспорт и проницаемость мембран клеток. Для развития результатов, полученных с использованием (gPVP/E. coli/NR)p/GCE дальше, были использованы нанотрубки TiO2, а также различные эффекты на образцах ГГС, OECD, мочевины и реальных сточных вод. Эти результаты показывают, что данный метод имеет потенциальное применение для быстрого определения БПК с помощью биосенсоров.[52]
В стать [53] для контроля очистки сточных вод от промышленности латекса в качестве рецепторного элемента БПК-биосенсора использовались иммобилизованная смесь микроорганизмов. Принцип измерения был основан на определении потребления кислорода вызванного клеточным дыханием. В качестве смеси для калибровки БПК-биосенсора согласно требованиям Организация экономического сотрудничества и развития использовались синтетические сточные воды (OECD). Время ответа биосенсора составляло 10 - 15 минут. БПК втекающих и вытекающих из анаэробного реактора вод измеряли как методом с использованием биосенсора, так и стандартным методом БПК5 . Был достигнут высокий уровень корреляции между данными, полученными обоими методами, разница между значениями составила менее 10%. Однако при использовании данной смеси культур для анализа сточных вод другого производства уровень корреляции со стандартным методом был низкий. БПК - биосенсор был успешно применен для off-line и on-line мониторинга процессов анаэробной обработки.
Существуют методы быстрого и медленного определения БПК (BODst). Медленный - основанный на использовании медиатора феррицианида представлен в работе [54]. Позволяет преодолеть некоторые проблемы, связанные со стандартным анализом БПК (БПК5), таких как долгая инкубация (5 дней), необходимость разбавлять образцы и низкая воспроизводимость. Здесь представлены вариант измерений, где Klebsiella pneumoniae успешно окисляет феррицианид без деаэрации образцов с линейной зависимостью БПК5 30 - 500 мг/л или 30 - 200 мг/л, с использованием глюкозо-глутаматной смеси (ГГС ) и стандарта OECD соответственно. Кроме того, предложено решение для прекращение анализа, что позволяет увеличить воспроизводимость и стандартизовать анализ, используя формальдегид (22,7 г/л) или другие соединения, чтобы остановить восстановление феррицианида без ущерба для амперометрического обнаружения и, следовательно, заменить центрифугирование, обычно используемое для остановки реакции феррицианида с микроорганизмами. Эти усовершенствования привели к точному определению БПК реальных образцов муниципальных сточных вод.[55]
Данные представленые в статье [56]
описывают быстрый метод определения БПК. Активный ил был успешно использован в
качестве биокатализатора в быстром методе определения БПК с использованием
феррицианида (FM-BOD). Процедура подготовки активного ила были оптимизированы
для трех потенциальных биокатализаторов: ила из аэротенка, ила из осадка
аэробного реактор и регенерированного активного ила. После 24 часов голода
регенерированный активный ил и ил из аэротенка показали самые высокие
показатели окисления стандарта ГГС и регенерированный активный ил также показал
самый низкий уровень эндогенного дыхания. Рабочий диапазон составил до 170 мг/л
БПК5 для стандарта OECD и 300 мг/л БПК5 для ГГС. Это значительное улучшение по
сравнению с другими методами быстрого анализа БПК. Высокие значения
коэффициента корреляция с стандартным методом БПК5 (n = 35, p < 0.001, R =
0.952) наблюдались для широкого разнообразия реальных образцах сточных вод.
Средняя эффективность деградации не отличался от наблюдаемой для стандартного
БПК5 анализа. Эти результаты показывают, что активный ил в FM-BOD анализе может
быть использован для простого ежедневного анализа сточных вод.