Материал: Определение характеристик макета БПК-биосенсора на основе дрожжей Debaryamyces hansenii, иммобилизованных в модифицированный ПВС с использованием различных синтетических сточных вод
1.5 Различные стандарты применяемые
для калибровки БПК-датчиков
Синтетические сточные воды служат основой многих анализов связанных с определением качества воды. Их применяют для таких анализов как определение биохимического потребления кислорода (БПК), химического потребления кислорода (ХПК), TS и TSS. Так, например, при контроле анаэробных процессов определяют высокий уровень биохимического потребления кислорода (БПК) в образцах сточных вод от фабрики, обрабатывающей концентрированный каучук. Эти данные представлены в статье: [53].
Для формирования синтетических сточных вод используют различные органические и неорганические компоненты. Состав синтетических вод зависит от того, какие воды моделируются: городские сточные воды или индустриальные (промышленные) сточные воды. В городских стоках нет таких веществ, как крахмал, сахар и других легко деградируемых веществ, т.к. для очистки воды используют бактерии. Для создания более сложных органических синтетических сточных вод подходят такие компоненты как пептон, дрожжевой экстракт, мясной экстракт и глюкоза. Для моделирования синтетической водопроводной воды используют органические и неорганические соединения азота и фосфора.
Во многих зарубежных статьях описаны методики приготовления синтетических сточных вод, их состав и свойства. Так в статье Xiufen Li описано применение синтетической сточной воды на основе следующих компонентов: глюкоза 360 г/л, протеин 80г/л, NaHCO3 24г/л, KH2PO4 14 г/л, NH4Cl 60 г/л, CaCl2 18 г/л, MgSO4.7H2O 24 г/л. Интервал рН 7,4±0,4. Показатель ХПК составил 300±150 г/л. . [57].
Для создания синтетических сточных вод моделирующих сточные воды текстильных предприятий был выбран следующий компонентный состав: КН2РО4 8,5 г/л, К2НРО4 21,75 г/л, Na2HPO4 .7H2O 50,3 г/л, NH4Cl 0,5 г/л , NaOH 60 г/л, HCl 0,1 мл/л. А также компоненты: В - CaCl2 27,5 г/л, С - MgSO4. 7H2O 22,5 г/л, D - FeCl3.6Н2О 0,25 г/л которые обновляли каждые две недели. Приготовление синтетических сточных вод: компонент В 1 мл/л, компонент С 1 мл/л, компонент D 1 мл/л, NaOH 2 мл/л, NaCl 1,5 г/л, пептон 0,5 г/л, глюкоза 0,5 г/л, КН2РО4 0,5 г/л. [57]
Автор статьи «Practical field application of a novel BOD monitoring system» показывает возможность использования микробных топливных элементов для определения индекса БПК. Синтетические сточные воды были использованы для предварительной работы БПК-сенсора. Синтетической основой сточных вод явились следующие компоненты: 15 мг/л КН2РО4, 30 мг/л (NH4)2SO4, 50 мг/л MgSO4-7H2O, 3,75 мг/л CaCl2, 0,25 мг/л FeCl3-6H2O, 5,0 мг/л MnSO4-H2O, 105 мг/л NaHCO3 и 10 мл/л микроэлементных компонентов. Микроэлементные компоненты: 1,5 г/л нитрилотриуксусная кислоты, 0,1 г/л FeSO4 -7H2O, 0,1 г/л MnCl2-4H2O, 0,17 г/л CoCl2-6H2O, 0,1 г/л CaCl2-2H2O, 0,1 г/л ZnCl2, 0,02 г/л CuCl2-2H2O, 0,01 г/л H3BO3, 0,01 г/л MoNa2O4, 0,017 г/л Na2SeO3, 0,026 г/л NiSO4-6Н2О, 1 г/л NaCl и 0,1 г/л Na2WO4 -7H2O. Для полного формирования синтетических сточных воды добавляли соответствующие количества глюкозы и глутаминовой кислоты на базе раствора буфера с рН 7,0±0,2. Для предотвращения засорения микробных топливных элементов осадок суспензии частично фильтруется через фильтровальную бумагу (4 класс, удержание частиц диаметром: 20-25 μm, Ватман, США). После проведения измерений с использованием синтетических сточных вод система была применена к измерению БПК в реальных сточных водах из очистных сооружений в тех же экспериментальных условиях. Ответы на синтетические сточные воды были больше, чем ответы на реальные сточные воды с тем же значением БПК. Автор статьи объясняет этот факт наличием в реальных образцах моющих средств и токсических веществ [59]
Во многих зарбежных работах для колибровки БПК-биосенсора используют ОЕСD-синтетическую сточную воду. В работе [60] при создании БПК-датчика использовали OECD-синтетическую сточную воду. Для приготовления OECD-синтетической сточной воды в литре водопроводной воды растворяют следующие компоненты: 160 мг пептона, 110 мг мясного экстракта, 30 мг мочевины, 28 мг K2HPO4, 7 мг NaCl, 4 мг CaCl2 • 2H2O, 2 мг Mg2SO4 • 7H2O. Значение БПК5 для данной смеси было определено стандартным методом и составило 14000мг/л. Выбор OECD-синтетической сточной воды, а не раствора на основе глюкозы и глутаминовой кислоты, основан на том, что реальные образцы сточных вод содержат различные виды органических веществ с широким диапазоном молекулярных масс. Линейный диапазон ответа сенсора от значения БПК5 составил от 15 до 260 мг/л. После калибровки датчика с использованием OECD-синтетических сточных вод, был проведен анализ реальных образцов сточных вод. Средний коэффициент корреляции составил 0, 8713.
Таким образом, актуальным направлением применения биосенсоров может являться анализ интегральных характеристик водных сред. Как видно из представленных в обзоре данных, биосенсорная детекция БПК является достаточно развитым направлением аналитической биотехнологии. Биосенсорные анализаторы БПК представляют собой надежные аналитические инструменты и с успехом используются для контроля водных экосистем наряду с традиционными методами определения БПК.
В то же время в Российской Федерации отсутствует опыт промышленного выпуска анализаторов этого типа, а исследования по данной проблеме начали проводиться сравнительно недавно и не продемонстрировали существенных успехов.
Следует отметить, что несмотря на полученные зарубежными исследователями положительные результаты, поиск новых решений, обеспечивающих более высокую точность оценки индекса БПК, оперативность и воспроизводимость анализа, продолжаются.
Основными тенденциями являются повышение
стабильности, увеличение степени корреляции данных, полученных биосенсорным
методом, с данными, полученными стандартным методом оценки БПК.
2. Экспериментальная часть
.1 Культивирование клеток
микроорганизмов
Для работы использовали: клетки штамма
Debaryamyces hansenii BKM-Y-2482, полученные во Всероссийской коллекции
микроорганизмов Института биохимии и физиологии микроорганизмов РАН (Пущино).
Клетки штамма Debaryamyces hansenii BKM-Y-2482 выращивали на богатой
минеральной среде (жидкая глюкозо-пептонная питательная среда). Состав жидкой
среды: глюкоза - 10 г/дм3, пептон - 5 г/дм3, дрожжевой экстракт - 0,5 г/дм3
(Sigma, США). Среду для выращивания клеток стерилизовали автоклавированием при
давлении в 1 атмосферу в течение 45 минут. Клетки выращивали аэробно 18-20
часов в качалочных колбах объемом 750 см3 при температуре 29 оС. Затем
полученную биомассу центрифугировали при комнатной температуре при 8000 об/мин
10 минут. Далее центрифугат промывали 20 мМ фосфатным буфером рН 6,8. Осевшие
клетки рассуспендировали в свежей порции буфера, распределяли по порциям и
осаждали на центрифуге «Eppendorf» 5 минут при 8000 об/мин. Промытую биомассу
взвешивали и хранили в микропробирках при температуре -25 °С.
2.2 Иммобилизация клеток
Debaryamyces hansenii в модифицированный ПВС
Для формирования рецепторного элемента к 40 мг
дрожжей Debaryamyces hansenii добавляли 200 мкл модифицированного ПВС. Для
распределения дрожжей в пленки проводили встряхивание в течение 5 минут на
центрифуге «Sky Line». Полученную субстанцию переносили на предметное стекло и
оставляли на воздухе до полного высыхания. Последующие измерения проводились
при комнатной температуре.
2.3 Биосенсорные измерения
Принцип работы микробного сенсора на основе
кислородного электрода основан на том, что при окислении субстрата
иммобилизованными на поверхности кислородного электрода микроорганизмами
возрастает их дыхательная активность, и в приэлектродном пространстве снижается
концентрация кислорода, что регистрируется с помощью электрода (рис.11).
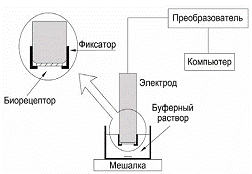
Рис. 11 - Схема биосенсора кюветного типа
Основным элементом биосенсорного анализатора
является кислородный электрод Кларка, на поверхности которого располагали
рецепторный элемент.
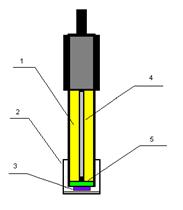
Рис. 12 - Электрод с рецепторным элементом: 1 -
раствор KCl - 30 мМ, 2 - защитный колпачок, 3 - рецепторный элемент, 4 -
платиновый электрод, 5 - полупроницаемая целлофановая мембрана
В качестве преобразователя использовали
многофункциональный анализатор Эксперт-001, в режиме «термооксиметр», что
позволило производить непрерывную регистрацию сигнала.

Рис. 13 - Внешний вид лабораторной модели
микробного биосенсора кюветного типа
Управление прибором проводилась с помощью встроенной программы «EXP2PR». Перед непосредственным измерением проводили промывку системы натрий-калиевым фосфатным буферным раствором рН = 6,8 (концентрация солей 33 мМ). Ввод пробы осуществлялся автоматическими микропипетками переменного объема (1-10мкл, 20-200мкл, 200-1000мкл, 1-5 мл) («ЛИНПИПЕТ» Россия) После окончания измерений систему снова промывали буферным раствором в течение 3 мин., до восстановления начальных параметров (концентрации кислорода).
Обработка данных проводилась в программе Exel. В
ходе измерения на мониторе компьютера отображались изменения параметров
системы, таких как зависимость концентрации кислорода от времени. Измеряемым
параметром (ответом биосенсора) являлась максимальная скорость изменения
выходного сигнала биосенсора при добавлении субстратов.
2.4 Заполнение и проверка качества
электрода
Кислородный электрод заполняли 30 мМ раствором хлорида калия. Полупроницаемая мембрана электрода - целлофан. Проверка качества электрода осуществлялась с помощью свежеприготовленного 20% раствора сульфита натрия. Данная операция носит название сульфидный тест.
При растворении сульфита натрия в воде
происходит восстановление свободного кислорода по реакции:
Na2SO3+O2=2Na2SO4
Электрод подключали к прибору «Эксперт-001» в
режиме «термоокиметр» в кювету добавляли 20% раствор сульфита натрия и
запускали процесс измерения пробы. Критерием пригодности электрода к измерениям
являлось снижение содержания кислорода в кювете до 0 мг/дм3.
2.5 Формирование рецепторного элемента
Полученную пленку разрезали на одинаковые части
размером 3×3 мм. Биорецепторный
элемент помещали на поверхность кислородного электрода типа Кларка и
фиксировали с помощью капроновой сетки.
2.6 Определение БПК5 методом разбавления
Определение БПК стандартным методом проводили по
методике описанной в ПНДФ [61]. Для определения БПК образцов браги проводили
предварительное разбавление, сточные воды анализировали без предварительного
разбавления.
2.6.1 Приготовление разбавляющей воды и растворов
Приготовление разбавляющей воды
Разбавляющую воду готовят из дистиллированной воды, полученной накануне анализа, выдержанной при температуре 20 °С; ее насыщают кислородом воздуха, аэрируя до концентрации растворенного кислорода не менее 8 мг/дм3 и не более 9мг/дм3. В разбавляющую воду добавляют фосфорные и аммонийные соли, гексагидрат хлорида железа, хлорид кальция и сульфат магния для создания устойчивой буферной системы, которая позволяет поддерживать постоянное значение рН в течение любого времени инкубации, не изменяющееся при выделении СО2 (продукт метаболизма бактерий).
Растворы солей для приготовления разбавляющей воды
Фосфатный буферный раствор рН = 7,2: 8,5 г однозамещенного фосфорнокислого калия (KH2PO4), 21,75 г двузамещенного фосфорнокислого калия (K2HPO4), 33,4 г двузамещенного фосфорнокислого натрия 7-водного (Na2HPO4·7H2O) и 1,7 г хлорида аммония (NH4Cl) растворяют в дистиллированной воде и доводят объем до 1 дм3.
Сульфат магния: 22,5 г MgSO4·7H2O ч.д.а. растворяют в дистиллированной воде, доводят объем до 1 дм3.
Хлорид железа: 0,25 г. FeCl3·6H2O ч.д.а. растворяют в дистиллированной воде, доводят объем до 1 дм3.
Хлорид кальция: 27,5 г. CaCl2 ч.д.а. безводного растворяют в дистиллированной воде, доводят объем до 1 дм3.
Растворы хранят в темноте, при комнатной температуре не более месяца. Не используют при появлении осадка.
В день анализа к 1 дм3 разбавляющей воды прибавляют 1 см3 фосфатного буферного раствора, 1 см3 раствора сульфата магния, 1 см3 раствора хлорида кальция, 1 см3 раствора хлорида железа.
Заражение микрофлорой.
В разбавляющую воду в день анализа добавляют бактериальную затравку. (При анализе сточных вод сооружений биологической очистки такой затравки не требуется). Бактериальную затравку добавляют при исследовании искусственно приготовленных растворов, производственных сточных, олиготрофных поверхностных пресных, грунтовых, глубоко очищенных и обеззараженных сточных вод.
Бактериальная затравка может отбираться из разных источников, приготовлений разбавляющей воды используется один из предлагаемых вариантов:
а) Сточные воды с городских сооружений биологической очистки, отобранные после песколовок. Добавляют 0,3-1,0 см3 на 1 дм3 разбавляющей воды.
б) Аквариумная вода. Добавляют 5,0-10,0 см3 на 1 дм3 разбавляющей воды.
в) Речная вода. Добавляют 10,0-20,0 см3 на 1 дм3 разбавляющей воды.
Проверка степени чистоты разбавляющей воды холостым опытом. При определении БПК5 две кислородные колбы заполняют разбавляющей водой, в первой определяют кислород сразу в день исследования («нулевой» день), время между разбавлением пробы и определением кислорода в «нулевой» день не должно превышать 15 мин. В во второй, которую помещают в термостат вместе с анализируемыми пробами, - через 5 суток.
Разница средней концентрации кислорода в пробе
холостого опыта нулевого дня и через 5-суточный срок инкубации не должна
превышать 0,5 мг/дм3 кислорода.
2.6.2 Выполнение измерений с разбавлением пробы
Для загрязненных речных и сточных вод с БПК5 выше 6 мг/дм3 требуется предварительное разбавление пробы. Определение производят в разбавленной пробе по разности содержания кислорода до и после инкубации в стандартных условиях. Для разбавления пробы применяют искусственно приготовленную разбавляющую воду (п. 3.5.1). При приготовлении разбавлений температура исследуемой пробы должна соответствовать температуре 18-20 °С.
Для расчета необходимых разбавлений пробы следует ожидаемое содержание БПК в пробе разделить на 4-5 (поскольку в воде после инкубации при правильном разбавлении должно остаться 4-5 мг/дм3 кислорода). Если нельзя предположить ожидаемое разбавление рассчитывается по результатам определения пермонганатной окисляемости (ХПК). Условно принимают биохимическое потребление кислорода 50% ХПК, а поскольку в воде после инкубации должно остаться 4-5 мг/дм3 кислорода, вычисленное значение (ХПК:2) делят на 4 или 5. Полученный результат показывает, во сколько раз надо разбавить анализируемую воду.
В мерную колбу вместимостью 1 дм3 наливают хорошо перемешанную испытуемую жидкость, отбирают пипеткой определенный объем и вносят в другую колбу (цилиндром отмеряются объемы больше 50 см3). Затем доливают до метки разбавляющей водой и хорошо перемешивают; полученную смесь сифоном, опущенным до дна колбы, наливают в шесть кислородных колб объемом 250 см3, закрывают пробкой, следя за тем, чтобы внутри не осталось пузырьков воздуха. Затем оставшейся смесью заполняют колпачки от колб и, наклонив колбу, вставляют их в колпачки с водой, вытесняя из них воду, чтобы не осталось пузырьков воздуха. Для каждого разбавления заполняют две колбы.
В первых двух кислородных колбах немедленно определяют кислород. Все остальные колбы помещают в термостат при 20 °С для инкубации.
Через 2, 5 сут от начала инкубации вынимают из термостата по две колбы с испытуемой водой, определяют в них растворенный кислород и содержание нитритов.
.6.3 Расчет БПК при определении с
разбавлением пробы
X = [(Cx1 - Cx2) - (Cy1 - Cy2)] N,
где, X - БПК, мг/дм3;
Сx1 - содержание растворенного кислорода в исследуемой воде до инкубации, мг/дм3;
Сx2 - то же, после инкубации, мг/дм3;
Сy1 - содержание растворенного кислорода в разбавляющей воде до инкубации, мг/дм3;