Материал: Общая химия с физкалом

означает, что концентрация вещества в объеме раствора больше, чем в поверхностном слое.
Адсорбция ПАВ ПАВ – дифильные по природе вещества, имеют
полярную (гидрофильную) и неполярную (гидрофобную) части. Например, мыло: С17Н35COONa
символ неполярной |
символ полярной |
части |
части |
ПАВ – это положительно адсорбирующиеся вещества, к ним относятся: жиры, жирные кислоты, кетоны, спирты, холестерин, мыла и другие органические соединения. При растворении таких веществ в воде происходит положительная адсорбция, сопровождающаяся накоплением вещества в поверхностном слое. Процесс выхода молекул этих веществ на поверхность очень выгоден, т.к. приводит к понижению поверхностного натяжения на границе раздела фаз. Схема адсорбции ПАВ:
Способность вещества понижать поверхностное натяжение на границе раздела фаз называется поверхностной
активностью
dσ dC
.
Правило Дюкло-Траубе
Величина поверхностной активности ПАВ – членов одного гомологического ряда органических соединений зависит от длины углеводородного радикала: удлинение ПАВ на одну группу –СН2– увеличивает поверхностную активность вещества в 3-3,5 раза.
121
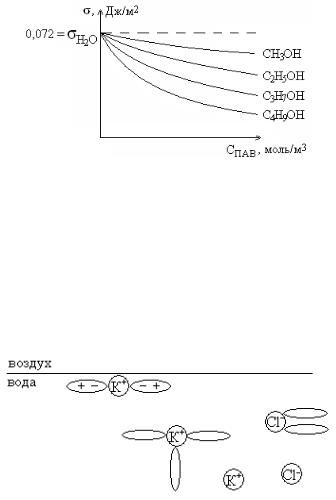
Рассмотрим правило Дюкло-Траубе на примере четырех представителей гомологического ряда спиртов.
Изотерма поверхностного натяжения:
Адсорбция ПИАВ По отношению к полярной воде такими веществами
являются электролиты: неорганические кислоты, соли, щелочи. Растворение этих веществ увеличивает поверхностное натяжение, поэтому ПИАВ будут выталкиваться из поверхностного слоя внутрь адсорбента. Такую адсорбцию называют отрицательной. Например: растворение КС1 в воде сопровождается диссоциацией соли с последующей гидратацией образующихся ионов.
Схема адсорбции ПИАВ:
Выход ионов электролита в поверхностный слой приводит к повышению поверхностного натяжения на границе жидкость – воздух. Поэтому вещества, повышающие поверхностное натяжение не содержатся в поверхностном слое.
122
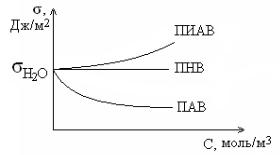
Лишь значительное увеличение концентрации ПИАВ приводит к перемещению в поверхностный слой значительного количества растворенного вещества и значительным увеличением σ.
Изотерма поверхностного натяжения – это зависимость поверхностного натяжения на границе жидкость – газ от концентрации растворенного в жидкости вещества при постоянной температуре.
8.3. Адсорбция на твердых сорбентах
Характерной особенностью твердых сорбентов является их пористость. Поглощение веществ на твердой поверхности значительно выше, чем на жидкой, т.к. на твердых сорбентах идет поглощение не только в поверхностных слоях, но и во внутренних.
При рассмотрении адсорбции из раствора на твердом теле принято различать два случая:
адсорбцию неэлектролитов, когда адсорбируются молекулы адсорбтива - молекулярная адсорбция;
адсорбцию электролитов, когда избирательно адсорбируется один из ионов электролита – ионная адсорбция.
3.1. Молекулярная адсорбция из растворов
Адсорбция на твердых сорбентах описывается теорией Лэнгмюра, основные положения которой сводятся к следующему:
123

адсорбция происходит не на всей поверхности сорбента, а только на адсорбционных центрах – вершинах неровностей и узких порах;
каждый адсорбционный центр может удерживать только одну молекулу сорбируемого вещества, что приводит к образованию мономолекулярного слоя;
процесс адсорбции обратим и носит динамический характер, т.е. одновременно с адсорбцией происходит десорбция (удаление вещества с поверхностного слоя).
Лэнгмюром было предложено уравнение для расчета величины адсорбции на твердом сорбенте.
Г Г |
С |
|
|
|
С В |
|
|
Г Г |
Р |
|
|
|
Р В |
|
-для адсорбции из растворов.
-для адсорбции газов.
Г (моль/г, моль/м2) – величина адсорбции; Г∞ – предельная адсорбция, соответствующая
образованию насыщенного мономолекулярного слоя на поверхности сорбента;
С – концентрация поглощаемого вещества (сорбтива), моль/м3, моль/л;
Р – парциальное давление газа; В – константа сорбционного равновесия.
Уравнению Лэнгмюра соответствует изотерма адсорбции. Изотерма – измерения проведены при постоянной температуре. Г∞ - определяется экспериментально по изотерме Лэнгмюра.
124
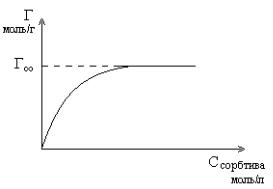
Адсорбция на границе твердое тело – газ и твердое тело
– раствор схожи по своей природе. Но при адсорбции из раствора явление сильно усложняется наличием третьего компонента – растворителя (среды), молекулы которого могут также адсорбироваться на поверхности адсорбента и, следовательно, являются конкурентами молекул адсорбтива. Т.о. адсорбция на границе раздела твердое тело – раствор – это адсорбция из смеси веществ, кроме того, необходимо учитывать взаимодействие молекул адсорбтива с молекулами растворителя.
Величина адсорбции зависит от следующих факторов:
природы сорбента;
природы сорбтива;
природы растворителя;
концентрации растворенного вещества - описывается уравнением Лэнгмюра;
температуры – с повышением температуры адсорбция из раствора уменьшается, это связано с повышением растворимости сорбтива в данном растворе.
Влияние природы адсорбента На адсорбцию из растворов сильно влияют полярность и
пористость адсорбента. Адсорбенты делятся на:
•полярные: СаСО3 (мел), силикогель xSiO2·yH2O, глина, цеолиты;
•неполярные: С (активированный уголь), сажа, тальк.
125