Материал: Общая химия с физкалом
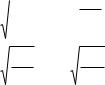
11. ПК ТРУДНОРАСТВОРИМОЙ СОЛИ AgCl ПРИ СМЕШЕ-
НИИ 10 МЛ 0,01 МОЛЬ/Л РАСТВОРА AgNO3 |
И 5 МЛ 0,1 |
МОЛЬ/Л РАСТВОРА КСl РАВНО |
|
1) 1 10 3
2) |
2,5 |
10 |
4 |
|
3) |
2,2 |
10 4
4) |
1,5 |
10 3
12. КОНЦЕНТРАЦИЯ ИОНОВ
Ag |
|
|
(МОЛЬ-ИОН/Л) В НАСЫ-
ЩЕННОМ
РАВНА
ВОДНОМ РАСТВОРЕ СОЛИ
ПР |
|
|
|
12 |
Ag |
CrO |
4 |
1,9 10 |
|
|
2 |
|
|
Ag CrO |
|
2 |
4 |
1) |
1,4 |
10 |
6 |
|
2) |
7,4 |
10 5
3) |
1,9 |
10 6
4) |
1,5 |
10 4
13. КОНЦЕНТРАЦИЯ ИОНОВ
Fe |
2 |
|
В НАСЫЩЕННОМ
РАСТВОРЕ НИЕ ПР
1) 1,2 10 9
FeS РАВНА |
6 10 |
10 |
моль ион/ л . |
ЗНАЧЕ- |
|||
|
|||||||
|
5 |
3) |
6 10 |
20 |
4) |
19 |
|
2) 2,4 10 |
|
3,6 10 |
|||||
14. КОНЦЕНТРАЦИЯ ИОНОВ Са2+ ВЫШЕ НАД ОСАДКОМ
1) CaF2 2) CaC2O4 3) CaCO3 4) CaSO4
15.РАСТВОРИМОСТЬ CdS МОЖНО РАССЧИТАТЬ ПО ВЫРАЖЕНИЮ
1) |
3 |
|
ПР |
|
2) |
|
|||||
|
4 |
|
|
||

 ПР
ПР
3) |
4 |
ПР |
4) |
5 |
ПР |
|
|
||||
|
27 |
|
108 |
||
|
|
|
|
16. МЕНЕЕ РАСТВОРИМО СОЕДИНЕНИЕ
1) |
BaCO3; |
2) |
CoCO3; |
3) |
MgCO3; |
4) PbCO
3
.
17. РАСТВОРИМОСТЬ |
Ag2S |
В |
ВОДЕ |
СОСТАВЛЯЕТ |
|
1,08 10 7 моль / л. ЗНАЧЕНИЕ ПР СУЛЬФИДА СЕРЕБРА |
|||||
РАВНО |
|
|
|
|
|
1) 1,16 10 34 ; |
2) 1,25 10 17 ; |
3) |
5 10 21; |
4) 3,3 10 9. |
|
116
18.ВЕЛИЧИНА ПР ГИДРОКСИДА ХРОМА (III), ВЫРАЖЕННАЯ ЧЕРЕЗ РАСТВОРИМОСТЬ S (МОЛЬ/Л) ЭТОГО ГИДРОКСИДА
1) |
ПР |
4 |
; |
27S |
2)
ПР
2 |
; |
S |
3)
3 |
; |
ПР 4S |
4)
ПР 108S5.
19. РАСТВОРЕНИЕ |
ОСАДКА ФОСФАТА |
||
|
ВОЗМОЖНО В КИСЛОТЕ |
|
|
1) |
СН3СООН; 2) |
CН3СН2СООН; |
3) HNO3; |
КАЛЬЦИЯ
4) НСООН
20. РАСТВОРЕНИЕ PbJ2 ПРОИЗОЙДЕТ ПРИ ДОБАВЛЕНИИ
1) NaCl 2) Na2CO3; 3) NaJ |
4) Pb(NO3 )2. |
21.РАСТВОРЕНИЕ ОСАДКА ДОБАВЛЕНИИ
CaSO4
НЕ ПРОИЗОЙДЕТ ПРИ
1) K2CO3; 2) Ca(NO3)2;
3) |
Na |
2 |
C O |
; |
|
2 |
4 |
|
|
4) KF.
22. ОСАДОК ГИДРОКСИДА НИКЕЛЯ |
Ni(OH)2 |
|
РИТСЯ ПРИ ДОБАВЛЕНИИ РАСТВОРА |
||
1) NaOH |
2) Ni(NO3)2 |
; |
3) HCl |
4) Na2CO3. |
|
РАСТВО-
23.БУДЕТ ЛИ ОСАДОК ИОДИДА СЕРЕБРА РАСТВОРЯТЬСЯ
ВУКСУСНОЙ КИСЛОТЕ
1) Нет, Кр>1 |
2) |
Нет, Кр <1 |
3) Да, Кр<1 |
4) |
Да, Кр>1 |
Ответы к тесту на стр. 238
Тестовые задания для самоконтроля по теме VII на стр. 303 Ответы к тестовым заданиям для самоконтроля по теме VII на стр. 313
117
ТЕМА VIII. ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ. АДСОРБЦИЯ
8.1. Поверхностное натяжение: физический смысл, факторы, от которых зависит σ
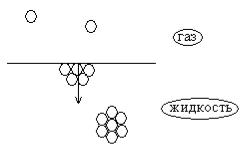
Рассмотрим границу раздела жидкость
– газ. Молекулы, находящиеся на поверхности жидкости, испытывают неодинаковое воздействие со стороны молекул жидкости и газа. Молекулы, находящиеся внутри жидкости,
окружены со всех сторон подобными. Силы, действующие на них со всех сторон, одинаковы, и равнодействующая этих сил равна нулю.
Силы межмолекулярного взаимодействия молекул жидкости, расположенных на поверхности, не скомпенсированы, их равнодействующая не равна нулю и направлена вглубь жидкости. Таким образом, энергия молекул на поверхности раздела фаз выше, чем у молекул внутри фазы. В результате возникает поверхностный слой с избыточной свободной поверхностной энергией F.
Свободная поверхностная энергия зависит от числа частиц на границе раздела и поэтому прямопропорциональна площади поверхности раздела фаз и удельной свободной поверхностной энергии (σ): F = σ·S,
S – площадь поверхности раздела фаз, м2, см2;
σ– удельная свободная поверхностная энергия
(поверхностное натяжение) – это избыточная энергия молекул единицы площади поверхности, Эрг/см2, Дж/м2.
Удельная свободная поверхностная энергия или поверхностное натяжение σ зависит от:
природы вещества;температуры;
природы граничащих фаз;
118
наличия примесей.
Поверхностное натяжение существенно зависит:
1) от природы вещества и, в первую очередь, от полярности молекул – чем выше степень полярности молекул, тем активнее они взаимодействуют друг с другом, тем выше поверхностное натяжение.
|
|
|
2 |
; |
|
|
22, 75 Эрг/см |
2 |
; |
Н |
О |
72, 75 Эрг / см |
этанола |
|
|||||
|
2 |
|
|
|
|
|
|
|
|
|
|
|
2 |
. |
|
|
|
|
|
С Н |
18, 01 Эрг / см |
|
|
|
|
|
|||
|
6 |
14 |
|
|
|
|
|
|
|
2) от температуры : |
с |
повышением температуры σ |
|||||||
снижается, т.к. при увеличении температуры жидкость переходит в пар, а при температуре кипения исчезает различие между паром и жидкостью, выравнивается энергия межмолекулярного взаимодействия, σ становится равным нулю.
3) от природы молекул пограничных фаз: σж-г ≠ σж-ж. 4) от наличия примесей.
Все вещества в зависимости от их влияния на поверхностное натяжение жидкости принято делить на три группы:
ПАВ – поверхностно-активные вещества – вещества, понижающие поверхностное натяжение на границе раздела фаз; ПИАВ – поверхностно-инактивные вещества – вещества,
повышающие поверхностное натяжение; ПНВ – поверхностно-неактивные вещества, не
изменяющие поверхностное натяжение (глицерин, сахароза). Т.о. избыточную поверхностную энергию и σ можно
снизить двумя путями:
1)уменьшить площадь поверхности раздела фаз за счет: а) слияния более мелких частиц в более крупные; б) жидкость при отсутствии внешних сил всегда стремится принять форму шара, т.к. поверхность шара это наименьшая поверхность, ограничивающая объем;
2)уменьшить величину σ за счет дополнительного поглощения молекул постороннего вещества – адсорбции.
Факторы, от которых не зависит поверхностное натя-
жение:
площадь поверхности раздела. Т.к. σ – удельная свободная поверхностная энергия, т.е. свободная поверхностная
119

энергия единицы площади поверхности, она относится к единице площади и от самой площади не зависит;
массы жидкости;
объема жидкости;
количества вещества жидкости.
8.2. Адсорбция на поверхности жидкости. Правило Дюкло-Траубе
Адсорбция – явление самопроизвольного накопления одного вещества на поверхности другого. Вещество, которое адсорбируется называется адсорбтивом; вещество, на поверхности которого происходит адсорбция – адсорбентом.
Адсорбция на поверхности жидкостей На поверхности жидкостей могут адсорбироваться
частицы веществ, растворенных в жидкостях. Адсорбция сопровождает процесс растворения, влияя на распределение частичек растворенного вещества между поверхностными слоями растворителя и его внутренним объемом.
Адсорбцию на поверхности жидкости можно рассчитать по уравнению Гиббса:
Г |
dσ |
|
C |
, |
|
|
|
|||
|
|
|
|
|
|
|||||
|
|
|
dC |
RT |
|
|
|
|
||
Г |
- величина удельной адсорбции, моль/м2; |
|
||||||||
С |
- молярная концентрация, моль/м3; |
|
|
|||||||
dσ - |
|
|
изменение |
поверхностного |
натяжения, |
|||||
соответствующее изменению концентрации |
С; |
|
||||||||
|
dσ |
|
|
- поверхностная активность. |
|
|
||||
dC |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
||
Если |
|
с |
|
увеличением |
концентрации |
вещества |
||||
поверхностное |
|
натяжение уменьшается |
σ < |
0, то его |
||||||
адсорбция Г считается положительной (Г > 0). Это означает, что концентрация вещества в поверхностном слое больше, чем в объеме раствора.
Если с увеличением концентрации вещества поверхностное натяжение на границе раздела фаз увеличивается σ > 0, то адсорбция считается отрицательной Г < 0, это
120