Материал: Общая химия с физкалом
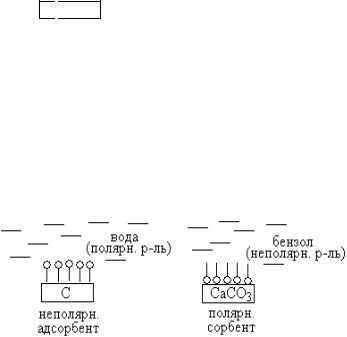
Адсорбция протекает по правилу: подобное адсорбируется на подобном – полярные сорбенты хорошо адсорбируют полярные вещества, а неполярные сорбенты – неполярные вещества. В схемах адсорбции адсорбент изображается С 
 СаСО3.
СаСО3.
Влияние природы сорбтива По своей природе сорбтивы также делятся на:
•полярные – это электролиты – о;
•неполярные – УВ: ароматические, алифатические – | ;
•дифильные – ПАВ: красители, спирты, карбоновые
кислоты и их соли – 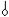 .
.
Дифильные молекулы ПАВ должны ориентироваться на границе раздела адсорбент – среда таким образом, чтобы полярная часть молекулы была обращена к полярной фазе, а неполярная часть – к неполярной. Воздух считается неполярной фазой, а вода – полярной.
Влияние природы растворителя Адсорбируемость одного и того же адсорбтива сильно
зависит от полярности адсорбента и среды. При этом можно исходить из правила уравнивания полярностей, сформулированного Ребиндером. Адсорбция растворенного
вещества наступает в том случае, если значения полярности адсорбтива лежит между значениями полярностей адсорбента и растворителя. Из правила уравнивания полярностей вытекает, что чем больше разность полярностей между адсорбтивом и растворителем, т.е. чем меньше растворимость вещества, тем лучше оно будет адсорбироваться.
Растворители по своей природе делятся на:
126
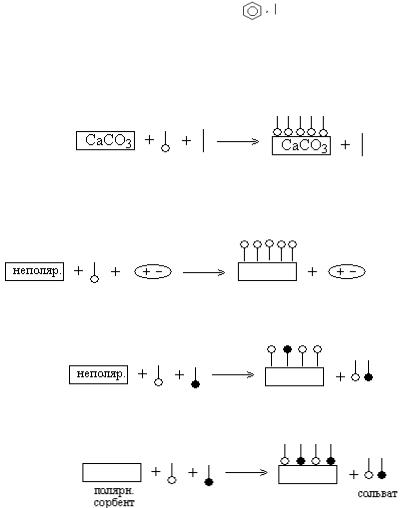
полярные – вода 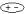
неполярные (бензол, УВ) –
дифильные (спирт) – 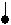
Отдельные случаи адсорбции 1. Адсорбция дифильного вещества из неполярного
растворителя на полярном адсорбенте. Схема адсорбции:
Адсорбция полная, схема подчиняется правилу Ребиндера.
2. Адсорбция дифильного вещества из полярного растворителя на неполярном сорбенте.
Схема адсорбции:
Адсорбция полная, схема подчиняется правилу Ребиндера.
3. Адсорбция дифильного вещества из дифильного растворителя.
Полярность растворителя близка к полярности сорбента, при поглощении растворитель конкурирует с сорбтивом. Сорбтив и растворитель образуют прочный сольват.
Чем среде идет адсорбция. Чем выше сродство между растворителем
и сорбтивом, тем хуже сорбтив поглощается на твердом сорбенте, удерживаясь в растворителе в виде прочного сольвата.
Молекулярная адсорбция из раствора широко используется в медицинской практике. Так, при отравлениях обычно используется активированный уголь, адсорбирующий газы, алкалоиды, барбитураты, токсины из пищеварительной
127
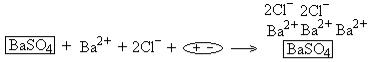
системы. В санитарно-гигиенической практике молекулярная адсорбция используется для очистки питьевой воды и сточных вод промышленных предприятий.
3.2. Ионная адсорбция
В зависимости от природы сорбента процесс адсорбции ионов электролита представлен двумя видами: ионной избирательной адсорбцией и ионообменной адсорбцией.
Механизм ионной адсорбции – электростатический за счет сродства между полярным сорбентом и ионами сорбтива. На величину ионной адсорбции оказывают влияние знак заряда иона и плотность заряда на поверхности гидратированного иона. Плотность заряда иона растет с повышением величины заряда иона и с уменьшением радиуса гидратированного иона. Избирательная ионная адсорбция подчиняется правилу Панета-Фаянса:
1.На поверхности твердого полярного сорбента преимущественно адсорбируются те ионы, которые входят
всостав кристаллической решетки сорбента или близкие к ним по природе и свойствам.
2.На заряженной поверхности сорбента могут дополнительно сорбироваться противоположные по знаку ионы.
Приведем пример: рассмотрим адсорбцию из водного
раствора ВаС12 на поверхности полярного сорбента – BaSO4; схема адсорбции: ВаС12 р-р → Ва2+ + 2С1-
При ионообменной адсорбции ионы растворенного электролита эквивалентно обмениваются на ионы того же знака заряда из сорбента. Сорбенты в данном случае получили название ионообменников (ионитов).
Если сорбент способен к обмену катионов, то он называется катионитом (R-H, R-Na, R-K); если он
128
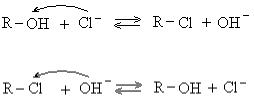
обменивается анионами, то называется анионитом (R-OH, R-Cl и др.).
Способность ионита к обмену зависит от структуры ионита и свойств ионов электролита в растворе. Количественно способность ионитов к обмену оценивается величиной обменной емкости, которая выражается числом моль-экв ионов, которое может обменивать 1 г сухого ионита или 1 см3 набухшего ионита.
Ионообменная адсорбция является эквивалентным и равновесным процессом и проходит обычно в две стадии:
поглощение ионов из раствора на ионите;
десорбция (элюирование) ионов из сорбента с последующим восстановлением структуры сорбента.
Ионообменная адсорбция лежит в основе извлечения ионов электролита из какого-либо раствора. Например, для извлечения Сl--ионов из мочи используются аниониты, работа которых может быть представлена следующим образом:
1 стадия:
В результате этого процесса рН вытекающей из анионита жидкости будет больше 7 (щелочная среда).
2 стадия:
Для извлечения сорбированных анионитом С1--ионов через колонку с сорбентом пропускают раствор натриевой щелочи – ионы ОН- вытесняют С1--ионы. Последние обнаруживаются в вытекающей жидкости, называемой элюатом, с помощью качественной реакции с нитратом серебра: Ag+ + Cl- = AgCl↓ - белый творожистый осадок.
129
ТЕСТОВЫЕ ЗАДАНИЯ К ТЕМЕ VIII. ПОВЕРХНОСТНЫЕ ЯВЛЕНИЯ. АДСОРБЦИЯ
Выберите один правильный ответ
1. НАИБОЛЬШЕЕ ЗНАЧЕНИЕ ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ σ НА ГРАНИЦЕ С ВОЗДУХОМ ИМЕЕТ ЖИДКОСТЬ
1) |
С2Н5ОН |
2) |
Н2О |
3) раствор КСl |
|
4) |
С3Н7ОН |
2. ПОВЕРХНОСТНОЕ |
НАТЯЖЕНИЕ ЖИДКОСТИ НЕ |
||
ЗАВИСИТ ОТ |
|
|
|
1) |
наличия примеси |
2) |
объема жидкости |
3) |
температуры |
4) |
природы жидкости |
3. ПАВ ПО ОТНОШЕНИЮ К ВОДЕ ЯВЛЯЕТСЯ
1) |
Na |
3 |
PO |
4 |
|
2) |
K |
2 |
CO |
3 |
3) |
C17H35COONa |
4) |
NH |
4
NO3
4. В СОСТАВЕ МОЧИ ПАВ ЯВЛЯЕТСЯ
1) соли желчных кислот |
2) NH4Cl |
3) Na3PO4 |
4) (NH4 )2 HPO4 |
5. ПРИ ДОБАВЛЕНИИ ПИАВ К ВОДЕ:
1) |
σр ра |
σH |
O |
2) |
σр ра |
σH |
O |
|
|
|
|
|
|
|
|
6. ФИЗИЧЕСКИЙ |
|
|
СМЫСЛ |
|
|||
НАТЯЖЕНИЯ
3) |
р ра |
H |
O |
|
|
2 |
|
ПОВЕРХНОСТНОГО
1)энергия, приходящаяся на единицу поверхности жидкой фазы
2)сила, приходящаяся на единицу поверхности жидкой фазы
3)энергия одного моля жидкости
130