Материал: Общая химия с физкалом
4)число моль адсорбтива в 1 литре жидкой фазы
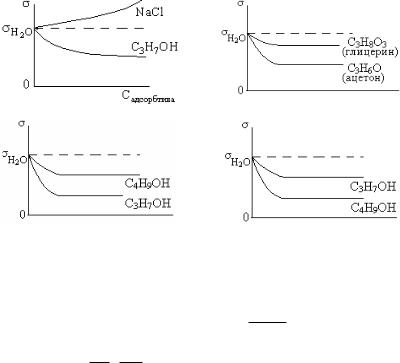
7.АКТИВНОСТЬ ПАВ ПРИ УВЕЛИЧЕНИИ УГЛЕВОДОРОДНОГО РАДИКАЛА НА ГРУППУ ( СН2 )
1)увеличивается примерно в 3 раза
2)не изменяется
3)уменьшается примерно в 3 раза
4)уменьшается примерно в 6 раз
8.ПРАВИЛО ДЮКЛО-ТРАУБЕ ИЛЛЮСТРИРУЕТ ИЗОТЕРМА ПОВЕРХНОСТНОГО НАТЯЖЕНИЯ
1) |
2) |
3) |
4) |
9.УРАВНЕНИЕ ДЛЯ РАСЧЕТА ВЕЛИЧИНЫ АДСОРБЦИИ НА ПОВЕРХНОСТИ ЖИДКОЙ ФАЗЫ
1) mg = σ·2πr;
3) Г d C ; dC RT
2) |
Г |
4) Г
Г |
|
|
С |
||
|
С В |
||||
|
|
||||
|
|
|
|||
Г |
Р |
||||
|
. |
||||
Р В |
|||||
;
131
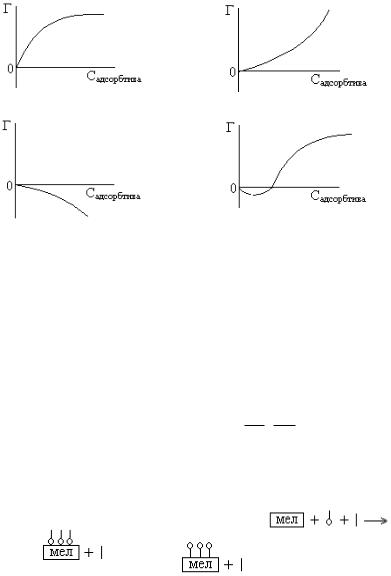
10.АДСОРБЦИИ ПАВ НА ПОВЕРХНОСТИ ЖИДКОЙ ФАЗЫ СООТВЕТСТВУЕТ ИЗОТЕРМА АДСОРБЦИИ
1) |
2) |
3) |
4) |
11.ПОВЫШЕННОМУ СОДЕРЖАНИЮ В МОЧЕ СОЛЕЙ ЖЕЛЧНОЙ КИСЛОТЫ (σ МОЧИ В НОРМЕ 57-68
Эрг / см |
2 |
) СООТВЕТСТВУЕТ ЗНАЧЕНИЕ σ |
|
|
|||
1) 78 |
|
2) 71 |
3) 63 |
(Эрг / см |
2 |
) |
|
||
4) 53 |
|
|
12.ВЕЛИЧИНА АДСОРБЦИИ НА ПОВЕРХНОСТИ ТВЕРДОГО СОРБЕНТА
1) рассчитывается по формуле Г Г |
Р |
|
|
||
Р В |
||
|
2)рассчитывается по формуле Г dCd RTC
3)определяется по изменению поверхностного натяжения
4)берется в справочных таблицах
13.ПРАВАЯ ЧАСТЬ СХЕМЫ АДСОРБЦИИ:
1) |
2) |
132
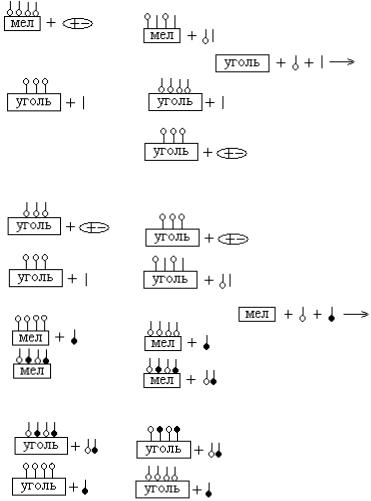
3) |
4) |
14. ПРАВАЯ ЧАСТЬ СХЕМЫ АДСОРБЦИИ
1) |
2) |
3)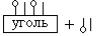 4)
4)
15. ПРАВАЯ ЧАСТЬ СХЕМЫ АДСОРБЦИИ 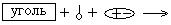
1) |
2) |
3) |
4) |
16. ПРАВАЯ ЧАСТЬ СХЕМЫ АДСОРБЦИИ
1) |
2) |
3) |
4) |
17. ПРАВАЯ ЧАСТЬ СХЕМЫ АДСОРБЦИИ 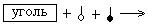
1) |
2) |
3) |
4) |
18.ПАРА «РАСТВОРИТЕЛЬ + АДСОРБЕНТ», НЕОБХОДИ-
МЫЕ ДЛЯ ПОЛНОГО РАЗДЕЛЕНИЯ СМЕСИ ТВЕРДЫХ ДИФИЛЬНОГО ( 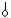 ) И НЕПОЛЯРНОГО (|) ВЕЩЕСТВ (РАСТВОРИТЕЛЬ РАСТВОРЯЕТ ОБА ВЕЩЕСТВА, А НА ТВЕРДОМ АДСОРБЕНТЕ ПОЛНОСТЬЮ АДСОРБИРУЕТСЯ ТОЛЬКО ОДНО ИЗ НИХ)
) И НЕПОЛЯРНОГО (|) ВЕЩЕСТВ (РАСТВОРИТЕЛЬ РАСТВОРЯЕТ ОБА ВЕЩЕСТВА, А НА ТВЕРДОМ АДСОРБЕНТЕ ПОЛНОСТЬЮ АДСОРБИРУЕТСЯ ТОЛЬКО ОДНО ИЗ НИХ)
133
1) |
2) |
3) |
4) |
19. ИЗБИРАТЕЛЬНО АДСОРБИРУЕТСЯ НА ПОВЕРХНОСТИ
PbSO4 |
ИЗ ВОДНОГО РАСТВОРА |
1) Na2SO4 |
2) НСООН 3) NaCl |
4) |
CH |
3 |
COOH |
|
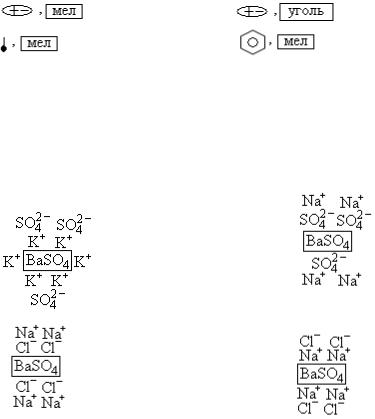
20. ИЗБИРАТЕЛЬНУЮ АДСОРБЦИЮ В ВОДНОМ РАСТВОРЕ НА ТВЕРДОМ СОРБЕНТЕ BASO4 ИЛЛЮСТРИРУЕТ СХЕМА
1) |
2) |
3) |
4) |
Ответы к тесту на стр. 253
Тестовые задания для самоконтроля по теме VIII на стр. 305 Ответы к тестовым заданиям для самоконтроля по теме VIII на стр. 313
ТЕМА IX. ДИСПЕРСНЫЕ СИСТЕМЫ
9.1. Классификация дисперсных систем
Фаза – часть системы одного состава, одинаковых физических свойств, ограниченная от других частей
134
поверхностью раздела. Систему, состоящую из одной фазы, называют гомогенной. Гетерогенная система состоит из двух и более фаз. Гетерогенную систему, в которой одна из фаз представлена в виде частиц микроскопических размеров, называют микрогетерогенной. Гетерогенная система может содержать частицы значительно меньших размеров в сравнении с видимыми в оптический микроскоп. Такие частицы наблюдают с помощью ультрамикроскопа. Систему, содержащую столь малые частицы, называют ультрамикрогетерогенной. По предложению Оствальда и Веймарна, фазу, входящую в микрогетерогенную и ультрамикрогетерогенную систему в виде мелких частиц, называют дисперсной.
Микрогетерогенные и ультрамикрогетерогенные системы – представители особого класса гетерогенных систем, называемых дисперсными системами.
Коллоидная химия – это наука о свойствах гетерогенных высокодисперсных систем и о протекающих в них про-цессах.
Дисперсными называются системы, в которых в одном веществе (дисперсионной среде ДС) распределено (диспергировано) другое вещество (дисперсная фаза ДФ).
Для характеристики дисперсных систем используются следующие понятия.
Лиофильность – наличие высокого химического сродства частиц ДФ и ДС, в результате чего они интенсивно взаимодействуют за счет молекулярных сил.
Лиофобность – сродство частиц ДФ и ДС низкое и межмолекулярное взаимодействие либо очень слабое, либо отсутствует совсем.
Гомогенность – однородность системы, отсутствие поверхности раздела фаз.
Гетерогенность – неоднородность системы, наличие поверхности раздела фаз, что приводит к возникновению поверхностной энергии.
Устойчивость системы характеризуется временем ее жизни в практически неизменном состоянии.
135