Материал: Общая химия с физкалом
ТЕМА II.............................................................................................. |
208 |
ТЕМА III. ........................................................................................... |
215 |
ТЕМА IV............................................................................................. |
219 |
ТЕМА V. ............................................................................................. |
233 |
ТЕМА VI............................................................................................. |
241 |
ТЕМА VII. .......................................................................................... |
247 |
ТЕМА VIII. ........................................................................................ |
262 |
ТЕМА IX............................................................................................. |
271 |
ТЕМА Х. ............................................................................................. |
279 |
ТЕМА XI............................................................................................. |
286 |
ТЕСТОВЫЕ ЗАДАНИЯ ДЛЯ САМОКОНТРОЛЯ |
|
ЗНАНИЙ СТУДЕНТОВ.................................................................... |
301 |
ОТВЕТЫ К ТЕСТОВЫМ ЗАДАНИЯМ ДЛЯ |
|
САМОКОНТРОЛЯ ЗНАНИЙ СТУДЕНТОВ................................. |
325 |
ПРИЛОЖЕНИЯ ................................................................................ |
326 |
РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА ............................................. |
350 |
6

ТЕМА I. ВИДЫ КОНЦЕНТРАЦИЙ. ЗАКОН ЭКВИВАЛЕНТОВ
1.1. Моль. Молярная масса. Моль эквивалент. Молярная масса эквивалента. Расчет молярной массы эквивалента для атома и вещества.
Фактор эквивалентности
Масса вещества m измеряется в г (кг)
моль, ν (ню),– это единица количества вещества, которая содержит столько же структурных единиц (атомов, молекул, ионов), сколько атомов в 12 г изотопа углерода-12, т.е. 6,02.1023.
Количество вещества можно вычислить по формуле:
ν = m/M.
Молярная масса (М, г/моль) – это масса одного моля вещества.
Из закона постоянства состава следует, что элементы соединяются друг с другом в строго определенных количественных соотношениях. Поэтому в химию были введены понятия моль эквивалент и молярная масса эквивалента: моль эквивалент, νЭ (ню с индексом э) - это такое количество элемента или вещества, которое взаимодействует без остатка с 1 моль атомов водорода или замещает такое же количество атомов водорода в химических реакциях.
Молярная масса эквивалента вещества (Х) (МЭ, г/моль экв) - это масса одного моль эквивалента вещества. Число моль эквивалентов можно вычислить по формуле: νЭ = m/ МЭ
Молярная масса эквивалента вещества Х:
Э |
=М( |
1 |
X)= |
1 |
M(X) |
М |
z |
z |
|||
|
|
|
|
1 z
- фактор эквивалентности, величина, показывающая какая
доля реальной частицы вещества, соответствует одному иону водорода в кислотно-основной реакции или одному электрону в окислительно-восстановительной реакции.
Молярная масса эквивалента кислоты рассчитывается как молярная масса кислоты, деленная на основность - число
7

атомов водорода в молекуле кислоты, способных замещаться на
металл или ион NH4+ с образованием соли:
М |
Э |
= |
1 |
М(кислоты) |
|
|
|||||
кислоты |
z |
||||
|
|
|
|||
|
|
|
|
Например, для одноосновных кислот, соляной НСl, азотной НNО3, уксусной СН3СООН и т.д. молярная масса эквивалента будет равна их молярной массе (т.к. z =1):
МЭНСl = 36,5/1 = 36,5 г/моль экв;
Э |
|
М |
СООН |
СН |
|
3 |
|
60 /1 60 г/моль экв
;
М |
Э |
63 /1 |
63 г/моль экв. |
HNO |
|||
|
3 |
|
|
Для двухосновных кислот, сернистой Н2SО3, серной Н2SО4, угольной Н2СО3, сероводородной H2S и т.д. молярная масса эквивалента равна их молярной массе, деленной на 2
(z=2):
Э |
|
|
= 82/2 = 41 г/моль экв; |
МH |
SO |
||
|
2 |
|
3 |
Э |
|
|
= 98/2 = 49 г/моль экв; |
МH |
SO |
||
|
2 |
|
4 |
МЭH |
|
СO |
= 62/2 = 31 г/моль экв; |
|
2 |
|
3 |
Э |
|
S = 34/2 = 16 г/моль экв |
|
МH |
|||
|
2 |
|
|
Для трехосновной фосфорной кислоты Н3РО4 молярная масса эквивалента равна молярной массе, деленной на 3 (т.к z = 3):
МЭH3РO4 = 98/3 = 32,7г/моль экв.
Молярная масса эквивалента основания
рассчитывается как молярная масса основания, деленная на кислотность - число групп ОН в основании, способных замещаться на кислотный остаток:
МЭоснования = 1z М(основания)
Например, для однокислотных оснований гидроксида натрия NаОН, гидроксида калия КОН и т.д. молярная масса эквивалента равна его молярной массе (т.к. z = 1):
МЭNаОН = 40/1 = 40 г/моль экв;
8

МЭКОН = 56/1 = 56 г/моль экв.
Для двухкислотных оснований гидроксида кальция Са(ОН)2, гидроксида бария Ва(ОН)2 и т.д. молярная масса эквивалента равна его молярной массе, деленной на 2 (z = 2):
М М
Э Са (ОН)2
Э Ва(ОН)2
=74/2 = 37 г/моль экв;
=171/2 = 85,5 г/моль экв.
Молярная масса эквивалента соли рассчитывается как молярная масса соли, деленная на число катионов, умноженное
на заряд катиона:
М |
Э |
= |
1 |
М |
|
|
|
|
|||||
соли |
z |
(соли) |
||||
|
|
|
||||
|
|
|
|
|
Например, молярная масса эквивалента карбоната калия равна его молярной массе, деленной на 2 (число катионов), умноженное на 1 (заряд катиона) (т.к. z = 2.1 = 2):
МЭК2СО3 = 138/2∙1 = 69 г/моль экв.
Молярная масса эквивалента оксида рассчитывается как молярная масса оксида, деленная на число атомов кислорода, умноженное на 2 (валентность атома кислорода):
Мэоксида= |
1 |
Моксида |
|
z |
|||
|
|
Например, молярные массы эквивалента оксидов фосфора Р2О3 и Р2О5 соответственно равны:
Мэ Р2О3= 110/(3 ∙ 2) = 18,3 г/моль экв Мэ Р2О5= 142/(5 ∙ 2) =14,2 г/моль экв
Молярные массы эквивалента химических соединений могут иметь переменные значения в зависимости от характера превращения в реакциях. Тот факт, что одно и то же вещество может иметь различный фактор эквивалентности в различных реакциях, особенно наглядно можно видеть на примере взаимодействия многоосновных кислот с основаниями. Например, возьмем взаимодействие фосфорной кислоты с гидроксидом калия. При этом может образовываться либо средняя соль, либо кислые соли. При этом фактор эквивалентности фосфорной кислоты имеет различные значения.
Н3РО4 + 3КОН→К3РО4 + 3Н2О
9
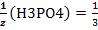 , т.к. одной молекуле кислоты в данной
, т.к. одной молекуле кислоты в данной
кислотно-основной реакции соответствует 3 иона водорода. Н3РО4 + 2КОН→К2НРО4 + 2Н2О
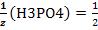 , т.к. одной молекуле кислоты в данной
, т.к. одной молекуле кислоты в данной
кислотно-основной реакции соответствует 2 иона водорода. Н3РО4 + КОН→КН2РО4 + Н2О
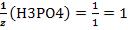 , т.к. одной молекуле кислоты в данной кислотно-основной реакции соответствует 1 ион водорода.
, т.к. одной молекуле кислоты в данной кислотно-основной реакции соответствует 1 ион водорода.
1.2. Растворы. Способы выражения концентрации растворов
Раствор − это гомогенная система переменного состава, состоящая из двух и более компонентов. Обязательными компонентами раствора (р-ра) являются растворитель (р-ль) и растворенное вещество (р.в.)
Важнейшей характеристикой раствора является концентрация, т.е. относительное содержание каждого из компонентов раствора. Существуют следующие наиболее часто употребляемые способы выражения концентрации раствора: массовая доля, молярная (молярность), молярная концентрация эквивалента (нормальность), моляльная (моляльность), титр и мольная доля. Каждый способ выражения концентрации имеет свои преимущества для определенных целей. Все способы выражения растворов представлены в таблице.
10