Материал: Неорганическая химия - курс лекций-презентаций

Пример 5
В одном моле железа содержится число Авогадро молекул:
В 56 граммах Fe — 6,02 1023 молекул,
а в 2,8 г Fe |
— Х молекул. |
х = 2,8 6,02 1023 =3,01 1022 молекул. 56
Ответ: m0 =9,3 10−23 г,
N =3,01 1022 молекул.

Пример 6
Закончите уравнение реакции и оцените окислительно-восстановительные свойства
FeSO4. Расставьте коэффициенты методом электронно-ионного баланса.
+2 |
+7 |
+2 |
|
|
|
FeSO4 + KMnO4 + H2 SO4 → MnSO4 +Fe...2 (SO4 )3 + Н2О. |
|||||
|
|
Решение. Расставим степень окисления |
|
||
|
|
элементов. |
|
|
|
|
|
Видим, что КMnO4 |
— окислитель, значит |
||
|
|
FeSO4— восстановитель. |
|
|
|
5 |
|
2Fe2+ −2е = 2Fe3+, в− ль, |
|
|
|
|
|
|
|||
2 |
|
MnO− +5е +8H + |
→ Mn2+ +4Н |
О, о |
− ль. |
|
|
4 |
2 |
|
|
|
|
|
|
||


Пример 8
Сколько тонн красного железняка,
содержащего 65 % Fe2O3, необходимо взять, чтобы получить одну тонну чугуна, содержащего 91 % (масс)
железа.
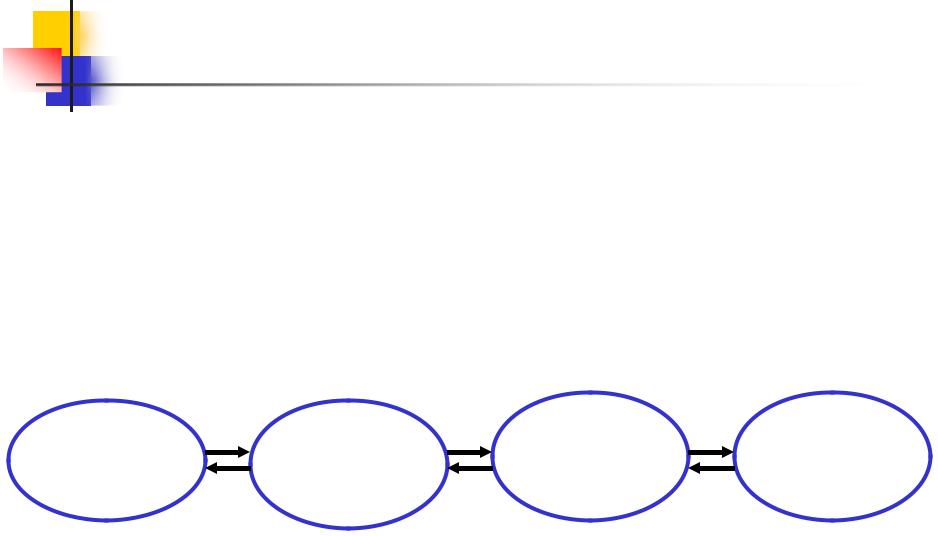
Решение. Составим алгоритм процесса:
|
3 |
2 |
1 |
Руда |
Fe2O3 |
2 Fe |
чугун |
65% Fe2O3 |
|
|
1т (91 % Fe) |
 Опишите
Опишите