Материал: Методичка. Лучевая терапия
костными метастазами в 1936 году, стронций-89 – в 1942. Радионуклиды могут использоваться и в составе тумороспецифических радиофармпрепаратов для лечения метастазов опухолей конкретных локализаций (например, рака щитовидной железы) либо первичных костных опухолей, в частности, остеосаркомы. Но наиболее распространённый вариант – применение остеотропных радиофармпрепаратов для воздействия на костные метастатические очаги, о чём и пойдёт речь ниже.
В идеале оптимальный в терапевтическом отношении радионуклид должен соответствовать следующим требованиям:
-обладать селективным захватом и пролонгированным удержанием в метастатическом очаге по сравнению с нормальной тканью;
-быстрым клиренсом из мягких тканей и нормальной кости;
-возможностью визуализации процесса распределения в организме с использованием традиционной сцинтиграфии;
-простотой процесса производства;
-радиохимической стабильностью;
-простотой транспортировки;
-адекватной стоимостью;
-низкой токсичностью;
-радиационной безопасностью.
Возможно, в настоящее время нет ни одного радиофармпрепарата,
идеально соответствующего вышеуказанным требованиям, но, тем не менее,
достаточно большой спектр радиоактивных изотопов применяется, и весьма успешно, с паллиативной целью – просто к выбору того или иного радионуклида желательно подходить творчески.
Остеотропные радионуклиды, их биофизические характеристики
и клиническая эффективность
41
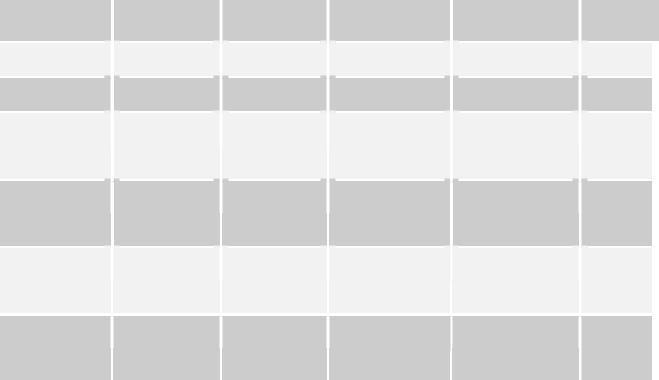
В таблице перечислены наиболее популярные и доступные для применения в системной лучевой терапии костных метастазов радиофармпрепараты, а также их физические характеристики. «Старина» фосфор-32, используемый в виде ортофосфата, и не менее проверенный временем стронций-89-хлорид являются чистыми бета-эмиттерами с относительно долгим периодом полураспада. Рений-186
гидроксиэтилендифосфонат (HEDP), рений-188 HEDP и самарий-153
этилендиаминтетраметиленфосфонат (EDTMP) имеют значительно более короткие периоды полураспада, а также гамма-излучение в своём спектре,
что позволяет обеспечить сцинтиграфическую визуализацию распределения радиофармпрепарата после его введения в организм больного. Максимальный пробег бета-частиц этих изотопов исчисляется миллиметрами, тогда как олово-117m в составе DTPA (диэтилентриаминпентауксусной кислоты) и
радий-223-фосфат, испуская поток электронов и альфа-частиц соответственно, обладают минимальным пробегом в тканях.
Таблица 4.
Остеотропные радиофармпрепараты и их физические характеристики
Радионуклид |
Химическая |
Период |
Максимальная |
Максимальный |
Гамма- |
|
форма |
полураспада |
энергия |
пробег |
эмиссия |
Р-32 |
ортофосфат |
14,3 дня |
β 1,7 МэВ |
8,5 мм |
нет |
Sr-89 |
хлорид |
50,5 дней |
β 1,4 МэВ |
7 мм |
нет |
Re-186 |
HEDP |
3,7 дней |
β 1,07 МэВ |
5 мм |
137 |
|
|
|
|
|
кэВ |
Re-188 |
HEDP |
16,9 ч |
β 2,1 МэВ |
10 мм |
155 |
|
|
|
|
|
кэВ |
Sm-153 |
EDTMP |
1,9 дней |
β 0,81 МэВ |
4 мм |
103 |
|
|
|
|
|
кэВ |
Sn-117m |
DTPA |
13,6 дней |
℮ 0,16 МэВ |
0,3 мм |
159 |
|
|
|
|
|
кэВ |
42

Ra-223 |
|
фосфат |
|
11,4 дня |
|
α 5,78 МэВ |
|
<10 нм |
|
|
154 |
|
|
|
|
|
|
|
|
|
|
|
|
кэВ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Выбор радиофармперапарата может определяться многими факторами, и прежде всего – клинической ситуацией, в частности,
распространённостью метастатического процесса, размером очагов поражения в костях, состоянием костномозгового кроветворения, о котором косвенно можно судить по анализам периферической крови; не будем забывать и о доступности тех или иных РФП. Например, пациенты с ограниченным количеством костных метастазов с умеренным болевым синдромом и достаточным резервом костномозгового кроветворения могут быть успешно пролечены с использованием хлорида стронция-89 или ортофосфата фосфора-32. В другой ситуации, пациентам с распространённым метастатическим процессом, сниженной функцией костного мозга и/или крайней необходимостью максимально быстрого развития противоболевого эффекта вследствие выраженности болевого синдрома – им более предпочтительны Re-186-HEDP или Sm-153-EDTMP. В рекомендованных дозах все вышеуказанные радиофармпрепараты (может быть, за исключением миелотоксичного фосфора-32) могут быть использованы без высокого риска развития нежелательных побочных эффектов.
Интересно, что дозиметрические исследования после введения некоторых из обозначенных агентов показали весьма благоприятное распределение поглощённой дозы ионизирующего излучения между патологическим очагом, нормальной костью и костным мозгом (см. табл. 4),
то есть костный метастатический очаг после одной инъекции радиофармпрепарата получает дозу, адекватную таковой после курса дистанционного облучения, тогда как нормальная кость и кроветворная ткань облучаются в разы меньше! Это ли не величайшее преимущество радионуклидной лучевой терапии!
Таблица 5.
43
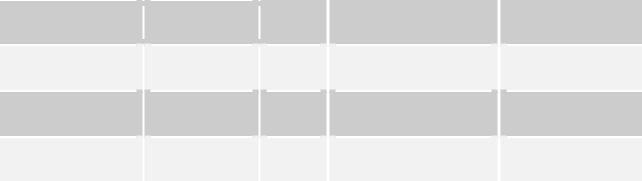
Распределение поглощённой дозы излучения в костном
метастатическом очаге, нормальной кости и костном мозге
Радионуклид |
Активность |
Доза в |
Доза в |
Доза в костном |
|
очаге |
нормальной кости |
мозге |
|||
|
|
||||
Sr-89 |
150 MБк |
35 Гр |
2,6 Гр |
1,7 Гр |
|
Re-186-HEDP |
1295 MБк |
40 Гр |
1,8 Гр |
1,7 Гр |
|
Sm-153-EDTMP |
2590 MБк |
87 Гр |
17,5 Гр |
4 Гр |
Основным показанием к радионуклидной терапии являются рефрактерные боли вследствие наличия костных метастазов преимущественно остеобластического или смешанного типа рака предстательной железы и молочной железы, а также других опухолей в случае регистрации на сцинтиграмме выраженного захвата вокруг очага метастазирования. Как правило, причиной неэффективности лечения является неадекватный отбор пациентов; остеосцинтиграфия позволяет определить показания к радионуклидной терапии более точно.
Итак, суть применения остеотропных радионуклидов – в селективном подведении дозы ионизирующего излучения к очагам усиленной остеобластической активности с одновременным воздействием как на болезненные, так и на асимптоматические костные метастазы. Основной мишенью в костном метастазе для радиофармпрепарата является кристалл гидроксиапатита (Са-ОН-апатит), с которым он и образует комплекс. В
настоящее время существует два основных химических класса терапевтических остеотропных радиофармпрепаратов – катионоактивные
(аналоги кальция) и анионоактивные (фосфонаты). К первым относятся хлорид стронция-89 и хлорид радия-223, ко вторым – все остальные известные остеотропные радиофармпрепараты.
44
К настоящему моменту опубликовано огромное количество исследований, оценивающих эффективность различных остеотропных радиофармпрепаратов в паллиативном лечении больных с метастазами в кости. Однако результаты варьируются в весьма широких пределах, прежде всего по причине отсутствия идентичности при отборе пациентов, а также избранных параметров оценки. Как правило, наилучшие результаты лечения наблюдались у больных с множественными костными очагами остеобластического типа и выраженным болевым синдромом, но без явных механических нарушений (патологический перелом, компрессия спинного мозга). В целом же, положительный эффект данного вида паллиативного лечения был отмечен приблизительно у 75% больных, а у четверти всех пролеченных пациентов развивался полный противоболевой эффект.
Временная вспышка болевого синдрома после введения РФП зарегистрирована примерно у половины больных; зачастую она является положительным прогностическим фактором, предвестником развития более выраженного противоболевого эффекта, хотя не все авторы поддерживают эту мысль. Наиболее часто встречаемое осложнение лечения – миелосупрессия, развивающаяся, как правило, на 2-6 неделе лечения, однако частота встречаемости и выраженность этого осложнения напрямую зависит от выбора радионуклида. Так, если при использовании фосфора-32
миелосупрессия наблюдается у большинства пациентов (вплоть до панцитопении), то применение олова-117m или радия-223, эмиттеров электронов и альфа-частиц с коротким и ультракоротким пробегом в тканях,
приводит к развитию минимальной миелосупрессии у небольшого количества больных.
В таблице 6 приведены сводные данные в отношении эффективности лечения радиоактивными изотопами.
45