Материал: Методичка. Лучевая терапия
лечения, стоит рассмотреть вопрос о хирургическом иссечении. Крупные метастазы в лимфоузлах шеи (более 1 см), как правило, лишь частично отвечают на лечение радиоактивным йодом, а посему операция должна быть предложена, прежде всего, как терапия первой линии.
3) Радиоактивный йод-131 в лечении отдалённых метастазов
Наиболее часто данный вид опухоли метастазирует в лёгкие и кости, и
происходит это, как правило, гематогенным путём. Терапия йодом-131
применялась в лечении отдалённых метастазов высокодифференцированного рака щитовидной железы в течение 50 лет и более. Стандартной процедурой,
предшествующей лечению, является отказ от использования гормонов щитовидной железы с целью поднятия уровня ТТГ. И опять-таки нет очевидных данных, что более высокие уровни ТТГ (свыше 25-30 мЕд/л)
обеспечивают лучшие результаты радионуклидной терапии. Назначаемые дозы препарата могут быть определены либо эмпирическим путём (как правило, от 3.7 до 11.1 ГБк), либо в соответствии с дозиметрическими исследованиями.
Schlumberger et al. в ретроспективном анализе результатов лечения
394 больных с отдалёнными метастазами рака щитовидной железы, которые были пролечены с помощью радиоактивного йода-131, показали, что у 46%
пациентов определялось полное отсутствие захвата радиофармпрепарата после проведённого лечения; у них же зарегистрированы наилучшие показатели выживаемости. Факторами, определяющими лучший ответ на лечение, явились молодой возраст и малый размер очагов, особенно в случае диффузных микроскопических очагов в лёгких. Эти данные были подтверждены последующими исследованиями.
Рис. 5 Пример успешного лечения множественных метастазов рака щитовидной железы в лёгких методом повторных введений радиоактивного йода 131: А) сцинтиграфия до начала лечения: диффузный захват йода-131 вследствие диффузного поражения лёгких; В) сцинтиграфия после двух
51
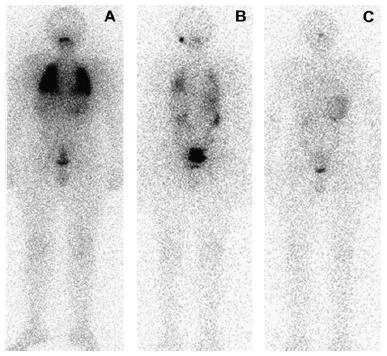
введений йода-131, указывающая на уменьшение захвата радиоактивного йода-131; С) после трех введений радиофармпрепарата: отсутствие захвата йода, означающее полный эффект лечения
Контрольные вопросы:
1.Дайте определение дистанционной и контактной лучевой терапии.
2.В лечении опухолей каких локализаций применяется внутриполостной метод? Внутрипросветная лучевая терапия? Интерстициальное облучение?
3.В чем сущность системной лучевой терапии?
4.В чем основные преимущества системной лучевой терапии по сранению с дистанционным облучением?
5.Каковы основные показания к применению радиоактивного йода-131?
52

Глава 6
Структура курса лучевой терапии: предлучевой и лучевой период.
Любое и, в частности, лучевое лечение может быть начато только после всестороннего обследования больного. Получение подробной диагностической информации позволяет решить вопрос о возможности и целесообразности лучевой терапии и составить план лечения. В идеале вся программа будущего лечения больного, первичного или пациента с рецидивом заболевания, обговаривается на консилиуме в составе мультидисциплинарной команды врачей, в которую входят: хирург,
радиотерапевт, химиотерапевт, при необходимости – врачи смежных специальностей (диагносты, анестезиологи и др.)
Лучевая терапия может быть успешной лишь при облучении всей опухоли в необходимой дозе и в оптимальные сроки. Это главное условие эффективного лечения. Если в опухоли сохранятся жизнеспособные клетки,
то через некоторое время они могут обусловить возникновение рецидива или метастазов. На успех лечения существенно влияет и степень распространения опухолевого процесаа к началу облучения. Чем больше опухоль, тем хуже результаты лечения при прочих равных условиях.
При общем выраженном истощении больного, а также наличии выраженной сопуствующей патологии лучевая терапия ничего, кроме вреда,
не принесёт. Сопутствующие воспалительные процессы осложняют проведение курса облучения. Все это подчеркивает необходимость строго определения показаний и противопоказаний к лучевой терапии.
Основные цели, которые преследуют врачи, проводя лучевое лечение,
состоят в следующем.
Радикальное лечение предусматривает полное уничтожение опухолевых элементов, как в первичном очаге, так и в зонах возможного
53
метастазирования. При этом к опухолевому очагу, как правило, подводятся максимально возможные дозы (с учетом чувствительности окружающих тканей), а для обработки зон регионарного метастазирования – несколько меньшие (46-50 Гр).
Паллиативное лечение направлено на продление жизни больного и улучшение качества его жизни, нормализацию его состояния за счет задержки дальнейшего роста опухоли на тот или иной срок. Данное лечение преследует цель снять тяжелые клинические симптомы, обусловленные локализацией опухоли и формой её распространения (например, устранение компрессии спинного мозга при метастазах в позвоночник, болей при метастатическом поражении костей, уменьшение проявлений синдрома сдавления верхней полой вены при наличии опухоли средостения, прекращение кровоточивости из язв опухолевого характера и т.д.)
Но уничтожение всех элементов опухоли и всстановление нарушенных функций организма редко достижимы при применении одного метода лечения. Поэтому современное лечение злокачественных опухолей является,
как правило, комбинированным (в сочетании с операцией или химиотерапией) или комплексным (использование 3 и более методов специального лечения). Применение лучевой терапии на предоперационном этапе направлено на уменьшение размеров опухоли,
перевод нерезектабельной опухоли в операбельное состояние, девитализацию опухолевых клеток и предупреждение их рассеивания в операционной ране.
При этом доза должна быть достаточной для того, чтобы вызвать гибель большей части клеток опухоли и тем самым предотвратить диссеминацию их во время операции, но и не вызывать заметных изменений в нормальных тканях, приводящих к нарушению процессов заживления послеоперационных ран и увеличению послеоперационной смертности.
Задачи послеоперационной лучевой терапии – 1) «стерилизация» операционного поля от рассеянных в процессе оперативного вмешательства злокачественных клеток и их комплексов; 2) воздействие на зоны
54
субклинического распространения опухоли либо на остаточную опухоль,
определяемую визуально или микроскопически. Теоретически, с учетом механизма действия ионизирующего излучения на нормальные и опухолевые ткани проведение послеоперационного облучения представляется менее целесообразным, чем предоперационного. Это связано с тем, что наличие воспалительных явлений в зоне выполнения оперативного вмешательства,
нарушение крово-и лимфоснабжения приводят к задержке поступления кислорода к опухолевым клеткам. Одновременно радиочувствительность нормальных тканей в состоянии регенерации повышается (а именно их в большом объёме необходимо включать в мишень для послеоперационного облучения, так как нужно воздействовать на ложе опухоли,
послеоперационный рубец и зоны регионарного метастазирования). Все это приводит к заметному уменьшению радиотерапевтического интервала. К
тому же существует потенциальная опасность активного роста диссеминированных опухолевых клеток в случаях отсрочки начала облучения из-за нарушения процессов заживления послеоперационной раны.
Однако, несмотря на вышеизложенное, есть и несомненные достоинства послеоперационной лучевой терапии:
- выбор объёма и методики облучения проводят на основе данных,
полученных во время операции и после тщательного морфологического изучения удалённых тканей;
- отсутствуют факторы, оказывающие явное отрицательное влияние на заживление послеоперационной раны.
Для сохранения нормальных тканей наиболее часто в послеоперационном периоде используется методика традиционного фракционирования, по 1,8-2 Гр за сеанс до суммарной дозы 50-60 Гр, хотя в ряде ситуаций прибегают и к более интенсивным режимам фракционирования.
Существует вариант интраоперационного облучения, когда сразу после удаления опухоли проводится однократное облучение её ложа
55