Материал: Методичка. Лучевая терапия
рентгеновским излучением либо электронным пучком. При этом виде лучевого воздействия имеется реальная возможность добиться минимального облучения нормальных тканей и максимального – опухоли и зон регионарного метастазирования.
Из противопоказаний к лучевой терапии принято выделять абсолютные и относительные. Сконцентрируем внимание на абсолютных противопоказаниях, ибо они практически всегда однозначно свидетельствуют о невозможности проведения лучевой терапии в данный момент времени. К ним относятся:
-истощённое состояние больного (кахексия)
-наличие острого воспалительного процесса
-активный туберкулёз легких
-беременность
-показатели периферической крови: гемоглобин ниже 90 г/л,
лейкоциты ниже 3,0х109/л, тромбоциты ниже 100х109/л
-любые соматические заболевания в стадии декомпенсации
-перенесённый инфаркт миокарда или инфаркт мозга в первые 6
месяцев.
Присоставлении плана лучевой терапии используют три набора правил:
общие правила лучевого лечения, специальные и особые правила. Общие правила постулируют принципы лучевого лечения всех больных злокачественной опухолью. Они в конечном итоге сводятся к требованию равномерного облучения опухоли и зон регионарного метастазирования в дозе, необходимой для полной резорбции опухолевых элементов, при условии минимального воздействия на окружающие нормальные ткани.
Специальные правила отражают современные принципы лучевого лечения данного заболевания; как правило, они содержатся в виде рекомендаций в мировых или национальных руководствах (например,
56
рекомендации Европейского общества медицинских онкологов по лечению рака легкого и т.д.)
Особые правила определяют наиболее рациональную тактику лечения конкретного пациента. Они предписывают составлять план лечения на основе всех сведений о пациенте, полученных до начала лечения. Если, например,
решается вопрос о выборе суммарной дозы и интервалах между фракциями,
то они выбираются с учетом не только морфологии опухоли, но и её локализации, стадии, темпов роста, наличия предшествующего облучения,
состояния окружающих тканей, состояния больного и т.д.
Таким образом, при проведении лучевой терапии принимают во внимание физические, биологические и клинические факторы и прежде всего такие, как полный клинический диагноз, данные о радиотерапевтическом интервале, картину распределения поглощённой энергии излучения в теле больного при разных условиях облучения, возможность и целесообразность комбинации лучевых и нелучевых методов воздействия.
Курс лучевой терапии делят на три периода: предлучевой, лучевой и постлучевой.
1.Предлучевой период включает всестороннюю подготовку больного
коблучению. Её следует начинать с психологической подготовки, разъяснить пациенту необходимость данного метода воздействия, его эффективность,
возможные изменения самочувствия и некоторые лучевые осложнения.
Нужно рассказать об особенностях режима питания и поведении. Беседа с больным – это важный компонент лечения, должный вселить в него чувство надежды и уверенность в правильном выборе.
В дальнейшем пациенту – при необходимости – назначаются витамины,
санация облучаемых поверхностей и полостей, коррекция показателей крови и устранение воспалительного процесса при его наличии, рекомендуется более обильное питье и полноценный отдых.
57
Техническая предлучевая подготовка – комплекс мероприятий,
предшествующих проведению облучения злокачественных опухолей. Когда установлен диагноз злокачественной опухоли у больного, получены все основные данные относительно распространённости первичного очага и наличия отдалённых метастазов (то есть, завершён диагностический процесс),
и консилиум специалистов определил показания к проведению лучевой терапии - начинать лечение возможно лишь после качественной предлучевой подготовки. Она включает следующие взаимосвязанные последовательные этапы:
1)описание будущего лечения
2)выбор положения и метода иммобилизации больного
3)визуализация опухоли и определение облучаемых объёмов
Основная задача лучевой терапии – максимально сконцентрировать дозу ионизирующего излучения на опухоли, не затрагивая, по возможности,
окружающие здоровые ткани и критические органы, повреждение которых может привести к необратимым процессам. Для этого необходимо максимально точно визуализировать опухоль, используя все возможные методы для этого (УЗИ, КТ, МРТ, ПЭТ (ПЭТ/КТ), ОФЭКT, а также - осмотр при хирургической ревизии). Золотым стандартом визуализации вполне оправданно можно считать метод компьютерной томографии.
Важно: визуализация опухоли на предлучевом этапе должна быть произведена в условиях, абсолютно схожих с процессом будущего лечения
(т.е. положение тела – неизменяемое, наполнение мочевого пузыря – одинаковое, дыхание – одинаковой интенсивности)
4) получение топометрических данных об анатомии органов в объеме,
подлежащем облучению (клиническая топометрия)
58
По своей сути, клиническая топометрия – это система определения
параметров мишени:
-линейных размеров
-площади
-объёма
-формы
-местоположения патологического очага
-синтопия с критическими структурами и здоровой тканью.
Её основная задача – объединить все данные об опухоли, полученные разными диагностическими методами, и представить их в виде топографо-
анатомической карты в масштабе 1:1 для формирования полей облучения и разработки программы облучения с помощью различных компьютерных программ. Ещё в 60-е годы прошлого века были созданы первые симуляторы
– рентгеновские установки, позволяющие провести предлучевую подготовку и симулировать будущий процесс облучения. Термин «симуляция» означает следующее: «заглянуть» в тело пациента так, как это сделает входящий пучок ионизирующего излучения. При этом возможно 2 пути:
1.«Взгляд» на симуляторе с использованием низкодозных Rо-лучей или КТ и последующая установка коллиматоров в соответствии с контурами опухоли (применяются рентгеновские или КТ-симуляторы).
Это более простой, но более грубый вариант предлучевой подготовки
(рис.1)
2.Виртуальная симуляция (проводится с применением современных компьютерных томографов и соответствующего программного обеспечения, позволяющего в короткие сроки создать множество изображений опухоли в разных проекциях и определить облучаемые
объёмы с учётом индивидуальных особенностей (размеров, формы,
распространённости и т.д.) (рис.6).
59
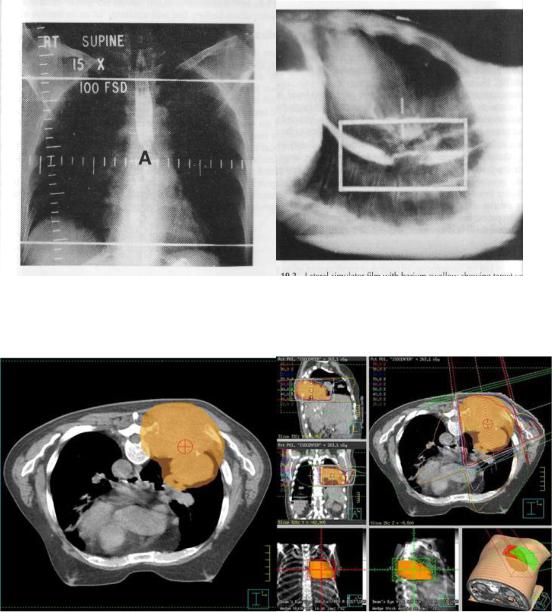
Рис.6. Пример рентгеновской симуляции при раке пищевода.
Рис.7. Пример виртуальной симуляции при раке лёгкого.
При составлении клинического задания на дозиметрическое
планирование на основании клинического и топометрического обследований больного должны быть установлены: радикальный объем мишени, поглощенная доза, уровни лучевых нагрузок на окружающие здоровые органы и ткани, максимальные ограничения дозы в критических органах, предполагаемый временной режим облучения. С учетом возможностей радиационно-технического (аппаратурного) оснащения
60