Материал: Лекции онко
разовой дозы более 10 млн МЕ не дает преимуществ. Средняя частота полных и частичных ремиссий при использовании интерферона альфа составляет по данным Savage P.D. (1995) – 15%.
Наиболее частые режимы введения: по 3-6 млн МЕ ежедневно в тече- ние 2 недель или 3 раза в неделю 3 – 4 недели; начиная со 2 недели, возможно увеличение разовой дозы до 9-18 млн МЕ/сут.
Поскольку почечно-клеточный рак считается химио – и гормонорезистентной опухолью, на сегодняшний день стандартом лечения метастати- ческого рака почки является иммунотерапия с использованием интерферона и интерлейкина – 2 в виде монотерапии или в различных сочетаниях, подобная терапия дает обьективный эффект у 10 до 20% больных.
Появление новых методов иммунотерапии (противоопухолевая вакцинотерапия, генная терапия и миниаллогенная трансплантация) позволяют надеяться на увеличение эффективности комбинированного лечения диссеминированного рака почки.
Лучевая терапия рака почки
По общему мнению злокачественные опухоли почки, в общем, резистентентны к лучевому воздействию, ее применение обосновано только при паллиативной терапии костных метастазов: для уменьшения болей, предотвращениядальнейшейпрогрессиииулучшениякачестважизни.Напрактикеиспользуются несколько наиболее распространенных режимов фракционирования: 3 Гр.х 10 в течение 2 недель или 4 Гр. х 5 в течение 1 недели. Анальгезирующий эффект лучевой терапии при СОД 30 – 40 Гр достигается у 80% больных.
Лучевая терапия применяется не только для уменьшения болевого синдрома, но и с целью стабилизации и предотвращения патологических переломов за счет реминерализации костной ткани. Для достижения рекальцификации показано использование более длительных курсов с более мелким фракционированием и высокими суммарными дозами: СОД 60-66 Гр. (по 2 Гр. х 5 дней в неделю, 6 – 7 недель), СОД 50 Гр.(по 2,5 Гр х 20), СОД 39 Гр.(по 3 Гр х 13). Выбор схемы лечения зависит от ожидаемой продолжительности жизни пациента и локализации поражения. Аналогичные режимы могут быть применены в песлеоперационном периоде, хотя доза облу- чения уменьшается в зависимости от размеров резидуальной опухоли.
Применение предоперационной лучевой терапии теоретически можно обосновать необходимостью профилактики местных рецидивов и интраоперационной диссеминации опухоли. С этой целью проводится интенсивный курс лучевой терапии по 5 Гр ежедневно в течении 5 дней, через 24-48 часов после окончания облучения пациента оперируют. Эффективность подобной терапии в настоящее время изучается.
494
Применение бисфосфонатов
С целью улучшения качества жизни больных РП с метастазами в кости в настоящее время активно используются препараты группы бисфосфонатов
(зомета,бонефос,бондронат, памиред милдронат, аредия), которые являются синтетическими аналогами пирофосфатов, регулирующих процесс минирализации в организме. Применение этих препаратов в два раза уменьшает процент осложнений со стороны костной системы, таких как патологические переломы и сдавление спинного мозга, позволяет избежать необходимости проведения лучевой терапии или хирургического вмешательства, увеличивает безрецидивный период на 6 мес.
Результаты лечения рака почки
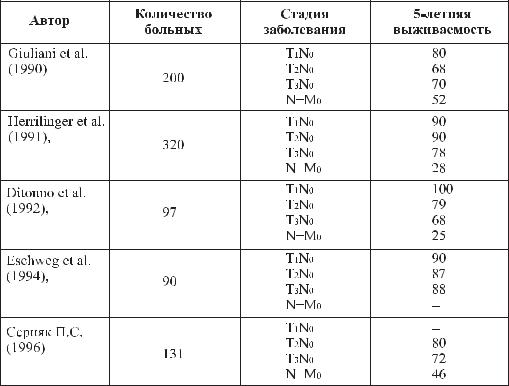
Результаты лечения РП представленные в литературе в значительной степени рознятся но, тем не менее, общие тенденции большинства исследователей очевидны. Giuliani et al. (1990), Herrilinger et al. (1991), Ditonno et al. (1992), Eschweg et al. (1994), Серняк П. С. (1996) приводят данные 5 летней выживаемости в зависимости от стадии заболевания.
5 – летняя выжи ваемость больных почечно-клеточным раком
по данным различных авторов
495
На 5 летнюю выживаемость в большей степени влияет метастатическое поражение лимфатических узлов, чем размеры опухоли, при неметастати- ческих стадиях рака возможно добиться 5-летней выживаемости у 68-100% больных. Если в регионарных лимфоузлах есть метастазы этот показатель снижается до 25-52%, а по данным отдельных авторов, ни один больной с метастазами в регионарные лимфоузлы не переживает пятилетний рубеж.
Диспансеризация больных
Диспансеризация должна быть направлена на раннее выявление опухолей почки. Прежде всего, у людей старше 40 лет, необходимо 1 раз в год брать анализ мочи и выполнять УЗИ брюшной полости и забрюшинного пространства. Эти исследования могут оказаться весьма эффективными, поскольку современные УЗИ аппараты способны выявлять опухоли до 0,5-1см в диаметре. Таким доступным в современных условиях методом, возможно, выявлять рак почки на ранних стадиях заболевания. В случаях, когда у больного выявляется аденома почки,. ему нужно предлагать оперативное лечение.У больных, имеющихдоброкачественныеопухолипочекнеобходимопроходитьУЗИ исследование не реже 1 раза в 6 месяцев. Обследования желательно проходить на том же аппарате и у того же врача, чтобы достоверно оценить динамику.
После проведенного радикального лечения первый осмотр проводится спустя 1 месяц, затем 1 раз в 3 месяца в течении первого года и в последующем 1 раз в полгода в течении 5 лет. Каждый осмотр должен сопровождаться УЗИ контролем, не реже одного раза в полгода, ренгенисследованием органов грудной клетки, взятием общего анализ крови и мочи. По показаниям необходимо выполнять КТ, МРТ, изотопное исследование костей скелета, ренографию и т.д.
Профилактика рака почки
Как указывалось выше, курение является основным фактором, увеличи- вающим вероятность заболевания РП. Как известно табакокурение наиболее существенно влияет на заболеваемость раком легкого, мочевого пузыря
èпочки. Складывается впечатление, что компоненты табачного дыма, оказывают канцерогенное действие «на входе и выходе» из организма. Особое внимание следует уделить разъяснительной работе с детьми, подростками
èмолодыми людьми поскольку риск заболеть РП с течением времени снижается очень медленно.
Больше внимания необходимо уделять профосмотрам на нефтеперерабатывающих, бумагопроизводящих и других производствах, связанных с возможностью канцерогенного воздействия на персонал.
496
ГЛАВА XX
РАК МОЧЕВОГО ПУЗЫРЯ
Академик АМН Украины, профессор Бондарь Г.В., профессор Борота А. В., профессор Семикоз Н. Г.
Введение
Рак мочевого пузыря (РМП) до настоящего времени остается одной из актуальнейших проблем онкоурологии, ряд вопросов которой не решены до конца.
Заболеваемость раком мочевого пузыря продолжает неуклонно расти. При этом риск развития заболевания может варьировать в различных регионах в 10 раз. Мужчины болеют в 2,5 – 6 раз чаще женщин. Основную массу опухолей мочевого пузыря составляют эпителиальные опухоли. Они разделяются на доброкачественные (папилломы) и злокачественные (переходноклеточный, сосочковый, плоскоклеточный рак и аденокарцинома).
Для рака мочевого пузыря особенно характерно нарастание заболеваемости с возрастом: опухоли почти не выявляются у людей моложе 35 лет, однако после 65 лет вероятность их появления резко увеличивается.
Среди заболевших РМП летальный исход, обусловленный основным заболеванием отмечается всего у 20 – 25% пациентов. Этот относительно благоприятный показатель обьясняется тем, что в 70 – 80% случаев, РМП диагностируется на неинвазивных стадиях. У остальных больных опухоль характеризуется инфильтративным ростом уже при ее выявлении, что указывает на неблагоприятный прогноз в течении заболевания.
Эпидемиология
РМП занимает 6-е место структуре онкологических заболеваний (11,4 на 100 тыс. населения), 3-е место среди урологической и 2-е место среди онкоурологической патологии (50% и 72 % соответственно). Заболеваемость мужского населения превышает таковую у женщин в 4 раза. Количество больных раком мочевого пузыря возрастает каждые 5 лет больше чем на 20%, и по прогнозам будет расти в том же темпе. Жители развитых стран, особенно представители белой расы, страдают в наибольшей степени, так в США и Западной Европе заболеваемость РМП в 2 – 3 раза превышает среднемировые показатели и в 10 раз выше, чем в Восточной Европе и Азии.
В Украине в настоящее время на учете находится 24 тыс. больных раком мочевого пузыря и прогнозируется увеличение заболеваемости до 2010 г. в 1,4 раза, а смертности – в 2,8 раза.
Этиология
Выделяют экзогенные и эндогенные (генетические) факторы риска развития РМП. К экзогенным факторам риска относятся следующие:
–воздействие производственных вредностей;
–курение;
497
–Хроническое воспаление;
–Ятрогенное воздействие.
Производственные вредности. Рак мочевого пузыря является одним из первых онкологических заболеваний, для которых была достоверно продемонстрирована взаимосвязь с работой на вредном производстве. Установлена повышенная заболеваемость среди рабочих, связанных с производством красителей, у работников резиновой и текстильной промышленности. Счи- тается, что наиболее значимым звеном в патогенезе «профессионального» рака мочевого пузыря является контакт с канцерогенами из группы ароматических аминов и их производных (бензидин, бета-нафтиламин, 4-аминобифенил, нитрозоамины). В настоящее время, благодаря повсеместному внедрению правил техники безопасности, направленных на уменьшение контакта с ариламинами индустриального происхождения, уровень заболеваемости РМП, сопряженной с вредным производством, заметно снижается.
Курение является одной из основных причин возникновения РМП, влияние которой значительно возросло в последние годы. Риск развития рака мочевого пузыря у курильщиков примерно в 20 –30 раз выше по сравнению с некурящими.
Влияние ароматических аминов, которые входят в состав табачного дыма, на негативные последствия курения, в недавнем прошлом расценивалось как умеренное по сравнению с полициклическими углеводородами (ПАУ). Однако, начиная с 80-х годов XX столетия, в развитых странах наблюдается вытеснение «крепких»сортов сигарет так называемыми «легкими» разновидностями табачных изделий («light », «superlight » и т.д.). Последние действительно характеризуются низкой концентрацией смол и уменьшенным содержанием ПАУ в табачном дыме, при этом содержание предшественников ароматических аминов в подобных модифицированных сигаретах остается прежним. Кроме того, курильщики компенсируют «недостаточную» крепость «легких» сигарет более глубокой и продолжительной ингаляцией табачного дыма. Указанные изменения в стиле курения привели к заметному увеличению роли ароматических аминов в канцерогенезе.
Хроническое воспаление. Воздействие хронического воспаления, отча- сти связанного с вторичными бактериальными инфекциями мочевого пузыря, также является фактором риска возникновения РМП. Многие из условно патогенных бактерий, активизирующиеся вследствие хронического цистита, способны образовывать нитрозосоединения, которые являются мощными канцерогенами. Наиболее классическим примером вялотекущего воспалительного процесса является мочеполовой шистосоматоз, чрезвычайно распространенный в странах Ближнего Востока, особенно в Египте.
498