Материал: Д6711 Федорова РА Санитария и гигиена
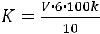
ли фенолфталеина и титруют 0,1 н. раствором гидроксида натрия (NaOH) до появления розовой окраски, не исчезающей в течение 1 мин.
Кислотность дрожжей (мг уксусной кислоты) определяют по формуле
, |
(6) |
где V – объем раствора гидроксида натрия, пошедший на титрование, мл; 6 – объем уксусной кислоты, соответствующий 1 мл 1 н. раствора гидроксида натрия; k – поправочный коэффициент к титру раствора щелочи (k = 1).
Кислотность дрожжей должна соответствовать следующим значениям:
–не более 120,0 мг уксусной кислоты в день выработки;
–не более 300,0 мг уксусной кислоты на 12 сут после выработки. 2.3. Определение подъемной силы дрожжей.
Подъемная сила дрожжей характеризует их бродильную актив-
ность. Это один из важных показателей качества. Ее можно определить двумя способами – ускоренным и стандартным.
У с к о р е н н ы й м е т о д. Навеску дрожжей массой 0,31 г переносят в фарфоровую ступку, приливают 4,8 мл нагретого до 35 °С 2,5 %-го раствора хлорида натрия и тщательно перемешивают пестиком. К полученной смеси добавляют 7 г муки, замешивают тесто и придают ему форму шарика. Шарик помещают сначала в стакан с водой, нагретой до 35 оС, а затем – в термостат той же температуры. Подъемная сила дрожжей характеризуется временем, прошедшим с момента опускания шарика в воду до момента его всплытия. Время всплытия шарика умножают на коэффициент 3,5.
С т а н д а р т н ы й м е т о д. В термостат температурой 35 °С предварительно помещают на 2 ч 280 г муки пшеничной и 160 мл 2,5 %-го раствора соли, приготовленного на питьевой воде.
Навеску дрожжей массой 5 г переносят в фарфоровую ступку, доливают 20 мл раствора соли и перемешивают до исчезновения комочков.
Разведенные дрожжи переливают в сосуд для замеса теста, туда же добавляют 280 г муки и оставшийся раствор соли – 140 мл. Замешивают тесто вручную. Тесту придают форму батона и переносят
21
в металлическую форму, смазанную растительным маслом и подогретую в термостате при температуре 35 оС.
Металлическая форма представляет собой в продольном и поперечном разрезах трапеции определенных стандартных размеров, регламентируемых ГОСТом. На длинные борта формы кладут поперечную металлическую перекладину, входящую на 1,5 см в форму.
Форму с тестом ставят в термостат с температурой 35 °С и следят за тем, когда тесто коснется перекладины. Время, прошедшее с момента внесения теста в форму до момента прикосновения его к нижнему краю перекладины, называется подъемной силой.
Подъемная сила у дрожжей хлебопекарных прессованных должна быть не более 70 мин.
2.4. Определение мальтазной активности дрожжей весовым ме-
тодом.
Бродильная активность дрожжей характеризуется их мальтазной активностью.
Дрожжи используются для разрыхления теста за счет сбраживания сахаров – глюкозы, фруктозы, мальтозы, – что выражается временем в минутах, затраченным для выделения 10 мл диоксида углерода при сбраживании 10 %-го раствора соответствующего сахара.
Приготовить 5 %-й раствор мальтозы на дистиллированной воде и раствор дрожжей прессованных. Для этого 0,5 г дрожжей смешать с 10 мл водопроводной воды температурой 35 °С.
Сухую колбу вместимостью 100 мл взвесить на технических весах. Записать вес колбы. В колбу добавить раствор дрожжей и 10 мл 5 %-го раствора мальтозы. Перемешать, взвесить колбу с раствором на технических весах. Вес записать. Далее колбу с раствором взвешивать каждые 10 мин, пока вес колбы не уменьшится на 10 г.
Мальтазная активность дрожжей должна быть 60–90 мин. 3. Написать отчет о проделанной работе.
РАБОТА 12 ОПРЕДЕЛЕНИЕ СОСТОЯНИЯ
КУЛЬТУРЫ ДРОЖЖЕЙ МИКРОСКОПИРОВАНИЕМ
Микроскопирование препаратов дрожжей позволяет следить за их состоянием и размножением, а также за развитием бактериальной флоры.
22
Молодые и зрелые дрожжи крупнее состарившихся. Оболочка у них едва заметна, вакуоли отсутствуют или очень малы. Они имеют большое количество почкующихся клеток. О старении культуры дрожжей можно судить по следующим признакам: их оболочка имеет вид утолщенного ободка, строение протоплазмы зернистое, она отстает от оболочки, имеет большие вакуоли, присутствуют капельки жира.
Бактерии Дельбрюка представляют собой расположенные попарно палочки длиной 3–7 мкм и более, их колонии округлой формы, беловатого цвета, мелкие, выпуклые. При нарушении нормальных условий культивирования бактерии образуют длинные, местами утолщенные нити.
Цель работы: приобрести навыки работы с микроскопом. Оборудование: микроскоп, предметные стекла.
Порядок выполнения работы:
1. Ознакомление с устройством микроскопа.
Микроскоп – это оптический прибор для получения увеличенных изображений очень малых тел. Современными моделями биологического микроскопа являются микроскопы серии «Биолам».
Микроскоп состоит из оптической системы и механической части. Оптическая система предназначена для увеличения изображения предмета. Она включает в себя увеличительную (объектив и окуляр) и осветительную системы (зеркало и конденсор с ирисовой диафрагмой и откидной линзой).
Объектив представляет собой систему линз, заключенных в трубку. В микроскопах серии «Биолам» используются объективы с увеличением Х3; Х5; Х9; Х10; Х20; Х40; Х60; Х85; Х90. Объективы малого увеличения (Х3; Х5; Х8; Х9) применяют для предварительного осмотра препарата; объективы среднего увеличения (Х20; Х40; Х60) – для изучения крупных клеток микроорганизмов; объективы большого увеличения (Х85; Х90) – и м м е р с и о н н ы е – для изучения внутренних структур клеток. Окуляр служит для увеличения изображения, полученного от объектива. Окуляры обычно имеют увеличение Х7, Х10 и X15. Увеличение объектива и окуляра указано на их оправе. Общее увеличение микроскопа равно произведению увеличений окуляра и объектива.
Осветительное устройство состоит из зеркала и конденсора. Зеркало имеет плоскую и вогнутую отражающие поверхности. Обычно при работе зеркало повернуто к свету плоской стороной. Конден-
23
сор состоит из двух линз. В плоскости исследуемого препарата параллельные лучи света, отраженные от зеркала, линзы собирают в один пучок. Конденсор укреплен на кронштейне и может передвигаться вверх и вниз с помощью рукоятки. На нижней части конденсора имеется ирисовая диафрагма, с помощью которой регулируют интенсивность освещения препарата.
Пучок лучей от источника света фокусируется на зеркало, отражается через диафрагму конденсора, проходит через нее, затем через исследуемый препарат попадает в объектив. Объектив дает увеличенное изображение препарата в плоскости окуляра.
Механическая часть микроскопа состоит из основания и тубусодержателя, на котором укреплены предметный столик, кронштейн конденсора и зеркало. В верхней части находятся головка для насадки с окуляром и револьвер с объективами. Предметный столик служит для закрепления на нем исследуемого препарата.
Фокусировка осуществляется при перемещении тубуса с помощью механизма, приводимого в движение двумя винтами – макрометрическим (грубая фокусировка) и микрометрическим (тонкая фокусировка).
2. Ознакомление с правилами работы с микроскопом.
Сначала ставят объектив с малым увеличением (Х8) и при этом увеличении устанавливают наилучшее освещение. Наилучшее освещение достигается при регулировке положения зеркала, конденсора и диафрагмы. При просмотре неокрашенных препаратов применяют суженную диафрагму и опущенный конденсор, при наблюдении окрашенных препаратов – открытую диафрагму и поднятый конденсор.
Затем препарат помещают на предметный столик микроскопа под объектив и укрепляют зажимами. Опускают объектив (Х8) при помощи макрометрического винта почти до соприкосновения с предметным стеклом на расстояние около 0,5 см от предметного столика. Медленно вращают макровинт против часовой стрелки до появления четкого изображения препарата, после чего наводят на резкость микрометрическим винтом, который вращают в пределах одного оборота макровинта. Повернув револьвер, устанавливают объектив со средним увеличением (Х20; Х40 или Х60).
Цель работы: оценить качество прессованных дрожжей микроскопированием.
24
Приборы и посуда: микроскоп, предметные стекла, стеклянная палочка, пробирки, мерный цилиндр, стакан, пипетка.
Материалы и реактивы: жидкие дрожжи, йод, йодид калия, вода.
Порядок выполнения работы:
1.Приготовление раствора Люголя. Приготовленные неокрашенные препараты окрашивают раствором Люголя. Для этого берут навески 1 г йода и 2 г йодида калия и растворяют в 300 мл воды.
2.Приготовление препаратов дрожжей. На 1 объем жидких дрожжей берут 3–5 объемов воды. Смесь энергично взбалтывают
иоставляют на 1 мин.
3.Микроскопирование препаратов дрожжей. Из верхнего слоя дрожжевой жидкости стеклянной палочкой переносят небольшую каплю на предметное стекло. Накрывают покровным стеклышком
ислегка прижимают его сухим концом стеклянной палочки для удаления пузырьков воздуха. Препараты рассматривают под микроскопом при увеличении в 500 –1000 раз (объективы Х40 и Х90).
4.Написать отчет о проделанной работе.
РАБОТА 13 ОПРЕДЕЛЕНИЕ КОЛИЧЕСТВА ДРОЖЖЕЙ
И МОЛОЧНОКИСЛЫХ БАКТЕРИЙ В ПОЛУФАБРИКАТАХ
Для учета количества дрожжей и молочнокислых бактерий в полуфабрикатах принят метод прямого подсчета Бургвица, или метод постоянно окрашенных препаратов.
Цель работы: приобрести навыки по определению количества молочнокислых бактерий и дрожжей в закваске (опаре) и тесте.
Приборы и посуда: технические весы с разновесами, фарфоровая чашка, стеклянная палочка, мерный стакан, колба вместимостью 1 л с пробкой, пипетки на 1 или 2 мл, предметное стекло, микроскоп.
Материалы и реактивы: этиловый спирт 96 %-й, формалин, метиленовый синий, парафин, полуфабрикат (закваска, тесто, жидкие дрожжи), вода.
Порядок выполнения работы:
1. Подготовка предметных стекол.
Предметное стекло обезжирить и наложить его на трафарет – небольшой кусок миллиметровой бумаги на плотной основе (картон
25