Материал: Белозеров В.И., Яркин А.Н., Кузина Ю.А. Сборник задач по курсу Техническая термодинамика
4.22. В цилиндре двигателя автомобиля «Волга» к концу хода сжатия объем рабочей смеси составляет 109 см3, температура 327ºC, давление 13 бар. Определить теоретическую температуру и давление после сгорания смеси, считая, что горение происходит мгновенно, а физические свойства смеси такие же, как у воздуха. Количество сгорающего топлива 19 мг, его теплотворная способность 43800 кДж/кг.
4.23. Вычислить
средние массовую и объемную теплоемкости
окиси углерода при постоянном объеме
для интервала температур 0 – 1200ºC,
если известно, что
![]() для окиси углерода равно 32,192 кДж/(кмоль·К).
для окиси углерода равно 32,192 кДж/(кмоль·К).
4.24. Вычислить
среднюю теплоемкость
![]() для воздуха при постоянном давлении в
пределах 200 – 800ºC,
считая зависимость теплоемкости от
температуры нелинейной. Решить эту же
задачу, считая зависимость теплоемкости
от температуры линейной.
для воздуха при постоянном давлении в
пределах 200 – 800ºC,
считая зависимость теплоемкости от
температуры нелинейной. Решить эту же
задачу, считая зависимость теплоемкости
от температуры линейной.
4.25. Вычислить
среднюю массовую теплоемкость при
постоянном объеме для азота
в пределах 200 – 800ºC,
считая зависимость теплоемкости от
температуры нелинейной. Решить эту же
задачу, если известно, что средняя
мольная теплоемкость азота при постоянном
давлении может быть определена по
формуле
![]() =28,7340+0,0023488Т.
=28,7340+0,0023488Т.
4.26. В закрытом сосуде объемом 300 л находится воздух при давлении P=8 бар и температуре t=20ºC. Какое количество тепла необходимо подвести для того, чтобы температура воздуха поднялась до 120ºC?
4.27. В компрессоре газовой турбины сжимается воздух. Начальная температура воздуха t1=30ºC, температура после сжатия t2=150ºC. Определить изменение энтальпии и внутренней энергии воздуха в процессе сжатия.
4.28. В регенеративном подогревателе газовой турбины воздух нагревается при постоянном давлении от t1=130ºC до t2=500ºC. Определить количество теплоты, сообщенное воздуху в единицу времени, если расход его составляет 250 кг/ч. Ответ дать в кДж/с и в киловаттах.
4.29. Баллон с водородом выносится из помещения с температурой 5ºC в машинный зал, где температура 25ºC. Найти количество теплоты, полученной газом после выравнивания температуры, если начальное давление в баллоне составляло 12 МПа. Объем баллона 40 дм3. Определить изменение энтальпии водорода.
4.30. Воздух выходит из компрессора при P=0,7 МПа и t= 160ºC и поступает в холодильник. На выходе из холодильника температура воздуха равна 25ºC. Определить количество теплоты, отданное охлаждающей воде в течение часа, если производительность компрессора 6 м3/мин.
4.31. При
определении средней изобарной теплоемкости
воздуха используется прямоточный
калориметр с электрическим нагревателем.
Определить среднюю массовую теплоемкость
воздуха
![]() ,
протекающего через калориметр, если
при включении электрического нагревателя
сила тока составляет 25 А, напряжение
питания 36 В. Разность температур воздуха
до и после нагревателя 18 К. Расход воздуха
через калориметр 0,00055 м3/с,
давление 750 мм рт. ст., температура
воздуха, поступающего в калориметр, 297
К.
,
протекающего через калориметр, если
при включении электрического нагревателя
сила тока составляет 25 А, напряжение
питания 36 В. Разность температур воздуха
до и после нагревателя 18 К. Расход воздуха
через калориметр 0,00055 м3/с,
давление 750 мм рт. ст., температура
воздуха, поступающего в калориметр, 297
К.
4.32. В сосуде объемом 300 л находится кислород (О2) при давлении 2 бар и температуре 20ºC. Какое количество тепла необходимо подвести, чтобы температура кислорода повысилась до 300ºC? Какое давление установится при этом в сосуде?
5. Процессы изменения состояния идеальных газов
Исследование термодинамического процесса включает в себя получение аналитической связи между термодинамическими параметрами газа, определение их значений и приращений в различных термодинамических состояниях, реализуемых в процессе.
Фундаментальные соотношения для идеального газа (в удельных массовых величинах):
Pv=RT – уравнение состояния (Клапейрона);
du=cvdT, dh=cpdT – закон Джоуля;
с
(5.1)
две формы уравнения
первого закона термодинамики
(5.2)![]() –
–
Изобарный процесс (P=P0=const)
а). В этом случае для любых двух состояний газа
P0 v1=RT1, P0 v2=RT2.
Отсюда следует характерная для этого процесса связь между термодинамическими параметрами (уравнение процесса):
![]() или
или
![]() .
.
б). Поскольку dP0, то из (5.1) следует, что все тепло идет на изменение энтальпии:
q = h = cpdT.
Располагаемая работа равна нулю.
в). С учетом этого из (5.2) следует
u = h – P0V = h – RT.
Работа расширения А = P0V.
Изохорный процесс (V=V0=const)
Поскольку M=const, то v0=V0/M=const.
a). Для любых двух состояний
P1v0=RT1 , P2v0=RT2.
Отсюда следует уравнение изохорного процесса
![]() или
или
![]() .
.
б). Из (5.2) получаем q=u=cvT – все тепло идет на изменение внутренней энергии; т.к. dv0, работа расширения равна нулю.
в). Из (5.1) следует
h = u +v0P = u+RT = q+v0P.
Располагаемая работа v0P = h –u = RT.
Изотермический процесс (T=T0=const)
4.33. В регенеративном подогревателе газовой турбины воздух нагревается от 170 до 580ºС. Определить количество тепла, сообщенное воздуху в единицу времени, если его расход составляет 350 кг/ч.
4.34. В калориметре с идеальной тепловой изоляцией находится вода в количестве Mв=0,8 кг при температуре t1=15ºC. Калориметр изготовлен из серебра, теплоемкость которого сv=0,2345 кДж/(кг·К). Масса калориметра MК=0,25 кг. В калориметр опускают 200 г алюминия при температуре tA=100ºC. В результате этого температура воды повышается до t2=19,25ºC. Определить теплоемкость алюминия.
а). Из уравнения состояния для двух произвольных «точек» этого процесса
P1v1=RT0 , P2v2=RT0
следует уравнение процесса
![]() или
Pv=RT0=const.
или
Pv=RT0=const.
б). В соответствии с законом Джоуля, т.к. dT0,
du = cvdT 0, dh = cpdT 0 (u=h=0).
в). Из уравнения (5.2) следует, что dq=Pdv – все тепло идет на совершение работы, и наоборот.
Из (5.1) следует, что dq = –vdP – располагаемая работа равна работе расширения с обратным знаком.
г). Произведенная работа (работа расширения)
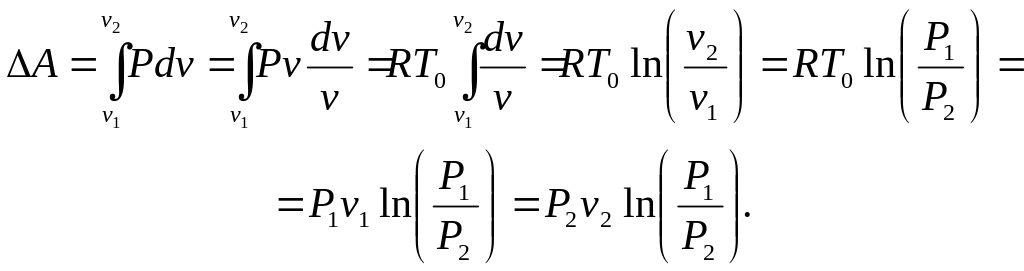
Здесь использованы следующие из уравнения процесса равенства:
P1v1= P2 v2 =Pv= RT0=const и .
Адиабатный процесс (dq=0)
В этом процессе отсутствует теплообмен с окружающей средой:
Q=Mq=0.
a). Поскольку dq=0, уравнения (5.1), (5.2) имеют вид
![]() ,
,
![]() (
(![]() =dh;
=dh;
![]() =du).
=du).
Разделив первое уравнение на второе (отдельно левые и правые части), получаем
![]()
(![]() – показатель адиабаты).
Из этого уравнения следует
– показатель адиабаты).
Из этого уравнения следует
![]() ,
т.е.
,
т.е.
![]() ,
,
![]() и
и
![]() или
или
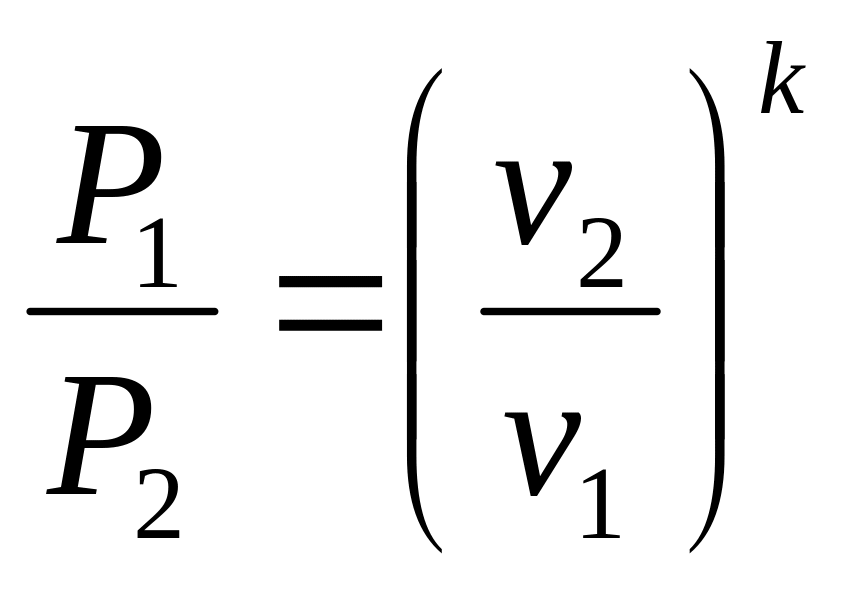 . (5.3)
. (5.3)
Это и есть уравнение адиабатного процесса, а т.к. Pv=RT, можно представить его в виде
![]() или
или
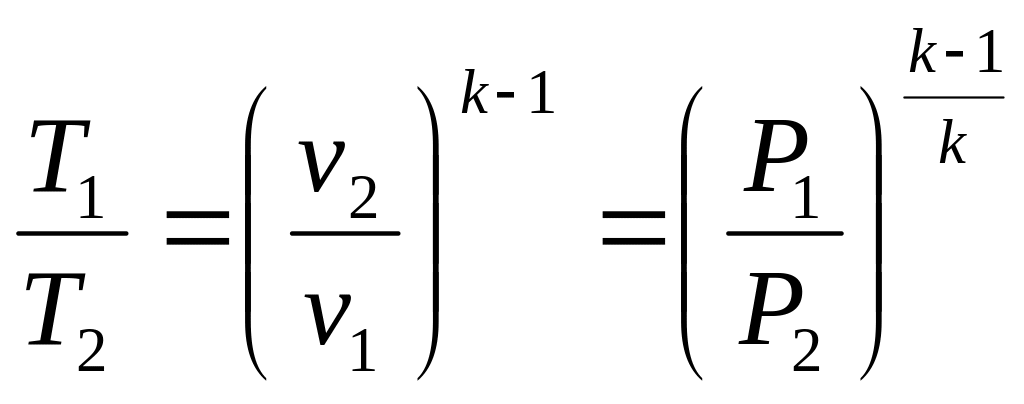 . (5.4)
. (5.4)
б). Располагаемая работа в адиабатном процессе в k раз больше работы расширения:
vdP= –k(Pdv).
Поскольку vdP=dh, а du= –pdv, приращение энтальпии в k раз больше приращения внутренней энергии:
dh=kdu.
в). Для работы (работа расширения), совершаемой газом в адиабатном процессе при переходе из одного состояние в другое,
dA=Pdv.
Поскольку h=u+Pv, то
dh–du=d(Pv)=Pdv+vdP=dA–kdA=(1–k)dA,
следовательно, получаем
dA= –d(Pv)/(k–1).
Отсюда после интегрирования
![]() .
.
Используя различные уравнения адиабатного процесса (5.3) или (5.4), формулам для A можно придать различный вид, например,
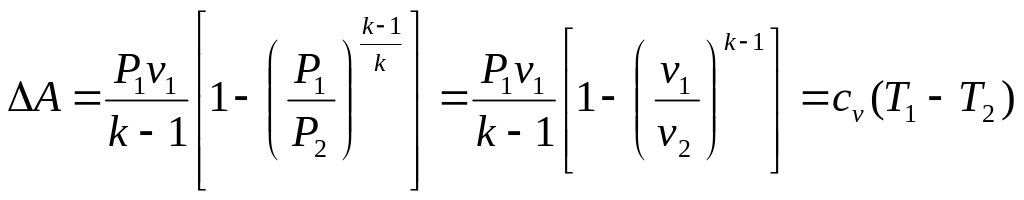 .
.
Политропный процесс (dq=cпdT, cп=const)
Этот процесс характеризуется линейной зависимостью Q от T.
а). Для этого процесса уравнения (5.1), (5.2) имеют вид
![]() (du=cvdT,
dh=cpdT),
(du=cvdT,
dh=cpdT), ![]() .
.
Перенесем
![]() в левые части этих уравнений:
в левые части этих уравнений:
![]() ,
,
![]() .
.
Разделив первое уравнение на второе, получим
![]() ,
vdP=
–n(Pdv)=
– ndA
,
vdP=
–n(Pdv)=
– ndA
(n – показатель политропы). Действуя как в предыдущем пункте, получим уравнение политропного процесса
![]()