Материал: Белозеров В.И., Яркин А.Н., Кузина Ю.А. Сборник задач по курсу Техническая термодинамика
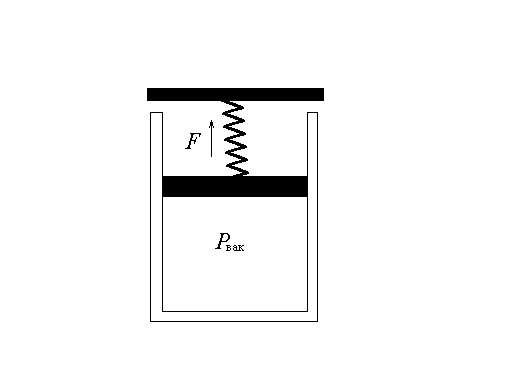
Рис. 1.2
1.18. По трубопроводу диаметром d=50 мм, присоединенному к сосуду, подается газ, удельный объем которого υ =0,5 м3/кг. За какое время газ наполнит сосуд, если его объем V=5 м3, средняя по сечению скорость газа в трубопроводе W=2,55 м/c, а плотность газа, заполнившего сосуд, ρ = 0,00127 г/см3.
1.19. Температура пара, выходящего из перегревателя парового котла, равна 950ºF. Перевести эту температуру в градусы Цельсия, Кельвина, Реомюра, Ренкина.
1.20. Водяной пар перегрет на 45ºС. Чему соответствует этот перегрев по шкале Фаренгейта и шкале Ренкина?
1.21. Температура пара после прохождения его через пароперегреватель котельного агрегата увеличилась на 450ºF. Чему равно увеличение температуры пара, выраженное в градусах Цельсия?
1.22. При установлении своей шкалы Фаренгейт принял за 100º нормальную температуру человеческого тела. Какова, по мнению Фаренгейта, эта температура в градусах Цельсия?
1.23. В США употребляется абсолютная шкала Ренкина, в которой за ноль принята температура абсолютного нуля, а цена деления такая же, как и цена деления шкалы Фаренгейта. Какова температура по абсолютной шкале Ренкина, если в градусах Цельсия она равна 520ºС?
1.24. Температура пара на входе в цилиндр высокого давления (ЦВД) составляет 350ºС, а его давление 64 бар. Перевести давление в МПа, а температуру в ºF.
2. Идеальные газы
Идеальный газ – это система материальных точек, взаимодействующих между собой и со стенками сосуда только путем упругих соударений. Другие механизмы взаимодействия отсутствуют. Существующие в действительности газы при не слишком низких температурах и достаточно малых давлениях – разреженные газы – по своим свойствам близки к идеальному газу.
Реальный газ тем больше отличается от идеального, чем выше его плотность. С точки зрения молекулярно-кинетической теории отклонение реального газа от идеального («неидеальность») обусловлено, в первую очередь, наличием у молекул собственного объема и сложным механизмом межмолекулярного взаимодействия.
Уравнение состояния идеального газа (уравнение Менделеева-Клапейрона), молярная масса которого μ (кг/кмоль), масса M (кг), занимающего объем V (м3) при давлении P (Па) и абсолютной температуре T (K), записывается следующим образом:
![]() ,
,
где R0 = 8314,41 Дж/(кмоль·К) ≈ 8314 Дж/(кмоль·К) – универсальная газовая постоянная. Величину R0/μ называют газовой постоянной.
Молярная масса – это масса в килограммах одного киломоля газа. Она численно равна атомной массе вещества для одноатомных газов либо сумме атомных масс составляющих элементов, если вещество газа – многоатомное химическое соединение. Например, для серной кислоты, пользуясь таблицей химических элементов Менделеева и округляя атомные массы до целого числа, находим
μ(H2SO4) = 2μ(H) + μ(S) + 4μ(O) = 2+42+64 = 98 кг/кмоль.
Поскольку удельный объем v=V/M – это объем занимаемый 1 кг газа, то (μ v) – это объем, занимаемый μ кг газа, т.е. одним киломолем (молярный объем). Из уравнения Клапейрона следует, что при одних и тех же P и Т киломоль любого идеального газа занимает один и тот же объем:
![]() .
.
Так, при нормальных физических условиях (P = 101325 Па, T = 273,15 K) μv= 22,4136 м3/кмоль. Следовательно, в объеме 22,4136 м3 при этих значениях P и Т будет находиться, например, либо 1 кг атомарного водорода, либо 32 кг двухатомного кислорода (μ(O2)=32 кг/кмоль).
Очевидно, что отношение n=M/μ определяет количество вещества в киломолях. Для идеального газа получаем
![]() .
.
Это равенство выражает закон Авогадро: в одинаковых объемах идеальных газов при одинаковых T и P содержится одно и то же число молекул. По определению, в одном киломоле любого вещества содержится одно и то же число молекул (атомов – для одноатомных). Его определяет фундаментальная физическая постоянная – число Авогадро (NA):
NA = 6,022045·1026 1/кмоль.
Наконец, отношение постоянных R0 и NA определяет третью физическую постоянную – число Больцмана (k):
k = R0 /NA = 1,380662·10-23 Дж/К 1,38·10-23Дж/К.
С учетом этого уравнение Клапейрона можно записать в виде
![]() .
.
Величину
![]() можно условно рассматривать как средний
объем, приходящийся на одну молекулу,
а kT
– как среднюю энергию теплового движения
одной молекулы.
можно условно рассматривать как средний
объем, приходящийся на одну молекулу,
а kT
– как среднюю энергию теплового движения
одной молекулы.
Задачи
2.1. Определить плотность и удельный объем двуокиси углерода (CO2) при нормальных физических условиях.
2.2. Плотность воздуха при нормальных физических условиях равна ρ=1,293 кг/м3. Чему равна плотность воздуха при давлении P=15 бар и температуре t=20ºC?
2.3. Определить массу углекислого газа в сосуде объемом V=4м3 при t=80ºC. Давление газа по манометру равно 0,4 бар. Барометрическое давление B= 780 мм рт. ст.
2.4. Начальное состояние азота задано параметрами: t=200ºC, v=1,9 м3/кг. Азот нагревается при постоянном давлении, причем объем азота увеличивается до 5,7 м3/кг. Определить конечную температуру.
2.5. В цилиндре с подвижным поршнем находится кислород при t=80ºC и разрежении (вакууме), равном 427 гПа. При постоянной температуре кислород сжимается до избыточного давления Pизб=1,2 МПа. Барометрическое давление B=993 гПа. Во сколько раз уменьшится объем кислорода?
2.6. Абсолютное давление азота в сосуде при комнатной температуре (t=20ºC) P=2,2 МПа. В сосуде азот нагревают, причем известно, что предельное избыточное давление, при котором возможна безопасная работа, P= 6 МПа. Определить температуру, до которой возможно нагревание азота. Барометрическое давление B=1000 гПа.
2.7. В воздухоподогреватель парового котла подается вентилятором 130000 м3/ч воздуха при температуре 28ºC. Определить объемный расход воздуха на выходе из воздухоподогревателя, если нагрев его производится до 400ºC при постоянном давлении.
2.8. Известно, что 1 кмоль газа содержит 6,022·1026 молекул. Для того чтобы представить себе, как велико это число, полезно проделать мысленно такой опыт. В сосуде объемом 1 см3 создан полный вакуум, т.е. удалены молекулы. В стенке сосуда сделано отверстие такого размера, что из окружающего воздуха в сосуд проникают молекулы с расходом 100000 молекул в секунду. Определить, сколько времени потребуется, чтобы плотность воздуха в рассматриваемом объеме стала равной плотности окружающего воздуха, если окружающий воздух находится при нормальных условиях, а скорость проникновения молекул остается неизменной.
2.9. Паротурбинная установка мощностью 100 МВт расходует 0,37 кг топлива на 1 кВт·ч. Какова должна быть суммарная массовая производительность вентиляторов, подающих воздух в топку котла, если для сжигания топлива требуется 16 м3 воздуха при нормальных условиях? Определить, что это за вещество.
2.10. В комнате площадью 42 м2 и высотой 2,9 м находится воздух при температуре 22ºC и барометрическом давлении 980,3 гПа. Какое количество воздуха проникнет с улицы в комнату, если барометрическое давление увеличится до 1020 гПа, а температура останется постоянной.
2.11. 0,37·10-3 кг газообразного вещества, формула которого СnHn , при температуре 400 К и абсолютном давлении 0,958 бар имеет объем 164·10-6 м3. Определить, что это за вещество.
2.12. Определить, действительно ли молекула кислорода является двухатомной, если известно, что в объеме, равном 4 дм3, находится 5 г кислорода при температуре 150ºC и P=0,1373 МПа. Чему было бы равно давление газа, если бы молекула состояла из трех атомов кислорода (озон O3)?
2.13. 0,003 м3 кислорода, отнесенного к нормальным физическим условиям, находится в сосуде емкостью 650 см3. Определить показания манометра, измеряющего давление в этом сосуде, если температура кислорода 200ºC. Атмосферное давление 1016 гПа.
2.14. Компрессор подает азот в резервуар емкостью 3 м3; избыточное давление в резервуаре увеличивается при этом от 0,01 до 0,6 МПа, а температура газа от 15 до 30ºС. Определить массу поданного компрессором азота. Барометрическое давление равно 987 гПа.
2.15. Определить подъемную силу шара-зонда, наполненного водородом и имеющего объем 1 м3. Абсолютное давление воздуха 0,1 МПа. Избыточное давление в шаре 0,333 бар. Температура водорода равна температуре воздуха T=288 K. Изменением температуры и давления при подъеме пренебречь.
Примечание. Подъемной силой называется разность удельных весов окружающей среды и газа, заполняющего шар.
2.16. Определить подъемную силу воздушного шара, наполненного водородом, если объем его на поверхности земли равен 1,2 м3 при давлении P=752 мм рт. ст. и температуре t=17ºC.
2.17. Определить необходимый объем аэростата, наполненного водородом, если подъемная сила, которую он должен иметь на высоте H=7000 м, равна 39240 Н. Параметры воздуха на этой высоте принять равными P=0,41 бар, t= –30ºC. Насколько изменится подъемная сила аэростата при заполнении его гелием? Чему равен объем аэростата на поверхности земли при давлении P=0,981 бар, t= 30ºC?
2.18. В герметически закрытом цилиндре поршень может двигаться без трения. По одну сторону поршня помещается 1 г водорода, а по другую – то же количество углекислого газа. Определить соотношение объемов справа и слева при равновесии.
2.19. Поршневой компрессор всасывает в минуту 3 м3 воздуха при температуре t = 17ºC и барометрическом давлении 753 мм рт. ст. и нагнетает его в резервуар, объем которого равен 8,5 м3. За сколько минут компрессор поднимает давление в резервуаре до 7 бар, если температура в нем будет оставаться постоянной? Начальное давление воздуха в резервуаре составляло 753 мм рт. ст. при температуре 17ºC.
2.20. На аналитических весах взвешивают образец из пластмассы, причем в момент равновесия на весах стоят гири общей массой 80,146 г. Определить истинную массу образца (т.е. с учетом поправки на выталкивающую силу воздуха), если известно, что плотность пластмассы равна 0,2 г/см3, а плотность вещества гирь 8,4 г/см3. Взвешивание производится в комнате при параметрах воздуха t=25ºC, P=0,102 МПа.
2.21. 5 м3 кислорода с начальным абсолютным давлением P1=0,4 МПа при температуре t=135ºC сжимаются изотермически до достижения давления P2=1,5 МПа. Определить количество газа, участвующего в процессе, и его конечный объем.
3. Смеси идеальных газов
Физической моделью идеального газа, приводящей к уравнению Клапейрона, является система материальных точек, взаимодействующих только путем упругих соударений; другие механизмы взаимодействия отсутствуют. В отсутствие химического взаимодействия смесь одноатомных или многоатомных идеальных газов также является идеальным газом, для которого справедливо уравнение Клапейрона.
Уравнение состояния отдельной компоненты газа в смеси
Ввиду отсутствия сил взаимодействия каждый газ «не чувствует» присутствия других компонент смеси и занимает весь объем сосуда (Vсм). В силу термодинамической равновесности температура (T) компонент и смеси одна и та же. Следовательно, давление (Pj), оказываемое на стенки сосуда только j-й компонентой k-компонентной смеси, определяется из уравнения
![]() (3.1)
(3.1)
Здесь nj – количество киломолей j-й компоненты в смеси. Эти давления называют парциальными.
Уравнение состояния смеси
В соответствии с законом Дальтона (закон парциальных давлений) полное давление рассматриваемой смеси газов равно сумме парциальных давлений:
![]() .
.
Суммируя отдельно левые и правые части уравнений (3.1) по j, получим
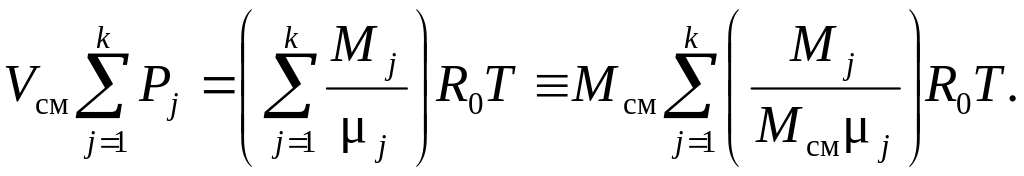
Здесь
![]() – масса смеси; Mj/Mсм=gj
– массовая доля j-й
компоненты в смеси. Это и есть уравнение
состояния смеси идеальных газов
(Менделеева-Клапейрона). С учетом закона
Дальтона оно имеет вид
– масса смеси; Mj/Mсм=gj
– массовая доля j-й
компоненты в смеси. Это и есть уравнение
состояния смеси идеальных газов
(Менделеева-Клапейрона). С учетом закона
Дальтона оно имеет вид
![]()
![]() – эффективная или
кажущаяся молярная масса газовой смеси.
– эффективная или
кажущаяся молярная масса газовой смеси.
Вне смеси любой газ при заданном давлении и температуре смеси (Pсм, T) занимал бы объем Vj, определяемый из уравнения
![]() (3.2)
(3.2)
Эти условные для смеси объемы называют парциальными объемами. Из уравнений (3.1), (3.2) ввиду равенства их правых частей следует, что
![]() или
или
![]() .
.
Суммируя это уравнение по j, с учетом закона Дальтона получаем
![]() .
.