Материал: Белозеров В.И., Яркин А.Н., Кузина Ю.А. Сборник задач по курсу Техническая термодинамика
Эффективную молярную массу смеси можно рассчитать, если известны объемные доли компонентов смеси ri=Vj/Vсм. Перепишем уравнение (3.2) в виде
![]()
Суммируя по j левые и правые части этого уравнения, с учетом вида уравнения состояния газовой смеси находим
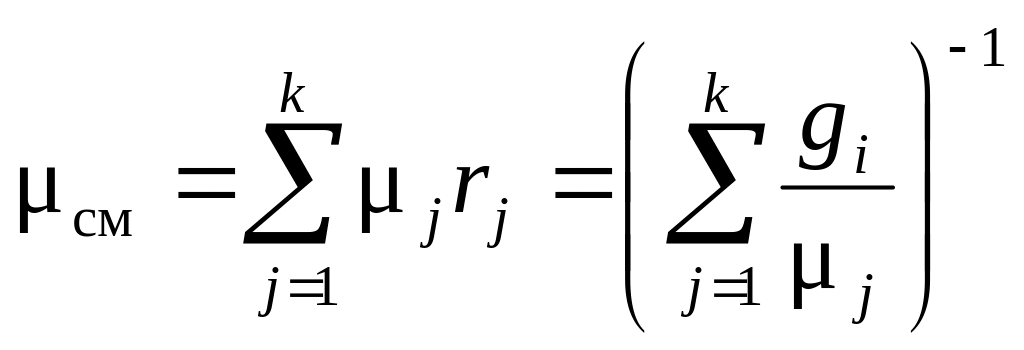 .
.
Замечание 1. Выше
было получено, что
![]() .
Из уравнения (3.1) и уравнения состояния
смеси следует, что
.
Из уравнения (3.1) и уравнения состояния
смеси следует, что
![]() ,
т.е. объемные и молярные (nj
/ n)
доли совпадают:
,
т.е. объемные и молярные (nj
/ n)
доли совпадают:
![]() .
.
Замечание 2.
Реальными величинами газовой смеси
являются количества молекул каждой
компоненты смеси (Nj).
Общее количество молекул смеси
![]() .
Поскольку каждый киломоль любого
вещества по определению содержит одно
и то же число молекул (NA),
то общее число киломолей в смеси равно
сумме киломолей компонент смеси (nj):
.
Поскольку каждый киломоль любого
вещества по определению содержит одно
и то же число молекул (NA),
то общее число киломолей в смеси равно
сумме киломолей компонент смеси (nj):
![]() .
.
По определению μсм:
a)
![]()
б)
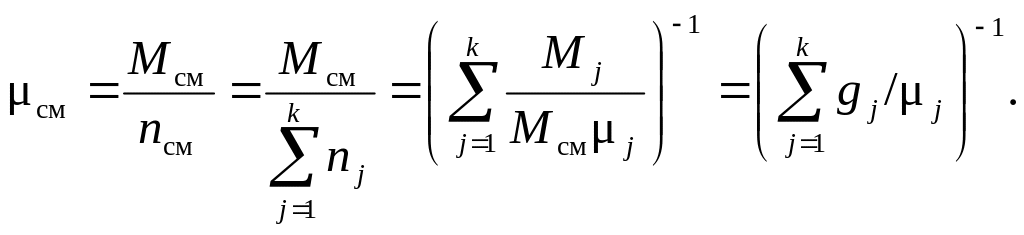
Теплоемкость смеси идеальных газов
Удельная теплоемкость вещества определяется как теплоемкость
а) единицы его массы (кг) – массовая удельная теплоемкость, сm [Дж/(кг·K)];
б) единицы его количества (кмоль) – молярная (мольная) удельная теплоемкость, сμ [Дж/(кмоль·K)];
в) единицы его объема (м3) – объемная удельная теплоемкость, с* [Дж/(м3·K)].
Для смеси идеальных газов или любой другой ее компоненты, имеющей массу M (кг), содержащей n киломолей и занимающей объем V (м3), изменение количества тепла Q и соответствующее изменение температуры T связаны уравнениями (сm, сμ , с* – средние значения)
Q= сm·M·T= сμ ·n·T= с*·Vн·T.
Здесь Vн – объем, который занимает газ массой M при нормальных физических условиях: P0=101325 Па, T0=273,15 К. Отсюда получаем соотношения:
![]()
Для смеси
![]() ,
следовательно,
,
следовательно,
![]() ,
,
![]() ,
,
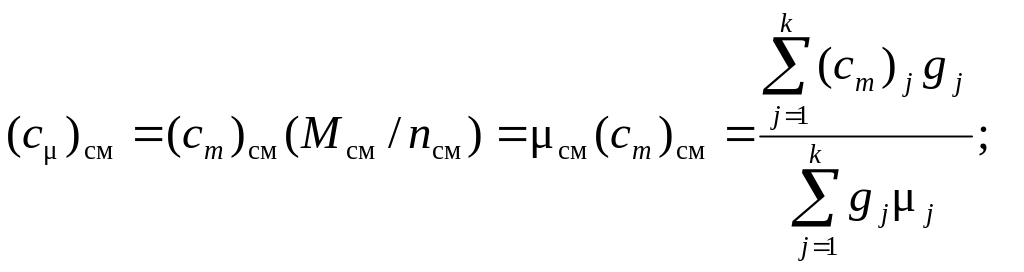
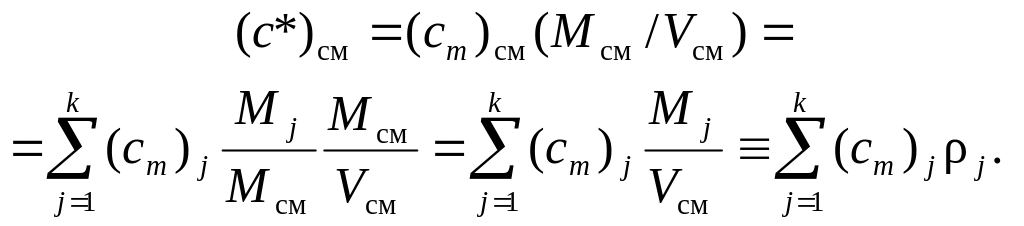
Если смесь задана объемными долями, то
![]()
и
![]()
Здесь Vj – парциальные объемы.
Задачи
3.1. Смесь 10 кг кислорода и 15 кг азота имеет давление 0,3 МПа и температуру 27ºC. Определить мольные доли zi каждого газа в смеси, кажущуюся молярную массу смеси, газовую постоянную, общий объем смеси, парциальные давления и объемы газов.
3.2. Определить газовую постоянную смеси газов, состоящей из 1 м3 генераторного газа и 1,5 м3 воздуха, взятых при нормальных физических условиях, и найти парциальные давления составляющих смеси. Плотность генераторного газа принять равной 1,2 кг/м3.
3.3. Газ коксовых печей имеет следующий объемный состав: H2=57%, CH4=23%, СО=6%, CO2=2%, N2=12%. Определить кажущуюся молярную массу смеси, массовые доли составляющий смеси, газовую постоянную, плотность смеси, парциальные давления газов при 15ºC и 1 бар.
3.4. Воздух объемом 0,3 м3 смешивается с 0,5 кг углекислого газа. Оба газа до смешения имели параметры P=0,6 МПа, t=45ºC. Определить парциальное давление углекислого газа после смешения.
3.5. Определить удельный объем пара натрия при P=1 МПа, t=927ºC, если известно, что при этих параметрах пар натрия является смесью одноатомных и двухатомных молекул мольного состава: r(Na)= 0,8628, r(Na2)=0,1372. Найти парциальные давления одно- и двухатомных паров натрия. Вычислить, как велика была бы ошибка в значении удельного объема, если бы пар натрия считался одноатомным. Молярная масса μ=23 кг/кмоль.
3.6. В энергетических установках, работающие по парогазовому циклу, в качестве рабочего тела используется смесь водяного пара и горячих продуктов сгорания топлива. Массовая доля продуктов сгорания g=0,7. Принять, что продукты сгорания обладают свойствами воздуха. Определить теплоемкость смеси cp при температуре 500 и 800ºC, а также удельный объем смеси при P=0,1 МПа и t=500ºC.
3.7. В сосуде находится смесь газов, образовавшаяся в результате смешения 10 кг азота, 13 кг аргона и 27 кг двуокиси углерода. Определить мольный состав смеси, ее удельный объем при нормальных условиях, кажущуюся молярную массу смеси и газовую постоянную, отнесенную к 1 м3 при нормальных условиях.
3.8. Влажный воздух представляет собой смесь сухого воздуха и перегретого водяного пара. Известно, что на каждый килограмм сухого воздуха во влажном воздухе приходится d граммов водяного пара. Определить массовые и объемные доли сухого воздуха и водяного пара, плотность при нормальных условиях, газовую постоянную и кажущуюся молярную массу смеси, если d=10 г/кг сухого воздуха.
3.9. Смесь газов, образовавшаяся при сжигании 1 кг мазута в топке парового котла, имеет состав, определенный парциальными объемами составляющих V(CO2)=1,85 м3, V(O2)=0,77 м3, V(N2)=12,78 м3. Определить массовые доли и парциальные давления составляющих, если общее давление P=0,1 МПа.
3.10. Сосуд разделен перегородкой на две части, объемы которых V1=1,5 м3, V2=1,0 м3. В части объемом V1 содержится двуокись углерода при P1=0,5 МПа и t1=30ºC, а в части объемом V2 – кислород при P2=0,2 МПа и t2=57ºC. Определить массовые и объемные доли двуокиси углерода и кислорода, кажущуюся молярную массу смеси и ее газовую постоянную после того, как перегородка будет убрана и процесс смешения закончится.
3.11. Горючий газ, полученный при подземной газификации угля, имеет следующий объемный состав: N2=63,6%, H2=14,5%, СО=10,0%, СO2=9,5%, H2S=0,6%, CH4=1,8%. Рассчитать приведенный к нормальным условиям объем воздуха, теоретически необходимый для сгорания 1 м3 газа, взятого также при нормальных условиях.
3.12. 2 м3 воздуха при давлении 5 бар и температуре 50ºC смешивается с 10 м3 воздуха при давлении 2 бар и температуре 100 ºC. Определить давление и температуру смеси.
3.13. В двух разобщенных между собой сосудах A и B содержатся следующие газы: в сосуде А – 50 л азота при P1 = 20 бар и t1 = 200ºC; в сосуде В – 200 л углекислого газа при P2 = 5 бар и t2 = 600ºC. Определить давление и температуру, которые установятся после соединения сосудов. Теплообменом с окружающей средой пренебречь.
3.14. Три разобщенных между собой сосуда A, B, C заполнены различными газами. В сосуде А, имеющем объем 10 л, находится сернистый ангидрид SO2 при давлении 60 бар и температуре 100ºC, в сосуде B объемом 5 л – азот при давлении 4 бар и температуре 200ºC и в сосуде C объемом 5 л – азот при давлении 20 бар и температуре 300ºC. Определить давление и температуру, которые установятся после соединения сосудов между собой. Считать, что теплообмен со средой отсутствует.
3.15. В сборном газоходе котельной смешиваются уходящие газы трех котлов, имеющих атмосферное давление. Для упрощения принимается, что эти газы имеют одинаковый состав, а именно: CO2=11,8%, O2=6,8%, N2=75,6%, H2O=5,8%. Часовые расходы газов составляют Q1=7100 м3/ч, Q2=2600 м3/ч, Q3=11200 м3/ч, а температуры газов соответственно равны t1=170ºC, t2=220ºC, t3=120ºC. Определить температуру газов после смешения и их объемный расход через дымовую трубу при этой температуре.
3.16. Определить средние объемную, мольную и массовую теплоемкости для смеси газов, состоящих из CO2 – 9%, CO – 1%, N2 – 81%, O2 – 9%. Давление смеси равно 1,5 бар, а температура 560ºF.
3.17. Определить парциальное давление кислорода, находящегося в смеси следующего объемного состава: Ar – 25%, CO2 – 39%, O2 – 36%. Смесь находится под давлением 1,5 атм при температуре 275ºR. Определить также плотность смеси.
3.18. В первом сосуде объемом 5 м3 содержится смесь газов N2 – 81%, O2 – 19%, давление в сосуде равно 15 МПа. Во втором сосуде объемом 150 л содержится He при температуре 137ºC. Определить, какое давление и температура установятся в системе из двух сосудов, если их соединить между собой.
4. Первый закон термодинамики
Подведенная к телу теплота Q расходуется на увеличение его внутренней энергии U и на совершение работы А. В дифференциальной форме уравнение первого закона (начала) термодинамики (в отсутствие обмена веществом) имеет вид
dQ=dU+dA.
Правило знаков. Теплота, подведенная к телу, считается положительной, а отведенная – отрицательной. Работа, произведенная телом, считается положительной, а работа, совершенная над телом,– отрицательной.
В СИ единицей измерения энергии является джоуль (Дж=Н·м). Теплота и работа как формы передачи энергии имеют ту же единицу измерения.
Внутренняя энергия является функцией состояния. Ее изменение в ходе любого термодинамического процесса, переводящего тело (термодинамическую систему) из одного равновесного состояния в другое равновесное состояние, определяется лишь ее значениями в начальном и конечном состояниях, т.е. U=U2–U1. Это означает, что dU является полным дифференциалом (dQ и dА таким свойством не обладают). Энергия – величина экстенсивная (аддитивная), т.е. энергия системы равна сумме энергий составляющих частей системы.
В случае, когда тело совершает работу только против сил внешнего давления, dА=PdV (работа расширения). Соответственно, уравнение первого закона термодинамики для удельных (массовых) величин с учетом правила знаков имеет вид
du = dq – Pdv. (4.1)
Здесь u=U/M (Дж/кг), q=Q/M (Дж/кг), v=V/M (м3/кг).
Энтальпия H=U+PV (Дж) так же, как и внутренняя энергия, является функцией состояния, т.к. P, V – параметры состояния. Поскольку du=dh–Pdv–vdP, уравнение первого закона в удельных величинах может быть записано в форме
dh = dq + vdP (Дж/кг). (4.2)
Произведение vdP называется располагаемой работой.
Идеальный газ. Согласно закону Джоуля внутренняя энергия идеального газа зависит только от температуры. Так как для идеального газа Pv=RT, то этим свойством обладает и энтальпия идеального газа. Прямым следствием закона Джоуля являются равенства
![]() (Дж/кг).
(Дж/кг).
сv, cp (Дж/кг K) – удельные теплоемкости в процессах подвода тепла при постоянном объеме и постоянном давлении соответственно.
Таким образом, для идеального газа уравнения (4.1) и (4.2) имеют вид
![]() (4.3)
(4.3)
Вычитая из первого уравнения второе, получим для удельных массовых теплоемкостей
![]()
![]() (Дж/(кг K))
(Дж/(кг K))
и, т.к. R=R0/,
![]() (формула Р.Майера).
(формула Р.Майера).