Материал: Spectr_lab_Grebennik

Составляющие энергии микрочастиц, как известно, квантуются, т.е. принимают значения из дискретного набора возможных. Расстояния между соседними квантовыми уровнями разных составляющих энергии существенно различаются, об этом уже шла речь в разделе 1 при анализе выражения (1.4). По формуле распределения Больцмана (11.1) возможно рассчитывать заселённость квантовых уровней энергии молекулами газа (см. раздел 11). И можно утверждать, что в выражениях (12.4) и (12.5) будут актуальны слагаемые, соответствующие тем составляющим энергии, которые в принципе существуют для данного вида молекул10 и для которых выражено распределение молекул по квантовым уровням, т.е. молекулы в равновесии находятся не только в основном состоянии, но и в возможных возбуждённых состояниях.
Статистическая термодинамика даёт строгие выражения для составляющих теплоёмкости11, которые подтверждают простой классический принцип в среднем равного распределения энергии и теплоёмкости по степеням свободы поступательного и вращательного движения молекул газа.12 Этот принцип заключается в том, что на каждую степень свободы поступательного или вращательного движения молекул газа приходится в
среднем одинаковый вклад в мольную теплоёмкость, равный R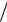 2 .
2 .
Это означает, что для любых молекул идеального газа поступательная составляющая теплоёмкости
C 3 |
R |
1,5R |
(12.6) |
пост |
2 |
|
Вращательная составляющая теплоёмкости зависит от геометрии молекулы. У одноатомных газов нет вращательных степеней свободы. Линейные молекулы имеют две вращательные степени свободы, а нелинейные – три. Следовательно:
Свращ 0 – для одноатомных газов, |
(12.7) |
||||
Свращ 2 |
R |
R – для линейных молекул, |
(12.8) |
||
|
|
||||
2 |
|
|
|
||
Свращ 3 |
R |
|
1,5R – для нелинейных молекул. |
(12.9) |
|
|
|||||
2 |
|
|
|
||
Названный классический принцип действует только для поступательной и вращательной теплоёмкостей, поскольку для соответствующих видов движения существует выраженное распределение молекул газа по
10Для одноатомных газов вращательная и колебательная составляющие не существуют.
11См., например, [6], с.165 – 168.
12Пояснение термина «число степеней свободы» см. в разделе 9.
41

энергиям. При нагревании газа энергии поступательного и вращательного движения молекул будут возрастать.
Для колебательной составляющей подобные простые формулы получить не удаётся, принцип в среднем равного распределения для колебательных степеней свободы не работает. Причина в том, что различные колебания атомов многоатомных молекул происходят с разными частотами (см. разделы 9 и 10) и характеризуются различными вкладами в теплоёмкость. Как правило, чем выше частота колебания, тем больше расстояния между колебательными уровнями и тем менее выражено распределение молекул по этим уровням, тем меньше вклад данного колебания в теплоёмкость газа. В итоге, при расчёте колебательной составляющей теплоёмкости каждый тип колебаний рассматривают отдельно.
Электронная составляющая теплоёмкости имеет ненулевое значение только у газов, молекулы которых, содержат неспаренные электроны. Для остальных газов разность энергий между основным и возбуждённым электронными состояниями оказывается очень велика по сравнению с kT и электронная составляющая теплоёмкости практически равна нулю. То же в большинстве случаев можно сказать и о ядерной составляющей, поэтому в выражениях, подобных (12.4), её обычно опускают.
Учитывая всё изложенное, можно записать простые выражения для мольных изохорной и изобарной теплоёмкостей одноатомных и двухатомных газов, молекулы которых не имеют неспаренных электронов.
Для одноатомных газов, атомы которых не содержат неспаренных электронов, существует только поступательная составляющая теплоёмкости:
CV Cпост 32 R 1,5R ,
Cp CV R 52 R 2,5R
Для двухатомных газов – поступательная и вращательная составляющие:
CV Cпост Cвращ 32 R R 52 R 2,5R ,
Cp 72 R 3,5R
При записи формулы для CV двухатомного газа пренебрегли колебательной составляющей теплоёмкости от одного колебания вдоль
42

оси молекулы. Это справедливо для двухатомных газов, состоящих из
лёгких молекул, у которых частоты колебаний атомов достаточно велики.13
Расчёт колебательной составляющей теплоёмкости многоатомного газа выполняют суммированием по всем типам колебаний с учётом их вырождения (наличия колебаний с одинаковой частотой и энергией):
Cкол giCi , |
(12.10) |
i |
|
где gi – кратность вырождения, Ci – колебательная теплоёмкость для данного типа колебаний (на одну колебательную степень свободы).
Для расчёта Ci для каждого типа колебаний требуется предварительно вычислить характеристическую температуру i :
|
hc( e )i |
, |
(12.11) |
|
|||
i |
k |
|
|
|
|
||
где ( e )i – колебательная постоянная данного |
типа колебаний, h – |
||
постоянная Планка, k – константа Больцмана. |
|
||
При расчёте по ИК-спектру поглощения вместо ( e )i в формулу
(12.11) подставляют волновое число центра соответствующей основной |
||||||||||||||
~ |
(приближение гармонических колебаний). Напомним, что |
|||||||||||||
полосы i |
||||||||||||||
значение i |
равно отношению разности колебательных энергий E E |
0 |
к |
|||||||||||
T |
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
произведению kT – см. уравнение (11.5). |
|
|
|
|
|
|
|
|||||||
По найденным значениям i |
можно |
вычислить Ci |
по формуле |
|||||||||||
Эйнштейна: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
||||
|
|
|
|
|
|
|
exp |
|
|
|
|
|
||
|
|
|
T |
T |
|
|
|
|||||||
|
C |
|
R |
|
|
|
|
|
(12.12) |
|||||
|
i |
|
|
|
|
2 |
||||||||
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
1 exp |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
T |
|
|
|
||||
13 Надо отметить, что записанные выражения достаточно точно описывают и теплоёмкость кислорода, молекула которого имеет два неспаренных электрона. В то же время, теплоёмкость одноатомного газа из атомов хлора слабо зависит от температуры, что связано именно с электронной составляющей (см. [5], табл. 44). Для двухатомных газов галогенов ошибка в Cp из за неучёта колебаний при T = 298 К будет более заметной и составит, к примеру, 14 % для
Cl2(г) и 21 % для I2(г).
43
Можно также определить Ci по таблице термодинамических
функций линейного гармонического осциллятора ([5], табл. 46, с. 93). В этой таблице даны значения колебательных составляющих термодинамических функций на одну степень свободы в зависимости от соотношения
T , значения Ci , приведенные в таблице, вычислены по формуле (12.12).
Видно, что с увеличением частоты колебаний, характеристической
температуры и соответственно соотношения |
|
вклад в теплоёмкость |
|
T |
|||
|
|
одной колебательной степени свободы Ci постепенно снижается от R до нуля.
13. Закон светопоглощения Ламберта-Бугера-Беера
При исследовании спектров поглощения веществ, в частности для аналитических целей, необходимо знать не только частоту или длину волны, при которых происходит поглощение излучения, но и количество поглощенного излучения. Последнее представляет интерес, поскольку оно однозначно связано с концентрацией поглощающих излучение частиц и позволяет определять её при наличии уравнения связи.
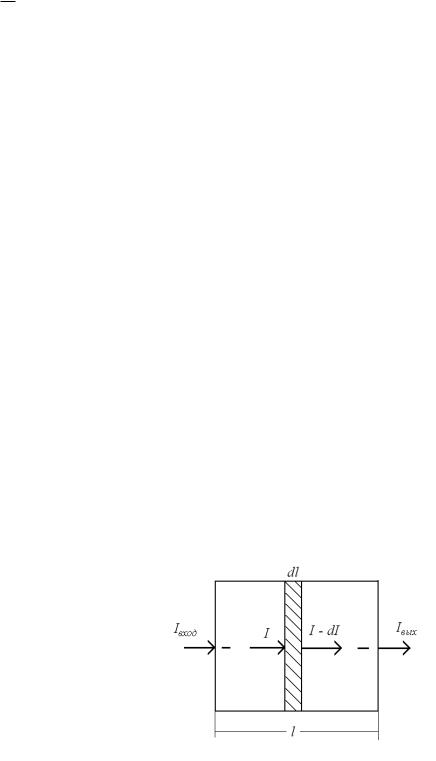
Пусть кювета (рис. 13.1) с толщиной слоя заполнена однородной поглощающей средой. Это может быть газ, жидкость или кристалл, одно индивидуальное вещество или раствор. При прохождении параллельного монохроматического пучка света через эту среду его интенсивность I уменьшается. Ослабление светового потока в данной поглощающей среде зависит, во-первых, от толщины поглощающего слоя и, во-вторых, от концентрации поглощающих частиц c. Аналитическое выражение этих зависимостей называется законом светопоглощения.
Рис. 13.1. К математической формулировке закона светопоглощения Ламберта–Бугера– Беера
44

Первую зависимость (из двух, названных выше) называют законом Ламберта–Бугера: каждый тонкий слой постоянной толщины внутри однородной среды поглощает одинаковую долю падающего на него монохроматического светового потока.
Вторая зависимость носит название закона Беера: поглощение монохроматического света данным тонким слоем внутри однородной среды пропорционально числу поглощающих частиц в единице объёма, т.е. концентрации.
Обе эти зависимости обычно объединяют и называют законом светопоглощения Ламберта–Бугера–Беера14.
Математическая формулировка закона светопоглощения основыва-
ется на утверждении, что относительное ослабление света dII (минус
указывает на поглощение света) в тонком слое не зависит от интенсивности падающего света и пропорционально толщине этого слоя d и концентрации поглощающих частиц c (рис. 13.1). Это положение, достаточно хорошо соблюдается при не слишком больших значениях интенсивности (I) и концентрации (c) и при отсутствии люминесценции15.
Для монохроматического пучка света можно записать
|
dI |
kcd , |
(13.1) |
|
I |
||||
|
|
|
где коэффициент пропорциональности k носит название коэффициента поглощения.
После интегрирования уравнения (13.1) в пределах в левой части от интенсивности входящего светового потока Iвход до интенсивности выходящего потока Iвых, а в правой части по толщине слоя от 0 до
|
|
Iвых |
dI |
|
|
|
|
|
|
|
|
|
kc d |
|
(13.2) |
||||
I |
|
||||||||
|
|
Iвход |
|
|
0 |
|
|
|
|
получаем: |
|
|
|
|
|
|
|
||
ln |
Iвход |
kc или |
I |
|
I |
|
exp( kc ) |
(13.3) |
|
|
вых |
вход |
|||||||
|
Iвых |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
||
14 Закон светопоглощения был установлен экспериментально П. Бугером в 1729 г., математически сформулирован И. Ламбертом в 1760 г. и в отношении концентрации подтвержден А. Беером в 1852 г.
15 Люминесценция – излучение света веществом, продолжающееся после поглощения квантов в течение времени, заметно превышающего период световых колебаний. При люминесценции между поглощением и испусканием кванта происходят промежуточные процессы, отличающие её от различных видов рассеяния и отражения света. По длительности люминесценции выделяют флуоресценцию (затухает быстро) и фосфоресценцию (длительное послесвечение).
45