Материал: Spectr_lab_Grebennik
соответствует небольшая энергия кванта, поэтому чисто вращательные спектры обычно наблюдаются в микроволновой или дальней ИК областях.
Если при взаимодействии излучения с веществом изменяются энергия колебаний и энергия вращения молекул газа, то спектр будет называться колебательно-вращательным. Такие спектры обычно располагаются в средней ИК области и представляют собой систему полос, расщепляющихся на отдельные линии.
Если эффекты (линии, полосы) в спектрах вызваны переходами электронов между уровнями энергии молекул газа, то такие спектры будут называться электронными, точнее электронно-колебательными или электронно-колебательно-вращательными. Электронные спектры обычно проявляются в видимой и УФ областях. Именно с избирательным пропусканием или отражением излучения в видимой области (света) при различных длинах волн связана окраска прозрачных растворов или непрозрачных систем.
Широкое применение спектроскопии в физико-химической практике привело к формированию самостоятельной области науки – спектрохимии. Всё многообразие решаемых в ней задач можно разделить на две большие группы: структурную и аналитическую.
Задачи структурной группы – исследование строения молекул, определение молекулярных констант (длин связей, моментов инерции, частот колебаний), описание энергетических состояний. На основе этой информации возможен расчёт термодинамических свойств веществ и характеристик химических реакций.
К задачам аналитической группы относятся качественный и количественный анализ химического состава системы, исследование состояния поверхности, непрерывный контроль протекания химических процессов.
2.Молекулярные спектры поглощения – основное уравнение
Выполнение закона сохранения энергии при поглощении кванта в соответствии с выражением (1.2) означает, что вещество способно поглощать не любые кванты, а только те, энергия которых равна разности энергии двух различных энергетических состояний молекул или атомов, между которыми возможен переход. Именно поэтому открытие спектров явилось одним из важнейших подтверждений квантовой теории.
Для удобства описания спектров вводят понятие «терм квантового энергетического уровня». Термом уровня называется отношение энергии
6
уровня к произведению постоянной Планка на скорость света в вакууме ( hc ). Для термов уровней различных составляющих энергии используют разные обозначения. Но универсальным остаётся правило, которое легко получить, разделив обе части уравнения (1.2) на hc :
~ |
|
|
|
|
|
E |
|
E |
|
||
|
|
|
|
|
(2.1) |
hc |
hc |
||||
Волновое число линии в спектре поглощения равно разности термов верхнего и нижнего уровней энергии молекулы, между которыми происходит переход при поглощении молекулой кванта. Отметим, что из уравнения (1.3) можно получить подобное выражение и для спектров испускания.
3. Описание вращения двухатомных молекул газа
Для описания вращения молекулы относительно оси, проходящей через центр масс перпендикулярно линии связи, используется момент
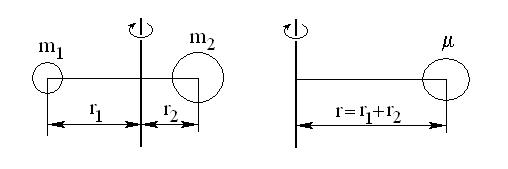
инерции: сумма произведений масс атомов ( mi ) на квадрат расстояния от ядра каждого атома до центра масс ( ri , на рис 3.1 слева):
I mi ri2 m1r12 m2r22 |
(3.1) |
i |
|
Рис. 3.1. Вращение гетероядерной двухатомной молекулы относительно оси, проходящей через центр масс (слева)
и переход к эквивалентной модели «жёсткий ротатор» (справа)
Вращение молекулы в трёхмерном пространстве при произвольном выборе системы координат описывается тензором инерции – матрицей моментов инерции размерностью 3x3. Если начало координат находится в центре масс молекулы, то тензор инерции становится диагональным – в матрице остаются не равными нулю только моменты инерции на главной
7
диагонали Ix , Iy , Iz . Они называются главными моментами инерции или
моментами инерции молекулы относительно осей координат x, y, z. Соотношение трёх главных моментов инерции зависит от геометрии
молекулы. Двухатомные молекулы являются линейными. Если провести координатную ось x вдоль оси молекулы, проходящей через ядра, то
момент инерции относительно этой оси Ix будет равен нулю. А ненулевые моменты инерции относительно осей y и z будут совпадать:
Iy Iz I |
(3.2) |
Собственные значения энергии вращения – вращательные энергетические уровни – это такие значения энергии, при которых существует решение уравнения Шредингера. Для упрощения решения этого уравнения от реальной двухатомной молекулы переходят к эквивалентной квантовомеханической модели «жёсткий ротатор» – две массы
заменяют одной (рис 3.1 справа). Для молекулы с атомами массой m1 и m2 , находящимися от центра масс на расстояниях r1 и r2 соответственно, эквивалентом будет приведенная масса , вращающаяся на постоянном расстоянии r r1 r2 от оси и дающая тот же момент инерции I , что и
двухатомная молекула.
Условие сохранения момента инерции
I m r2 m |
r2 |
r2 |
(3.3) |
|
1 1 |
2 |
2 |
|
|
с учётом выражения для центра масс |
|
|
|
|
m1r1 |
m2r2 |
(3.4) |
||
приводит к формуле для приведённой массы (вывод в Приложении 2):
|
|
|
|
m1m2 |
|
|
A1A2 |
|
|
|
|
1 |
|
, |
(3.5) |
||||
|
|
m m |
2 |
A A |
2 |
1000N |
A |
||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
1 |
|
1 |
|
|
|
|
|
|
|
||||
где A , A |
2 |
– массы атомов (а.е.м.), N |
A |
– число Авогадро (моль–1). |
|
||||||||||||||
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
При решении уравнения Шредингера получается набор собственных |
|||||||||||||||||||
значений энергии вращения жёсткого ротатора: |
|
|
|
||||||||||||||||
|
|
E |
|
|
h2 |
J(J 1) hcB J(J 1) , |
|
(3.6) |
|||||||||||
|
|
r |
8 2I |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
8
где J – вращательное квантовое число энергетического уровня, принимающее значения 0, 1, 2, 3…, B – вращательная постоянная
молекулы, связанная с её моментом инерции:
|
|
|
B |
|
h |
|
|
|
(3.7) |
||
|
|
|
|
|
|
|
|
|
|||
|
|
|
8 2cI |
|
|
|
|||||
|
Вращательный терм F(J) для уровня с квантовым числом J |
||||||||||
выражается формулой: |
|
|
|
|
|
|
|
|
|
||
|
|
|
F(J) |
Er |
|
B J(J 1) |
|
|
|
(3.8) |
|
|
|
|
hc |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
В соответствии с (3.8) вращательные термы уровней оказываются |
||||||||||
кратными вращательной постоянной молекулы (B): |
|
|
|
||||||||
J |
0 |
1 |
2 |
|
3 |
4 |
5 |
6 |
… |
||
F(J) |
0 |
2B |
6B |
|
12B |
20B |
30B |
42B … |
|||
Возможными переходами молекул между этими уровнями можно объяснить положение линий в чисто вращательных спектрах поглощения.
4.Вращательные спектры поглощения двухатомных газов
Чисто вращательные спектры поглощения газов регистрируются в микроволновой области или дальней ИК области для молекул, обладающих ненулевым дипольным моментом. Это означает, что вращательные спектры будут наблюдаться только у тех двухатомных газов, которые образованы гетероядерными молекулами (CO, HF, HCl, HBr и т.п.). Причина появления таких спектров – переходы молекул между уровнями энергии вращения при поглощении квантов.
Разрешённые переходы описываются так называемыми квантовыми правилами отбора. В данном случае возможны переходы с изменением
вращательного квантового числа J на единицу. В |
соответствии с |
||
уравнением (3.6) энергия вращения с ростом J увеличивается. Поэтому |
|||
J 1 |
– |
при поглощении кванта; |
(4.1) |
J 1 |
– |
при испускании кванта. |
(4.2) |
9
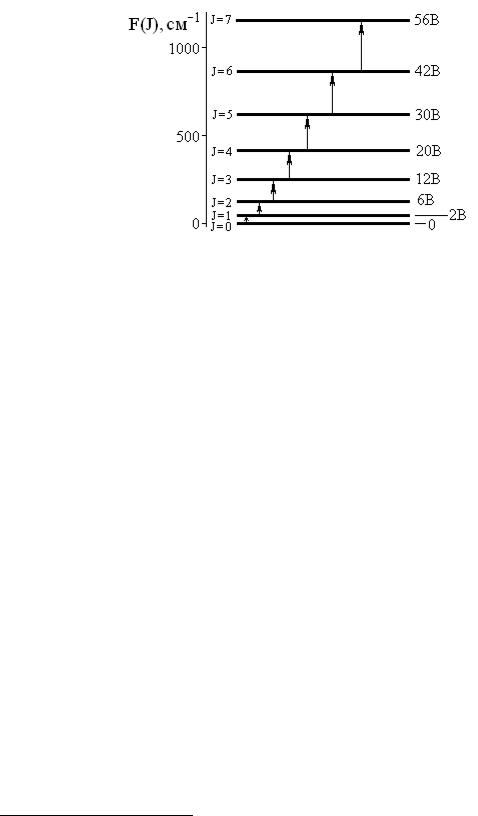
Диаграмма вращательных квантовых уровней для молекулы H19F приведена на рис. 4.1.
Рис. 4.1. Диаграмма термов вращательных квантовых уровней для молекулы H19F.
Термы первых восьми вращательных уровней на рис. 4.1 рассчитаны по уравнению (3.8) для молекулы в основном электронном состоянии с низшей энергией колебаний2. Стрелки указывают возможные переходы между уровнями при поглощении квантов.
Если квантовое число нижнего уровня обозначить J , а квантовое число верхнего уровня – J J 1, то в соответствии с (2.1) можно записать выражение для волнового числа линий в чисто вращательном спектре поглощения:
~ |
|
|
|
|
|
|
|
1) |
|
|
|
F(J ) F(J ) F(J 1) |
F(J ) B(J |
2)(J |
B(J |
1)J ,(4.3) |
|||||||
что после упрощения даёт: |
|
|
|
|
|
|
|
|
|||
|
|
|
|
~ |
|
1) |
|
|
|
|
(4.4) |
|
|
|
|
2B(J |
|
|
|
|
|||
|
Последовательно подставляя возможные значения |
J в уравнение |
|||||||||
(4.4), можно составить таблицу волновых чисел линий вращательного спектра поглощения, соответствующих переходам между уровнями, показанным стрелками на рис. 4.1:
J |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 … |
~ |
2B |
4B |
6B |
8B |
10B |
12B |
14B |
16B … |
|
Соответствующий вращательный спектр поглощения схематически изображен на рис. 4.2 на примере газообразного H19F.
2 О влиянии энергии колебаний на вращательные параметры молекулы – см. раздел 6, предварительно прочитав раздел 5.
10