Материал: Spectr_lab_Grebennik

1.Вычислите число колебательных степеней свободы молекулы газа по формуле (9.1) или (9.2).
2.Запишите выражение для изохорной теплоёмкости газа, аналогичное уравнению (12.4). Определите значения поступательной и вращательной составляющих теплоёмкости по уравнениям (12.6) – (12.9), выясните, можно ли пренебречь электронной составляющей теплоёмкости.
3.При наличии спектра определите волновые числа основных полос. Уточните данные, отнеся наблюдаемые полосы к определённому типу колебаний с помощью справочной таблицы ([5], табл. 110, с. 182).
4.Вычислите характеристические температуры колебаний i по
уравнению (12.11), рассчитайте значения отношения Ti .
5.Определите колебательную составляющую теплоёмкости расчётом по формуле (12.9) или с помощью справочной таблицы ([5], табл. 46,
с. 93).
6.Вычислите изохорную теплоёмкость по уравнению (12.4) и затем
изобарную теплоёмкость по уравнению CP CV R . Результат сравните со справочными данными ([5], табл. 44, с. 72).
7.Если требуется сравнить два результата расчёта для разных газов
сподобной пространственной структурой молекул – выполните расчёт теплоёмкости для другого газа и объясните причину различий, если они наблюдаются. Сделайте вывод.
71

Приложение 1
Параметры электромагнитного излучения и границы спектральных областей
Частота – количество колебаний в секунду, единица – Герц, 1 Гц =1с–1
Период T 1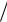 – время одного полного колебания (с).
– время одного полного колебания (с).
Длина волны – расстояние, проходимое волной в пространстве за период T. Для измерения длины волны в зависимости от области спектра используют единицы, являющиеся производными от основной единицы длины в СИ – метра: в ультрафиолетовой (УФ) и видимой областях – нанометр (1 нм = 10–9 м), в ближней и средней инфракрасной (ИК) областях – микрометр (1 мкм = 10–6 м), в дальней ИК и микроволновой
областях – мм и см.
~
Волновое число 1 – обратная длина волны или число длин волн на
единицу длины – чаще используется в ИК-спектроскопии и выражается в м–1 или в см–1.
Энергия кванта E h h |
c |
hc , |
где h 6,6262 10 34 Дж·с – |
|
|
||||
|
|
|
постоянная Планка, с = 2.99792 108 м/с – скорость света в вакууме.
В физике используют также круговую частоту 2 , её тоже можно подставить в формулу Планка для энергии кванта: E 2h 2 , где
|
h |
1,0546 10 34 Дж·с – также постоянная Планка. |
|
2 |
|||
|
|
Энергию кванта выражают, как правило, в Джоулях (Дж), допускается использование также электрон-вольта (эВ); 1 эВ = 1,6022 10 19 Дж. Для указания одного моля квантов используют наименование Эйнштейн (Эн).
Наименования и границы спектральных областей |
Таблица П1 |
||||||
Область |
Длина волны |
Волновое |
Частота |
|
Энергия Е, |
||
спектра |
, см |
|
~ |
–1 |
, Гц |
|
кДж/Эн |
число |
, см |
|
|||||
Радиоволны |
более 10 |
менее 10-1 |
менее 3∙109 |
|
менее 0,0012 |
||
Микроволновая |
10 – 10-1 |
10-1 – 10 |
3∙109 – 3∙1011 |
|
0,0012 – 0,12 |
||
ИК дальняя |
10-1 – 5∙10-3 |
10 |
– 200 |
3∙1011 – 6∙1012 |
|
0,12 – 2,4 |
|
ИК средняя |
5∙10-3 – 2∙10-4 |
200 |
– 5000 |
6∙1012 – 1,5∙1014 |
|
2,4 – 60 |
|
ИК ближняя |
2∙10-4 – 0,76∙10-4 |
5000 |
– 13000 |
1,5∙1014– 3,9∙1014 |
|
60 – 155 |
|
Видимая |
0,76∙10-4–0,4∙10-4 |
1,3∙104–2,5∙104 |
3,9∙1014– 7,5∙1014 |
|
155 – 300 |
||
УФ ближняя |
0,4∙10-4 – 0,2∙10-4 |
2,5∙104 – 5∙104 |
7,5∙1014– 1,5∙1015 |
|
300 – 598 |
||
УФ дальняя |
0,2∙10-4 – 10-6 |
5∙104 – 106 |
1,5∙1015 – 3∙1016 |
|
598 – 12000 |
||
Рентгеновское и |
менее 10-6 |
более 106 |
более 3∙1016 |
|
более 12000 |
||
γ-излучение |
|
|
|
|
|
|
|
72

Приложение 2
Вывод уравнения для расчёта приведённой массы гетероядерной двухатомной молекулы с массами атомов m1 и m2 , находящимися от центра масс на расстояниях r1 и r2 соответственно
Исходные выражения: |
|
|
|
межъядерное расстояние r r1 r2 |
(п.1) |
||
момент инерции I m r2 m |
r2 r2 |
(п.2) |
|
1 1 |
|
2 2 |
|
условие центра масс m1r1 |
m2r2 |
(п.3) |
|
Выражая m2 из (п.3), получаем:
m2 m1r1 , r2
подставляем это в выражение для суммы масс m1 m2 и преобразуем:
|
|
|
|
|
|
m1r1 |
|
|
|
|
|
|
|
r1 |
|
|
|
r2 r1 |
|
|
r |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
m1 |
m2 m1 |
|
|
|
|
m1 1 |
|
|
|
m1 |
|
|
|
m1 |
|
|
|
|
(п.4) |
||||||||||||
|
r2 |
|
|
|
r2 |
|
r2 |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
r2 |
|
|
|
|
|
|
||||||||||||
Сопоставляя первое и последнее выражение в (п.4), выразим r2 : |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
r2 |
|
|
|
|
m1 |
|
|
r |
|
|
|
|
|
|
|
|
|
|
(п.5) |
||||
|
|
|
|
|
|
|
|
|
m1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
m2 |
|
|
|
|
|
|
|
|
|
|
|
|||||||
Аналогично может быть выведено подобное выражение для r1 : |
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
r1 |
|
|
|
m2 |
|
|
r |
|
|
|
|
|
|
|
|
|
|
(п.6) |
|||||
|
|
|
|
|
|
|
|
m1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
m2 |
|
|
|
|
|
|
|
|
|
|
|
||||||||
Подставляя (п.5) и (п.6) в (п.2), получим: |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
I m r2 |
m r2 |
|
|
|
m1m22 |
|
|
r2 |
|
|
m12m2 |
|
|
r2 |
m1 m2 |
|
|
|
r2 r2 , |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
1 1 |
2 2 |
|
(m m |
|
)2 |
|
|
|
|
|
(m m |
|
)2 |
|
m m |
|
|
|
|
||||||||||||
|
|
|
2 |
|
|
|
|
|
2 |
|
2 |
|
|
|
|||||||||||||||||
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
1 |
|
|
|
|
||||||
откуда следует выражение (3.5) для приведенной массы молекулы:
m1m2 m1 m2
73
Приложение 3
Материальный баланс для слабого электролита HA, диссоциирующего в растворе на два иона
Цель составления баланса в данном случае заключается в получении выражений для равновесных молярных концентраций ионов и недиссоциированных молекул. Степень диссоциации по определению равна доле количества продиссоциировавших молекул по отношению к исходному их числу или аналогичному отношению чисел моль:
|
Nдисс |
|
nдисс |
(п.7) |
Nисходное |
nисходное |
Будем считать, что объём раствора в результате диссоциации не изменяется ( V const ), в этом случае числа моль пропорциональны
молярным концентрациям: ni ciV . Составим материальный баланс
диссоциации, традиционно записывая под уравнением процесса три строки с выражениями для числа моль соответствующего реагента или продукта – исходного, прореагировавшего и оставшегося в равновесии. Исходную концентрацию раствора электролита обозначим буквой c .
|
НА |
Н+ |
+ |
А– |
Исходное |
cV |
0 |
|
0 |
Прореагировало, |
x cV |
x cV |
|
x cV |
или образовалось |
|
|||
|
cV |
|
cV |
|
В равновесии |
cV cV |
|
||
|
(c c)V |
|
|
|
|
|
|
|
|
Количество моль продиссоциировавших молекул HA, обозначенное буквой x во второй строчке баланса, связано со степенью диссоциации в соответствии с уравнением (п.7): nдисс 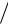 nисходное x
nисходное x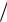 (cV), откуда x cV . Разделим выражения в третьей строке баланса на объём и получим уравнения для равновесных молярных концентраций:
(cV), откуда x cV . Разделим выражения в третьей строке баланса на объём и получим уравнения для равновесных молярных концентраций:
cHA c c, |
c |
H |
c |
A |
c |
|
|
|
|
подстановка которых в выражение (14.8) для константы диссоциации Kc
даёт уравнение, называемое законом разведения Оствальда:
K |
|
|
c |
H |
c |
A |
|
|
c c |
|
|
2c |
c |
|
|
cHA |
|
|
c c |
1 |
|||||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
||||
74
Приложение 4
Распределение цвета по длинам волн в видимом спектре
400 – 420 нм |
фиолетовый |
560 – 600 нм |
жёлтый |
420 – 450 нм |
синий |
600 – 650 нм |
оранжевый |
450 – 490 нм |
голубой |
650 – 760 нм |
красный |
490 – 560 нм |
зелёный |
|
|
Приложение 5
Молекулярные константы некоторых двухатомных молекул
Молекула |
re , Å |
Be, см 1 |
H19F |
0,917 |
20,896 |
H35Cl |
1,275 |
10,606 |
|
|
|
H79Br |
1,414 |
8,485 |
|
|
|
12С16О |
1,1283 |
1,9313 |
12С32S |
1,535 |
0,8200 |
7Li19F |
1,564 |
1,345 |
133Cs19F |
2,345 |
0,1844 |
208Pb80Se |
2,402 |
0,0506 |
6Li35Cl |
2,021 |
0,7065 |
|
|
|
28Si32S |
1,929 |
0,3035 |
118Sn32S |
2,209 |
0,1369 |
207Pb32S |
2,287 |
0,1163 |
75