Материал: Spectr_lab_Grebennik
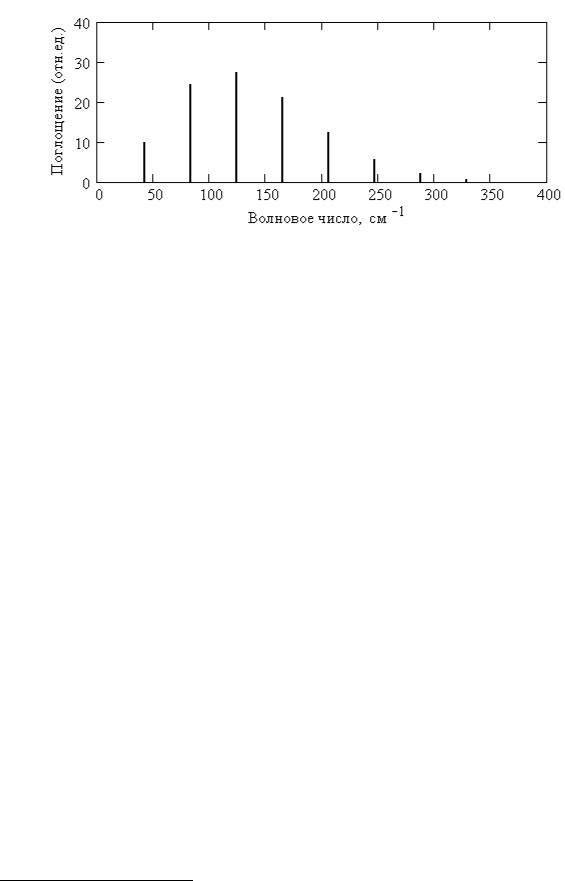
Рис. 4.2. Вращательный спектр поглощения газообразного H19F
при T = 298 К
Заметим, что линии в этом спектре расположены на одинаковых расстояниях одна от другой, разность волновых чисел соседних линий соответствует удвоенной вращательной постоянной (2B). Этот вывод можно подтвердить, выражая волновые числа соседних линий по (4.4):
~ |
~ |
|
|
|
|
1) 2B (4.5) |
i 1 |
i 2B((J |
1) 1) 2B(J |
1) 2B(J |
2 J |
||
Относительная интенсивность линий поглощения в чисто вращательном спектре определяется заселённостью молекулами исходных квантовых уровней J , с которых происходит переход. Заселённость уровня – это число молекул, имеющих соответствующее значение энергии или доля молекул с данной энергией от общего их числа. Заселённость уровней возможно рассчитать по уравнению распределения Больцмана молекул газа по энергиям вращения3. На рис. 4.2 по оси ординат отложена относительная интенсивность линий в процентах от максимально возможной в гипотетическом случае, когда все молекулы находятся на одном вращательном уровне. Эти же проценты выражают заселённость молекулами HF вращательных квантовых уровней, соответствующую доле молекул на данном уровне по отношению к общему числу молекул при температуре 298 К. Из рис. 4.2 видно, что при сколь угодно большом предполагаемом числе вращательных уровней молекулы HF при комнатной температуре только первые 7 или 8 из них оказываются заметно заселены молекулами.
Если чисто вращательный спектр поглощения вещества содержит большое число линий, то с увеличением волнового числа расстояние между линиями немного уменьшается. Это происходит из-за центробежного растяжения связи при больших энергиях вращения, когда
3 О расчёте заселённости квантовых уровней энергии молекул по уравнению распределения Больцмана см. раздел 11.
11
постепенно увеличивается длина связи – ротатор уже не является «жёстким». Для точного учёта этого эффекта в уравнение (3.8) вводят дополнительный член, включающий постоянную центробежного растяжения D:
F(J) BJ(J 1) DJ2 (J 1)2 |
(4.6) |
Использование выражения (4.6) необходимо при обработке вращательных спектров с большим числом линий, когда математические усложнения оправданы требованиями к точности расчёта.
5. Описание колебаний атомов в двухатомных молекулах
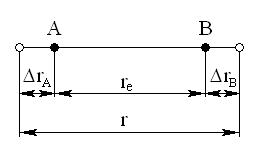
Атомы в двухатомной молекуле совершают непрерывные колебания вдоль линии, соединяющей их центры. При этом в молекуле AB периодически изменяется расстояние между атомами A и B ( r , рис. 5.1).
Рис. 5.1. Схема колебательного движения атомов в двухатомной молекуле
Существует некоторое равновесное расстояние между атомами ( re ), отклонение от которого (смещение) на величину q rA rB r re
приводит к появлению силы f , возвращающей ядра в положение равновесия.
Простейшая модель колебаний атомов в молекуле называется «гармонический осциллятор» – это система, совершающая гармонические, (т. е. синусоидальные), колебания. Для этой модели возвращающая сила f
пропорциональна смещению атомов q (закон Гука), |
коэффициент |
пропорциональности k называется силовой постоянной: |
|
f kq |
(5.1) |
При этом потенциальная энергия U пропорциональна квадрату смещения:
12
U |
1 |
kq2 |
|
1 |
k(r r )2 |
(5.2) |
|
|
|||||
2 |
|
|
2 |
e |
|
|
|
|
|
|
|||
Решение уравнения Шредингера с использованием выражения (5.2) существует при собственных значениях энергии колебаний атомов в двухатомной молекуле, рассматриваемой как гармонический осциллятор:
|
1 |
|
|
|
Ev hc e v |
|
, |
(5.3) |
|
2 |
||||
|
|
|
где v – колебательное квантовое число, которое может принимать целые неотрицательные значения (0, 1, 2, 3… ), e – колебательная постоянная
молекулы (её называют также «собственной частотой» колебаний), она имеет размерность волнового числа (см–1, м–1).
Уравнение (5.3) даёт энергию колебаний атомов одной молекулы, для вычисления энергии в расчёте на моль надо умножить выражение (5.3) на число Авогадро.
Колебательная постоянная e связана с силовой постоянной k уравнением:
|
1 |
|
|
k |
|
, |
|
|
|||||
e |
2 c |
|
|
|
||
|
|
|
||||
где – приведённая масса молекулы, вычисляемая по уравнению (3.5), c – скорость света в вакууме.
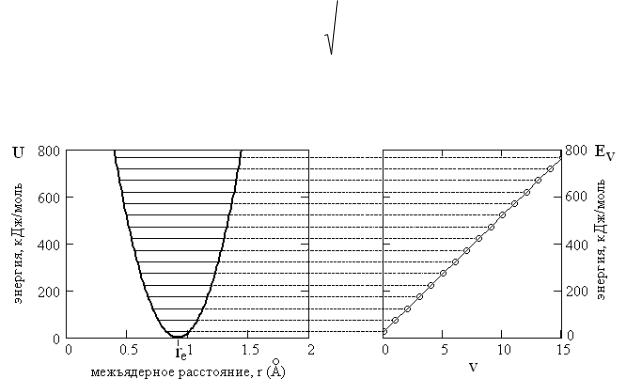
Рис. 5.2. Кривая потенциальной энергии (парабола слева) и зависимость энергии колебаний атомов от квантового числа v (прямая справа) для гармонического осциллятора на примере H19F
13
На рис. 5.2 совмещены кривая потенциальной энергии молекулы – гармонического осциллятора, рассчитанная по уравнению (5.2), и система колебательных квантовых уровней в соответствии с выражением (5.3).
Энергии U и Ev в расчёте на моль вычислены по уравнениям (5.2) и (5.3),
умноженным на число Авогадро, с использованием параметров молекулы H19F. Из рис. 5.2 видно, что с ростом смещения атомов от положения
равновесия ( r re ) потенциальная кривая уходит в бесконечность, а на ней
подобно лестнице располагаются равноотстоящие квантовые уровни. Модель гармонического осциллятора в целом противоречит экспе-
риментальным данным. Энергия колебаний атомов не может принимать сколь угодно большие значения, существует её предел, связанный с диссоциацией молекулы. Однако в тех случаях, когда существенное значение имеют только низшие колебательные уровни (в твёрдых телах), а также при расчёте термодинамических функций газов, модель гармонического осциллятора вполне приемлема и значительно упрощает математическое описание задачи. Так, в соответствии с распределением Больцмана большая часть лёгких двухатомных молекул при комнатной температуре находится на нулевом колебательном уровне. Поэтому модель гармонического осциллятора с успехом используется при расчёте термодинамических свойств газов, так как с достаточной точностью описывает уровни с квантовыми числами v 0 и
Для более точного описания потенциальной кривой двухатомной молекулы используется функция Морзе (Ф. Морзе, США, 1929 г.):
U D |
e |
1 e q 2 |
D |
e |
1 e (r re ) 2 |
, |
(5.4) |
|
|
|
|
|
|
где De – энергия диссоциации, отсчитанная от минимума потенциальной кривой, – постоянный параметр для каждой молекулы. Легко видеть, что в положении равновесия при r re экспоненциальный член в (5.4) равен единице и потенциальная энергия равна нулю. Если смещение атомов от положения равновесия q r re становится очень большим, то
происходит диссоциация молекулы. В этих условиях экспонента в (5.4) стремится к нулю, а потенциальная энергия приближается к энергии диссоциации (рис. 5.3).
Функция Морзе (5.4) существенно отличается от уравнения потенциальной энергии гармонического осциллятора (5.2), она описывает негармонические (несинусоидальные) колебания, соответствующая модель называется «ангармонический осциллятор». При использовании для потенциальной энергии функции Морзе решение уравнения Шредингера существует при собственных значениях энергии колебаний,
14
описываемых двучленным уравнением (5.5) с колебательным квантовым числом v :
|
1 |
|
|
1 |
|
2 |
|
Ev hc e v |
|
|
hc e xe v |
|
|
(5.5) |
|
2 |
2 |
||||||
|
|
|
|
|
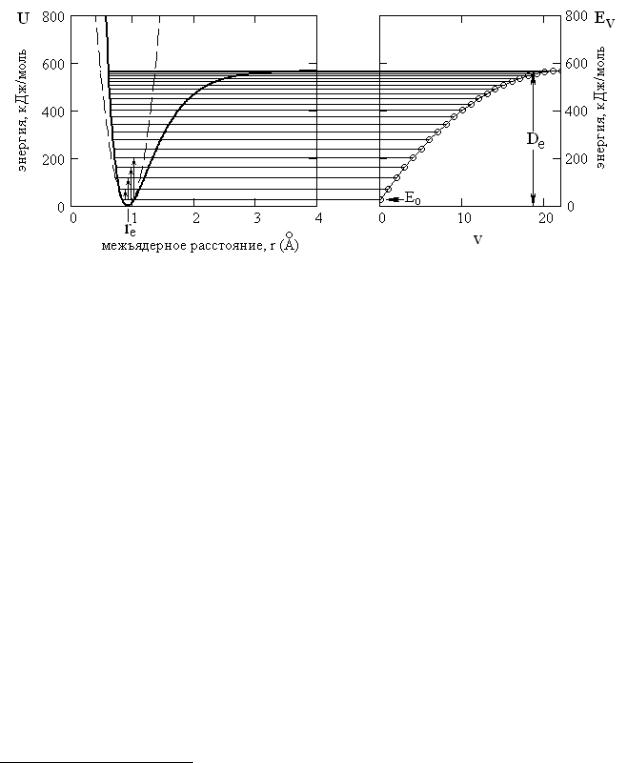
Рис. 5.3. Кривая потенциальной энергии (слева) и зависимость энергии колебаний от квантового числа v (справа) для ангармонического осциллятора на примере H19F. Пунктиром в левой части построена парабола гармонического осциллятора (рис. 5.2)
Первый член в уравнении (5.5) совпадает с уравнением (5.3) для гармонического осциллятора, второй член описывает отклонение
колебаний от гармоничности. Произведение exe имеет размерность волнового числа (см–1, м–1) и называется коэффициентом ангармоничности. Безразмерный множитель xe , обычно имеющий значения от
нескольких тысячных до нескольких сотых, также иногда называют коэффициентом ангармоничности. Уравнение (5.5), как и (5.3), даёт энергию колебаний атомов одной молекулы. Для вычисления энергии
колебаний Ev или потенциальной энергии U в расчёте на моль надо
умножить соответствующие выражения (5.5) или (5.4) на число Авогадро4. Отметим, что в соответствии с (5.5) энергия колебаний атомов на
низшем – нулевом ( v 0 ) колебательном уровне не равна нулю:
E |
|
|
1 |
hc |
|
1 |
hc x |
|
(5.6) |
0 |
|
|
e |
||||||
|
|
2 |
e |
|
4 |
e |
|
||
|
|
|
|
|
|
|
|
Это означает, что в молекуле, состоящей из двух (или более) атомов, колебания атомов происходят всегда.
4 Что и было сделано при построении графиков, показанных на рис. 5.3.
15