Материал: Spectr_lab_Grebennik
Несовпадение числа полос в спектре поглощения с числом внутримолекулярных колебаний возможно по двум причинам (здесь и далее речь будет идти только об основных полосах поглощения).
Во-первых, как уже указывалось, некоторые колебания атомов многоатомных молекул могут быть вырожденными, т.е. иметь одинаковые частоты. Если у молекулы имеется несколько таких колебаний, то число различных частот по сравнению с числом колебаний будет меньше, а вся группа вырожденных колебаний даст лишь одну основную полосу в ИК-спектре поглощения. Чем выше симметрия молекулы, тем больше степень вырождения некоторых колебаний и тем больше групп вырожденных колебаний имеет молекула.
Во-вторых, при различных колебаниях молекула обладает разной способностью к поглощению электромагнитной энергии – не каждое колебание активно в ИК-спектре поглощения. Согласно классической электродинамике поглощение электромагнитной энергии должно сопровождаться изменением осцилляции электрических зарядов в поглощающей среде. Поэтому в ИК-спектре поглощения будут активны только те колебания, при которых происходит смещение центров тяжести электрических зарядов, т.е. изменяется дипольный момент молекулы P . На это указывает ненулевая производная дипольного момента по
соответствующей колебательной координате qi : |
|
||||
|
P |
|
|
|
|
|
|
0 |
(10.1) |
||
|
|||||
|
|
|
|
|
|
|
qi |
qi 0 |
|
||
|
|
|
|
||
При этом постоянный (равновесный) дипольный момент молекулы может быть равен нулю, что характерно, например, для неполярных молекул
CO2, СН4, ВF3, C6H6).
Далее рассмотрим описание типов колебаний и основных полос колебательно-вращательных спектров поглощения для нескольких многоатомных газов.
Линейные и нелинейные трёхатомные молекулы ХУ2
На рис. 10.1 приведены (схематически, без соблюдения масштаба) формы колебаний молекул СО2 и H2O.
Молекула СО2 линейная, в равновесном состоянии межъядерное расстояние С–O re 1,16 10 10 м или 1,16 Å. Число колебательных
степеней свободы этой молекулы равно 4. Имеются два валентных и два деформационных колебания (рис. 10.1а), однако последние имеют одинаковую частоту, т.е. являются вырожденными, кратность вырождения
31
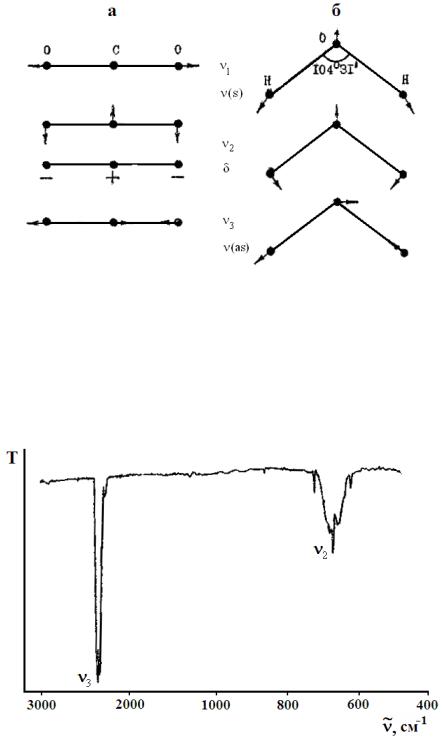
равна двум. Движение ядер в этом случае можно представить как суммарный результат колебаний в двух взаимно перпендикулярных плоскостях. Таким образом, молекула СО2 имеет три частоты колебаний: ν1 (валентное симметричное), ν2 (деформационное антисимметричное) и ν3 (валентное антисимметричное). В размерности волнового числа им соответствуют значения 1388,17 см–1, 667,4 см–1 и 2349,16 см–1.
Рис. 10.1. Формы колебаний молекул CO2 (a) и H2O (б)
Из них ν2 и ν3 удовлетворяют условию (10.1), поэтому в ИК-спектре поглощения СО2 (рис. 10.2) наблюдаются две полосы, соответствующие частотам ν2 и ν3.
Рис. 10.2. ИК-спектр поглощения CO2
32
Молекула Н2О – нелинейная, в равновесном состоянии межъядерное расстояние О–Н re 0,957 10 10 м или 0,957 Å, угол между связями
НОН = 104°31'. Вырождение колебаний для неё отсутствует, поэтому трём колебательным степеням свободы соответствуют три частоты колебаний ν1, ν2 и ν3 (волновые числа 3656,65 см–1, 1594,78 см–1 и 3755,79 см–1 соответственно). Все три частоты удовлетворяют условию (10.1) и поэтому проявляются в виде основных полос в ИК-спектре поглощения.
Пирамидальные четырёхатомные молекулы ХУ3, ХУ2Z
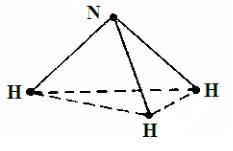
Рассмотрим молекулу аммиака NH3. Три атома водорода лежат в основании симметричной пирамиды, вершину которой занимает атом азота (рис. 10.3). В равновесном состоянии угол между связями HNH = 107°17', а межъядерное расстояние (N–H) re = 1,0156·10–10 м или 1,0156 Å.
Рис. 10.3. Строение молекулы аммиака
Число колебательных степеней свободы для этой молекулы равно 6, однако из-за симметричного строения два колебания имеют одинаковую частоту, т.е. являются вырожденными (кратность вырождения равна 2). Вследствие этого молекула NH3 имеет 4 колебательные частоты ν1 – ν4 (волновые числа 3336,68 см–1, 950,42 см–1, 3443,47 см–1 и 1627,75 см–1). Все четыре частоты активны в ИК спектре поглощения, так как колебания удовлетворяют условию (10.1).
На рис. 10.4 представлен ИК-спектр поглощения NH3, а в табл. 10.2 показаны формы соответствующих колебаний атомов в молекуле. Каждая полоса в ИК-спектре поглощения NH3 расщепляется на две полосы вследствие так называемого "инверсионного удвоения" частот. Последнее возникает в пирамидальных молекулах, для которых равновероятны две конфигурации (рис. 10.5а). Если потенциальный барьер между этими конфигурациями невелик, то молекула может переходить из одной конфигурации в другую. В результате каждый колебательный уровень расщепляется на два (положительный и отрицательный). "Инверсионное удвоение" частот в ИК-спектре поглощения является следствием переходов молекул NH3 между двумя уровнями различных знаков (рис. 10.5б).
33
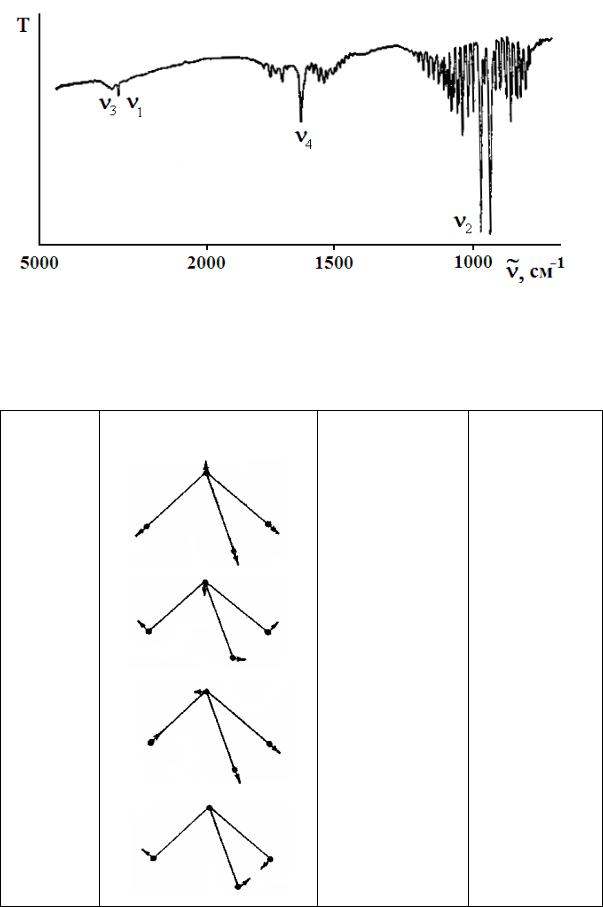
Рис. 10.4. Колебательно-вращательный ИК-спектр поглощения газообразного аммиака (инверсионное удвоение наиболее заметно для частоты симметричных деформационных колебаний ν2 )
Таблица 10.2. Формы колебаний атомов в молекуле NH3
Частота |
Форма колебания |
Обозначение |
Степень |
|
вырождения |
||||
|
|
|
||
ν1 |
|
ν(s) |
1 |
ν2 |
δ(s) |
1 |
ν3 |
ν(as) |
2 |
ν4 |
δ(as) |
2 |
34

Рис. 10.5. Равновесные конфигурации молекулы аммиака (а); разрешенные колебательные переходы в ИК-спектре поглощения (б) – иллюстрация инверсионного удвоения частот.
Колебательные переходы в многоатомных молекулах (как и в случае двухатомных молекул) сопровождаются вращательными переходами. Если инфракрасный спектрофотометр обладает хорошей разрешающей способностью, то в спектрах поглощения веществ в газовой фазе можно наблюдать тонкую структуру, обусловленную переходами между вращательными уровнями колебательных состояний v 0 и v 1 (тонкая структура основной полосы, подобная показанной на рис. 7.2 и 7.4).
В отличие oт двухатомных молекул, в колебательно-вращательной полосе поглощения многоатомных молекул наряду с Р-ветвью ( J 1) и R-ветвью ( J 1) может наблюдаться лежащая между ними Q-ветвь, соответствующая переходам без изменения вращательного квантового числа ( J 0 ) (рис. 10.6). Волновое число полосы в спектре определяют по положению Q-ветви, если она не расщепляется на вращательные линии. В тех случаях, когда Q-ветвь не наблюдается, положение полосы определяют по её центру – по среднему волновому числу двух ближайших к центру линий в Р- и R-ветвях так же, как это делают в случае двухатомных молекул.
Рис. 10.6. Колебательно-вращательная полоса валентного антисимметричного колебания газообразного метана.
35