Материал: Spectr_lab_Grebennik
также будут проявлять молекулы, обладающие постоянным дипольным моментом.
Молекулы типа сферического волчка. К этой группе относятся молекулы тетраэдрического и октаэдрического строения (CH4, CCl4, SF6), имеющие несколько осей симметрии. Для молекул данного типа главные моменты инерции относительно трёх пространственных осей координат
совпадают: Ix Iy Iz I 0 . Вращательные уровни для молекул
такого типа определяются тем же уравнением (3.6), что и для двухатомных молекул.
Молекулы типа симметричного волчка. К этой группе относятся,
например, молекулы, имеющие форму симметричной пирамиды и плоские молекулы в форме правильных фигур, они имеют одну ось симметрии. Поскольку для молекул этого типа два главных момента инерции равны, но отличаются от третьего, вращательный терм таких молекул усложняется и содержит две вращательные постоянные А и В и два вращательных квантовых числа J и К:
F(J, K) BJ(J 1) (A B)K2 , |
(8.1) |
||||||||
где |
|
|
|
|
|
|
|
|
|
A |
|
h |
|
и |
B |
h |
|
|
|
|
|
|
|
|
|
||||
8 2cI |
|
8 2cI |
B |
|
|||||
|
|
|
A |
|
|
|
|||
В этих выражениях IA |
– момент инерции относительно оси |
||||||||
симметрии молекулы, IB – |
момент |
инерции относительно |
осей, |
||||||
перпендикулярных оси симметрии; J и К – вращательные квантовые числа, которые принимают значения целых чисел: К = 0, 1, 2,...; J = К,
К+1, К+2,... .
Молекулы типа асимметричного волчка. Это наиболее сложный случай, поскольку молекулы данного типа не имеют осей симметрии. Выражение для энергии вращения Еr здесь существенно усложняется, приходится вводить три вращательные постоянные. Вращательные спектры поглощения таких молекул чрезвычайно сложны.
Вращательные спектры поглощения многоатомных молекул наблюдаются только в том случае, если молекулы обладают постоянным дипольным моментом. По этой причине линейные симметричные молекулы (например, CO2, CS2, C2H4), все молекулы типа сферического волчка и некоторые молекулы типа симметричного волчка (например, C6H6) не дают чисто вращательных спектров поглощения, так как их равновесный дипольный момент равен нулю.
Переходы между вращательными уровнями неполярных многоатом-
26
ных молекул можно наблюдать в колебательно-вращательных спектрах поглощения в средней и ближней ИК областях, а также при изучении спектров комбинационного рассеяния.
9.Колебательные состояния многоатомных молекул
Колебательно-вращательный спектр поглощения двухатомных газов, рассмотрен в разделе 7. Он соответствует переходам между уровнями энергии колебаний атомов в молекуле вдоль линии связи (см. рис. 5.1). Такие колебания называются валентными, это единственный тип колебаний атомов в двухатомной молекуле. В спектре ему соответствуют одна основная полоса (основной тон) и один набор обертонов. Другими словами, двухатомные молекулы имеют одну колебательную степень свободы.
Колебательно-вращательный ИК спектр поглощения многоатомных газов значительно сложнее. Это объясняется тем, что многоатомные молекулы имеют не одну, а как минимум 3 колебательных степени свободы, причём с ростом количества атомов в молекуле число колебательных степеней свободы увеличивается.
Степень свободы – термин из математики. В узком смысле число степеней свободы – это разность количества независимых переменных и количества независимых уравнений их связи. В более широком смысле степень свободы – это незафиксированная координата, от которой зависят свойства системы. В данном случае число степеней свободы – количество независимых координат, необходимых для описания того или иного вида движения конкретной молекулы.
Для описания поступательного движения любой молекулы газа в трёхмерном пространстве в общем случае требуется три координатные оси (x, y, z). Поэтому молекула любого газа имеет 3 поступательные степени свободы.
Число вращательных степеней свободы молекулы газа определяется её строением. У одноатомных молекул нет вращательных степеней свободы. Если один атом установить в начале координат – его вращение не приводит к различимым изменениям. Линейные молекулы имеют две вращательные степени свободы, так как одну из трёх осей координат – например, x – можно провести вдоль оси молекулы и, тем самым, исключить её (к различимым изменениям будет приводить вращение вокруг двух оставшихся осей y и z). Нелинейные молекулы имеют три вращательные степени свободы.
27
Число колебательных степеней свободы n зависит от числа атомов в молекуле ( N ) и определяется по формулам:
n 3N 5 (для линейных молекул) |
(9.1) |
n 3N 6 (для нелинейных молекул) |
(9.2) |
Эти выражения легко обосновать. У частиц одноатомного газа кинетическая энергия распределена по трём степеням свободы поступательного движения, так как каждый отдельный атом имеет три поступательных степени свободы. Если мы представим себе N несвязанных атомов в пространстве (двигающихся независимо), то такая система будет иметь 3N поступательных степеней свободы. Если из этих N атомов образована молекула (между атомами возникли связи), то она сохраняет те же 3N степеней свободы, которые имели N свободных атомов. Но эти 3N степеней свободы молекулы распределяются по различным видам движения. Три из них приходятся на поступательное движение молекулы, две (для линейных) или три (для нелинейных) – на вращательное движение молекулы как целого. Остальные (3N 5 или 3N 6 ) приходятся на изменение формы молекулы, на её изгибание или растяжение её связей, т.е. на колебательное движение. Это и есть число колебательных степеней свободы молекулы или число независимых колебательных координат, описывающих колебательное движение атомов.
Колебания ядер молекулы представляют собой сложное явление. В классическом (т.е. основанном на законах классической механики) приближении колебания многоатомных молекул при малых амплитудах можно считать гармоническими (как и в случае двухатомных молекул). На основании теории малых колебаний было показано, что любое сколь угодно сложное колебательное движение молекулы в гармоническом приближении можно разложить на n независимых движений, которые называются нормальными колебаниями. Каждое нормальное колебание совершается с определённой частотой νi, которая называется частотой данного нормального колебания – основной (фундаментальной) частотой.
Для описания колебательного движения атомов линейной или
нелинейной молекулы вводят соответственно 3N 5 или |
3N 6 |
колебательных координат. В качестве таких координат удобно выбрать величины, характеризующие изменение расстояний между ядрами и изменение углов между связями (по отношению к их равновесным значениям). Такая система внутренних координат получила название валентно-силовой системы координат, а сами координаты – естественных колебательных координат qi.
Так, для трёхатомной нелинейной молекулы, имеющей 3 колебательные степени свободы (3 3 6 ), можно ввести 3 колебательные координаты (рис. 9.1), две из которых отвечают изменению расстояний
28
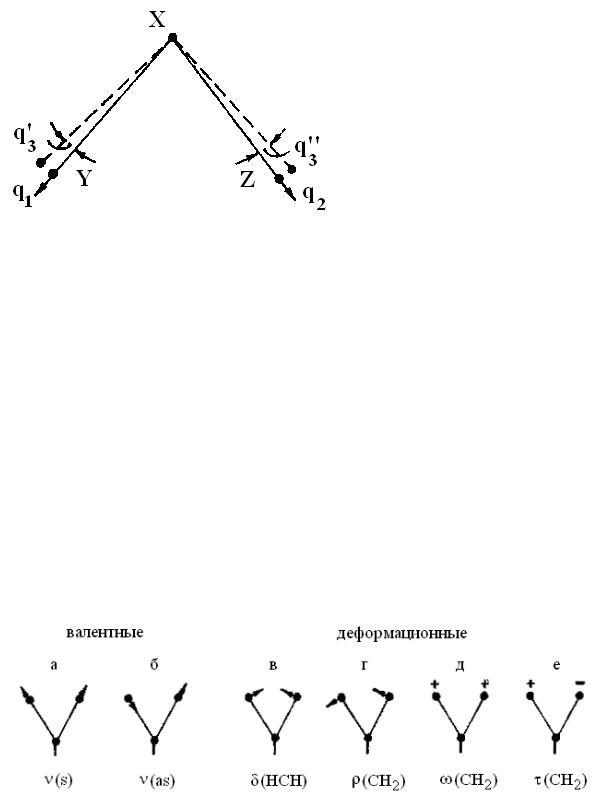
XY(q1) и XZ (q2), а третья – изменению утла между связями YXZ (q3). Таким образом, молекула XYZ имеет три нормальных колебания и, следовательно, три основных частоты колебаний.
Рис. 9.1. Внутренние колебательные координаты трёхатомной молекулы:
|
|
q1 , q2 , q3 q3 |
q3 |
Величина и направление амплитуд смещения ядер для данного нормального колебания определяют его форму, исходя из которой колебания разделяют на валентные ( ) и деформационные ( ).
Валентными называют колебания, при которых в основном изменяются длины связей, а углы между связями и другие углы в пространственной конфигурации молекулы остаются почти неизменными.
Деформационными называют колебания, при которых в пространственной конфигурации молекулы в основном изменяются углы между связями и другие углы, а длины связей изменяются незначительно. И те и другие колебания могут быть симметричными (s) или антисимметричными (as), если подобные атомы совершают колебания в одной фазе или в противофазе соответственно.
В качестве примера на рис. 9.2 схематически показаны колебания атомов водорода метиленовых (=СН2) групп (“а” – валентное симметричное, “б” – валентное антисимметричное, “в” – ножничное, “г” – маятниковое, “д” – веерное, “е” – крутильное).
Рис. 9.2. Колебания атомов водорода метиленовых групп
29

Чисто валентные и чисто деформационные колебания встречаются редко, чаще всего они проявляются у линейных или высокосимметричных молекул. Для большинства молекул характерны смешанные колебания, в которых одновременно изменяются и длины связей, и углы.
Для молекул с низкой симметрией число различных частот нормальных колебаний равно числу колебательных степеней свободы (возможны только невырожденные колебания). В более симметричных молекулах7 некоторые нормальные колебания различной формы совершаются с одинаковой частотой. Такие колебания называют
вырожденными, а число таких колебаний – степенью вырождения.
Колебания могут быть дважды или трижды вырожденными, причём в молекуле может быть несколько групп вырожденных колебаний. Примеры описания типов колебаний многоатомных молекул имеются в справочнике
[5] (табл.110, с.182–186).
10.Общие представления о колебательных спектрах поглощения многоатомных газов
Число колебательных степеней свободы n для молекулы газа несложно найти по формулам (9.1) или (9.2). Казалось бы, число основных полос8 в спектре поглощения должно соответствовать числу n. В то же время эксперимент показывает, что число основных полос часто бывает меньше числа внутримолекулярных колебаний. Табл. 10.1 иллюстрирует это на примере нескольких веществ.
Таблица 10.1 Соотношение числа основных полос в спектре поглощения и числа колебательных степеней свободы молекулы
|
Число колебательных |
Число частот |
Число основных |
|
Молекула |
полос в ИК спектре |
|||
степеней свободы |
колебаний |
|||
|
поглощения |
|||
|
|
|
||
H2O |
3∙3 – 6 = 3 |
3 |
3 |
|
CO2 |
3∙3 – 5 = 4 |
3 |
2 |
|
NH3 |
3∙4 – 6 = 6 |
4 |
4 |
|
CH4 |
3∙5 – 6 = 9 |
4 |
2 |
|
CHCl3 |
3∙5 – 6 = 9 |
6 |
6 |
7Речь идёт в первую очередь о молекулах типа симметричного волчка или о молекулах типа сферического волчка, имеющих оси симметрии (см. раздел 8).
8Основная полоса или полоса основного тона в спектре поглощения соответствует переходу молекулы с нулевого колебательного уровня v=0 на уровень v=1 (см раздел 7, рис. 7.1). В спектрах поглощения двухатомных газов такая полоса одна, что соответствует одной колебательной степени свободы.
30