Материал: Spectr_lab_Grebennik
Следовательно, излучение с длиной волны 1 преимущественно поглоща-
ется недиссоциированными молекулами HA, их концентрация с ростом pH уменьшается, так как равновесие (14.1) при этом смещается вправо.
Второй максимум (при 2 ) наиболее выражен в щелочных средах, а с уменьшением pH его интенсивность снижается. Это означает, что излучение с длиной волны 2 преимущественно поглощается анионами
А–, концентрация которых возрастает с увеличением pH.
Все кривые спектров на рис. 14.1 пересекаются в одной "изобестической" точке, где оптическая плотность не зависит от рН, так как интенсивность поглощения квантов частицами HA и А– одинакова.
Слева и справа от изобестической точки оптическая плотность i-го раствора при данном значении рН будет складываться из составляющих для молекулярной и анионной форм:
|
|
Ai HAcHA |
A |
c |
A |
|
(14.3) |
|||||
|
|
|
|
|
|
|
|
|
|
|||
Если общая концентрация вещества в растворе равна c , а степень |
||||||||||||
диссоциации кислоты в i-м растворе равна i , то |
|
|||||||||||
|
|
Ai HAc(1 i ) |
A |
c i |
(14.4) |
|||||||
|
|
|
|
|
|
|
|
|
|
|
||
или |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ai |
|
i ) |
|
|
|
|
|
(14.5) |
||
|
|
A (1 |
A |
i |
||||||||
|
и |
|
|
c – |
предельные оптические |
плотности |
||||||
где A HAc |
A |
A |
||||||||||
раствора соответственно в кислой (α = 0, cHA c) и в щелочной (α = 1, cA c ) средах при λ = const.
Из уравнения (14.5) находим степень диссоциации электролита:
i |
Ai A |
(14.6) |
|
A A |
|||
|
|
Все значения оптической плотности здесь должны быть измерены при одной длине волны, соответствующей максимуму поглощения молекулярной или анионной форм.
Таким образом, степень диссоциации слабого электролита α можно найти для каждого раствора с заданным значением рН, причём расчёты можно вести как по одной, так и по другой полосе поглощения. Для параоксипропиофенона λ1 = 273 нм, λ2 = 323 нм.
Термодинамическая константа диссоциации Ka слабой кислоты HA
51

может быть выражена через равновесные активности ионов и молекул в растворе:
K |
aH aA |
(14.7) |
a aHA
Если речь идёт о разбавленном водном растворе слабого электролита, то взаимодействием (взаимным притяжением или отталкиванием) ионов можно пренебречь. В названном случае это действительно так, поскольку количество ионов в растворе невелико, они расположены далеко друг от друга. Это означает, что коэффициенты активности в данной системе близки к единице, и можно упростить задачу, перейдя к анализу эмпирической (т.е. получаемой по эксперимен-
тальным данным) константы диссоциации Kc , выражаемой через равновесные молярные концентрации электролита и ионов:
|
|
|
|
|
|
|
K |
|
|
cH |
cA |
|
|
|
|
|
|
|
|
|
(14.8) |
||
|
|
|
|
|
|
|
c |
cHA |
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
18 |
c |
|
c , |
а cHA c (1 ) , |
|
|
|
|
c |
A |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||
Так как |
|
A |
то дробь |
|
|
|
|
|
можно заменить |
||||||||||||||
|
cHA |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
на |
|
|
. Тогда после подстановки в (14.8) и логарифмирования получаем: |
||||||||||||||||||||
|
|
||||||||||||||||||||||
1 |
|||||||||||||||||||||||
|
|
|
|
|
|
|
lg Kc |
lg c |
|
|
lg |
|
|
|
|
|
|
|
(14.9) |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Вводя величины |
pKc lg Kc |
и |
pH lg c |
H |
, можно записать |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
окончательное уравнение для расчёта рКс:
pKc pH lg |
|
|
(14.10) |
|
|
||
|
|
||
1 |
|
||
Расчёт по уравнению (14.10) даёт значение pKc – показателя эмпирической или кажущейся константы диссоциации Kc , которая в общем случае зависит от ионной силы раствора. Если получить ряд значений pKc при различной ионной силе раствора, можно найти значение pKa lg Ka , применяя графическую экстраполяцию на нулевую ионную силу.
18 Вывод выражений для равновесных концентраций молекул и ионов см. в Приложении 3.
52
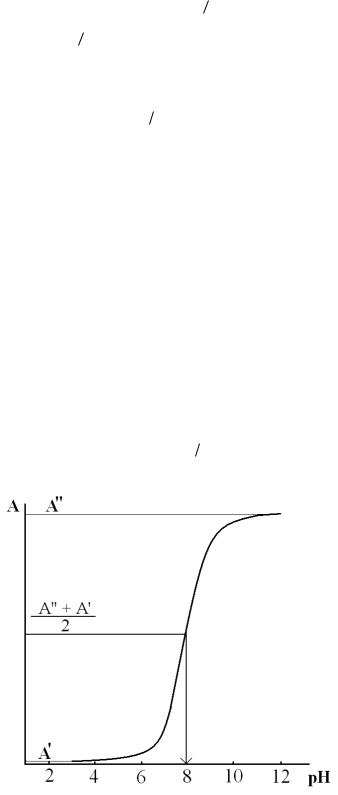
Определение pKc по уравнению (14.10) можно провести и графически. Если 0,5 то pKc pH1 2 (второе слагаемое в равенстве
(14.10) равно 0), где pH1 2 – так называемый "половинный показатель", т.е. значение pH , при котором 50 % вещества находится в диссоциированном состоянии.
Для нахождения pKc pH1 2 строят график зависимости оптичес-
кой плотности от рН при постоянной длине волны максимума поглощения λ1 или λ2. На рис. 14.2 показан пример такого графика для оптической плотности растворов параоксипропиофенона при длине волны λ2, при которой основными поглощающими частицами являются анионы.
Выполнение закона Беера относительно концентрации поглощающих частиц при равных начальных концентрациях электролита (c) приводит к уравнению прямо пропорциональной связи между оптической плотностью A и степенью диссоциации электролита α. Например, если
поглощающими частицами являются анионы, то A |
A |
c |
A |
|
A |
c . |
|
|
|
|
|||
Это означает, что степени диссоциации 0,5 на графике соответствует |
||||||
средняя арифметическая оптическая плотность (A A )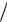 2 между двумя
2 между двумя
её предельными значениями A и A при низких и высоких pH. По кривой на графике при средней оптической плотности на шкале абсцисс
находят соответствующее значение pH1 2 pKc .
Рис. 14.2. Графическое определение рКc параоксипропиофенона по оптической плотности при длине волны максимума
поглощения его анионной формы (λ2). Значение рКc = рН1/2= 8,1
53
Определив pKc , можно вычислить |
константу диссоциации по |
|
формуле: |
|
|
Kc 10 |
pKc |
(14.11) |
|
||
В случае графического определения константы диссоциации слабой кислоты по значениям оптической плотности недиссоциированных молекул при длине волны λ1 кривая зависимости A от pH, аналогичная показанной на рис 14.2, будет убывающей. Значения pKc, найденные по поглощению при λ1 и при λ2 должны приблизительно совпадать.
15. Практические работы по спектрохимии
В этом разделе дано описание практических работ (номера работ соответствуют действующим в лаборатории кафедры физической химии РХТУ им. Д. И. Менделеева). Для каждой работы приведены контрольные вопросы и ссылки на учебный материал данного пособия для подготовки, а также основные этапы обработки экспериментальных данных.
Работа № 42. Расчёт константы диссоциации слабого электролита по электронным спектрам поглощения растворов
Контрольные вопросы:
1.Закон светопоглощения Ламберта–Бугера–Беера. Его определение и математическая формулировка. Понятия оптической плотности и процента пропускания, связь между ними. Коэффициент погашения, его физический смысл и экспериментальный способ определения.
2.Причины отклонений от закона Беера. Графическое выражение закона Беера.
3.Константа диссоциации и степень диссоциации одноосновной слабой кислоты, уравнение их связи.
4.Принцип определения константы диссоциации слабых электролитов в растворах спектрофотометрическим способом. Вид спектра поглощения слабой кислоты в зависимости от рН буферного раствора.
5.Расчёт степени диссоциации слабой кислоты по оптической плотности, соответствующей поглощению света анионами или молекулами кислоты. Вычисление рКс по этим данным.
6.Графический метод определения рКс.
Разделы пособия для подготовки к работе: 1, 13, 14, Приложения 3, 4
54
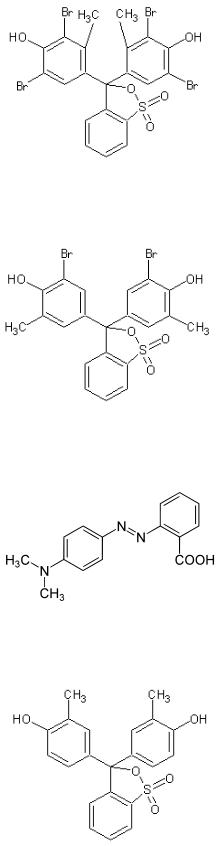
Задание 1. Определение константы диссоциации бромкрезолового зелёного в водном растворе. Рабочий диапазон рН от 3 до 9.
Структурная формула бромкрезолового зелёного:
Задание 2. Определение константы диссоциации бромкрезолового пурпурного в водном растворе. Рабочий диапазон рН от 3 до 12.
Структурная формула бромкрезолового пурпурного:
Задание 3. Определение константы диссоциации метилового красного в водном растворе. Рабочий диапазон рН от 1,9 до 7.
Структурная формула метилового красного:
Задание 4. Определение константы диссоциации крезолового красного в водном растворе. Рабочий диапазон рН от 3 до 12.
Структурная формула крезолового красного
55