Материал: Spectr_lab_Grebennik
Таким образом, при прохождении монохроматического света через поглощающую среду его интенсивность экспоненциально уменьшается в зависимости от толщины поглощающего слоя ( ) и концентрации (c).
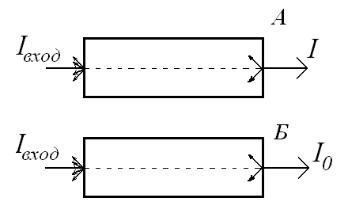
На практике приходится, однако, учитывать, что ослабление светового потока в кювете происходит как в результате поглощения, так и в результате рассеяния и отражения, особенно при прохождении пучка через границу раздела фаз у стенок кюветы. Поэтому для определения поглощения света именно исследуемой средой (веществом, раствором) применяют так называемую двухлучевую схему с кюветой сравнения
(рис. 13.2).
Рис.13.2. Ослабление светового потока в кювете с поглощающим веществом (А) и в кювете сравнения (Б).
Если пропустить свет через вторую такую же кювету, но заполненную непоглощающей средой (например, прозрачным растворителем в случае исследования раствора), то в ней ослабление светового потока произойдет только из-за рассеяния и отражения от стенок кюветы, А эти явления (рассеяние и отражение от стенок) в рабочей кювете и в кювете сравнения идентичны. Таким образом, для учёта собственной поглощающей способности вещества необходимо сравнивать световой поток I, прошедший через кювету с поглощающим веществом (кювета А на рис. 13.2), и световой поток I0, прошедший через кювету сравнения (Б):
ln |
I0 |
|
kc |
(13.4) |
||
I |
||||||
|
|
|
|
|||
I I |
0 |
e kc |
(13.5) |
|||
|
|
|
|
|
||
Переходя к десятичным логарифмам и вводя обозначение
46
|
|
|
lg |
I0 |
|
A , |
(13.6) |
||
|
|
|
I |
|
|||||
|
|
|
|
|
|
|
|
||
получаем: |
|
|
|
|
|
|
|
|
|
|
|
|
A |
|
k |
c |
(13.7) |
||
|
|
|
|
|
|||||
|
|
|
|
|
2.3 |
|
|||
Величину А называют оптической плотностью (экстинкцией, |
|||||||||
погашением), а дробь |
k |
|
– коэффициентом погашения (коэффициентом |
||||||
2.3 |
|||||||||
|
|
|
|
|
|
|
|||
экстинкции) и обозначают буквой . |
|
|
|
|
|||||
Окончательно закон светопоглощения обычно записывают в виде: |
|||||||||
|
|
|
A c |
(13.8) |
|||||
На основании уравнения (13.8) можно дать следующую формулировку объединённого закона светопоглощения Ламберта– Бугера–Беера: при данной длине волны оптическая плотность прямо пропорциональна концентрации поглощающих частиц ( c ) и толщине поглощающего слоя ( ).
Оптическая плотность обладает свойством аддитивности, т.е. для смеси веществ, подчиняющихся закону светопоглощения и не вступающих в химическое взаимодействие друг с другом, оптическая плотность при данной длине волны равна сумме оптических плотностей компонентов ( = const):
A Ai ici |
(13.9) |
|
i |
i |
|
где εi и ci – соответственно, коэффициент погашения и концентрация i-го компонента смеси.
При использовании молярной концентрации ε называют молярным коэффициентом погашения. Если концентрацию выражают в моль/л, а толщину поглощающего слоя в см, то молярный коэффициент погашения имеет размерность л/(моль см). Очевидно, что ε численно равен величине оптической плотности А при = 1 см и c = 1 моль/л.
Кроме оптической плотности, на практике часто используют процент пропускания Т излучения образцом:
T |
I |
100 (%) |
(13.10) |
|
|||
|
I0 |
|
|
47
Оптическая плотность (A) и процент пропускания (T) связаны
между собой соотношением: |
|
A 2 lg T |
(13.11) |
Коэффициент погашения ε зависит от природы поглощающей среды, и длины волны падающего света, а значения А и Т зависят, кроме того, ещё от концентрации c и толщины поглощающего слоя .
В эксперименте, переходя от одной длины волны к другой или меняя концентрацию, часто приходится работать с кюветами различной толщины. Для того, чтобы иметь возможность сравнивать данные разных
опытов, используют приведённую оптическую плотность A , которая не
зависит от толщины поглощающего слоя.
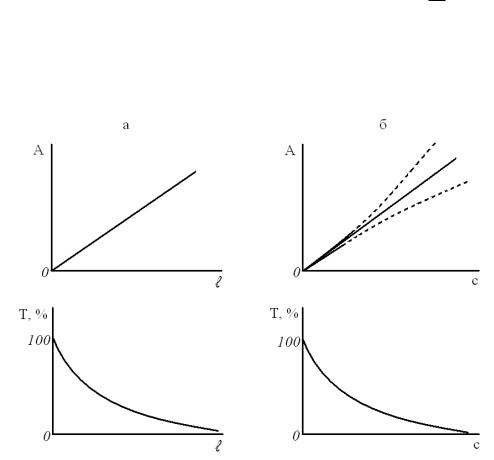
На рис. 13.3 показаны варианты графического представления законов светопоглощения.
Рис. 13.3. Графическое представление законов светопоглощения при λ = const: а – закон Ламберта–Бугера (c = const); б – закон Беера ( = const); пунктир – отклонения от закона Беера
Наблюдаемые иногда на практике отклонения от закона Беера (рис. 13.3б) могут быть вызваны физико-химическими или инструментальными причинами. Физико-химические причины включают в себя все явления, связанные с изменением состояния поглощающих частиц при изменении концентрации, вследствие чего истинная концентрация поглощающих
48

частиц в растворе отличается от исходной концентрации исследуемого вещества (рассчитанной по исходно взятому его количеству). Причиной этого могут быть процессы диссоциации, ассоциации, полимеризации или комплексообразования, протекающие в растворе с участием частиц исследуемого вещества.
Инструментальные причины связаны с особенностями устройства и работы спектрофотометрических приборов и в основном сводятся к двум факторам: недостаточно строгой монохроматичности светового потока и недостаточной точности работы фотоприёмников излучения. Чтобы устранить первую причину, необходимо работать при довольно узких выходных щелях спектрофотометров или использовать излучение лазеров. Вторая причина заставляет проводить измерения в таком диапазоне оптических плотностей, где ошибка наименьшая (сигнал от излучения из кюветы с исследуемым раствором во много раз больше собственного шума фотоприёмника). Обычно считают, что удовлетворительные по точности результаты в смысле выполнения закона светопоглощения можно получать в диапазоне А = 0,2 – 0,8. Однако в каждом конкретном случае этот интервал должен быть уточнён на основании эксперимента.
14. Изучение равновесия диссоциации слабых электролитов в растворах
Для определения степени и константы диссоциации слабых электролитов в растворах можно воспользоваться спектрофотометрическим методом. Решение задачи оказывается простым, если в электронном спектре поглощения возможно выделить две различные полосы, характерные для молекулярной и ионизированной форм данного вещества.
Пусть какая-либо одноосновная слабая кислота диссоциирует по схеме:
НА Н+ + А–, |
(14.1) |
Слабые электролиты диссоциируют на ионы частично, равновесная степень диссоциации 0 < α < 1. При этом в растворе находятся как молекулы НА, так и анионы А–, в спектре раствора (в видимой и/или в ультрафиолетовой областях) могут одновременно наблюдаться по крайней мере две полосы поглощения, связанные с этими частицами (гидратированный ион водорода не поглощает во всей УВИ области16). При изменении степени диссоциации (вследствие разбавления раствора,
16«УВИ область» – краткое обозначение сочетания ультрафиолетовой, видимой и инфракрасной областей.
49
изменения рН среды, температуры или природы растворителя) соотношение между интенсивностями этих полос будет меняться. Проще всего повлиять на положение равновесия (14.1), изменяя pH среды с помощью буферных растворов. В пределе при α = 1 (в щелочной среде) в спектре раствора останется только одна полоса, соответствующая поглощению квантов анионами А–. В другом предельном случае при α = 0 (в кислой среде) эта полоса исчезнет, а полоса поглощения, отвечающая молекуле НА, достигнет максимальной для данной концентрации интенсивности.
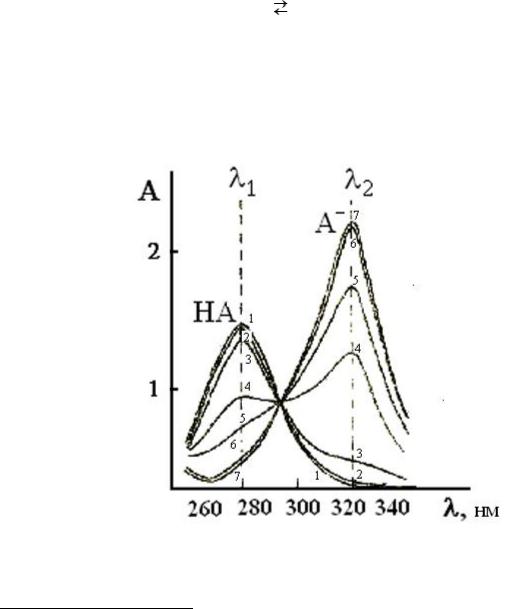
На рис. 14.1 представлен пример семейства спектров поглощения17, отвечающих различным значениям степени диссоциации при разных значениях рН буфера для слабой органической кислоты параоксипропиофенона, уравнение диссоциации которого в водном растворе имеет вид:
HO-C6H4-CO-C2H5 Н+ + (О-С6Н4-СО-С2Н5) –, |
(14.2) |
что соответствует равновесию (14.1).
В спектрах растворов видны два максимума поглощения при длинах волн 1 и 2 . Первый максимум (при 1 ) проявляется в кислой среде, при данной длине волны оптическая плотность снижается с ростом pH.
Рис. 14.1. Спектры поглощения растворов параоксипропиофенона при рН = 4,0 (1); 5,0 (2); 7,0 (3); 8,0 (4); 8,5 (5); 11,0 (6); 12,0 (7)
17 По существу это электронно-колебательные полосы поглощения, их появление связано с переходами электронов с одновременным изменением энергии колебаний атомов.
50