Материал: GMP_prefinal
-
Приведите перечень типов лекарственных препаратов, которые подлежат обязательной государственной регистрации и обоснуйте, почему каждый из этих типов включен в этот перечень.
Согласно п. 2 ст. 13 Закона «Об обращении ЛС» государственной регистрации подлежат:
-
все лекарственные препараты, впервые подлежащие вводу в обращение в РФ;
-
лекарственные препараты, зарегистрированные ранее, но произведенные в других ле-карственных формах в соответствии с перечнем наименований лекарственных форм, в но-вой дозировке при доказательстве ее клинической значимости и эффективности;
-
новые комбинации зарегистрированных ранее лекарственных препаратов.
Статья 13. Государственная регистрация лекарственных препаратов (в ред. Федерального закона от 22.12.2014 N 429-ФЗ)
-
В Российской Федерации допускаются производство, изготовление, хранение, пе-ревозка, ввоз в Российскую Федерацию, вывоз из Российской Федерации, реклама, отпуск, реализация, передача, применение, уничтожение лекарственных препаратов, если они за-регистрированы соответствующим уполномоченным федеральным органом исполнитель-ной власти.
(часть 1 в ред. Федерального закона от 13.07.2015 N 241-ФЗ)
-
Государственной регистрации подлежат:
-
все лекарственные препараты, впервые подлежащие вводу в обращение в Россий-ской Федерации;
-
лекарственные препараты, зарегистрированные ранее, но произведенные в других лекарственных формах в соответствии с перечнем наименований лекарственных форм, в новой дозировке при доказательстве ее клинической значимости и эффективности;
-
новые комбинации зарегистрированных ранее лекарственных препаратов.
-
Государственная регистрация лекарственных препаратов осуществляется по ре-зультатам экспертизы лекарственных средств, а государственная регистрация орфанных лекарственных препаратов осуществляется по результатам экспертизы документов, пред-ставленных для определения возможности рассматривать лекарственный препарат для медицинского применения при осуществлении государственной регистрации в качестве орфанного лекарственного препарата, и по результатам экспертизы лекарственных средств.
-
Государственная регистрация лекарственного препарата осуществляется соот-
ветствующим уполномоченным федеральным органом исполнительной власти в срок, не
превышающий ста шестидесяти рабочих дней со дня принятия соответствующе-го заявления о государственной регистрации лекарственного препарата. В указанный срок включается время, необходимое для повторного проведения экспертизы лекарственного средства в соответствии со статьей 25 настоящего Федерального закона. Срок государ-ственной регистрации лекарственного препарата исчисляется со дня принятия соответ-ствующим уполномоченным федеральным органом исполнительной власти соответству-ющего заявления о государственной регистрации лекарственного препарата с приложени-ем необходимых документов по день выдачи регистрационного удостоверения лекар-ственного препарата. Время, необходимое для направления уполномоченным федераль-ным органом исполнительной власти запроса о представлении необходимых материалов и представления заявителем ответа на данный запрос в соответствии со статьями 16, 19 и 23 настоящего Федерального закона, не учитывается при исчислении срока госу-дарственной регистрации лекарственного препарата.
-
Государственной регистрации не подлежат:
73
-
лекарственные препараты, изготовленные аптечными организациями, ветеринар-ными аптечными организациями, индивидуальными предпринимателями, которые имеют лицензию на фармацевтическую деятельность, по рецептам на лекарственные препараты и требованиям медицинских организаций, ветеринарных организаций;
-
лекарственные препараты, приобретенные физическими лицами за пределами Российской Федерации и предназначенные для личного использования;
-
лекарственные препараты, ввозимые в Российскую Федерацию для оказания ме-дицинской помощи по жизненным показаниям конкретного пациента на основании раз-решения, выданного уполномоченным федеральным органом исполнительной власти;
-
лекарственные средства, ввозимые в Российскую Федерацию на основании вы-данного уполномоченным федеральным органом исполнительной власти разрешения и предназначенные для проведения клинических исследований лекарственных препаратов и (или) проведения экспертизы лекарственных средств для осуществления государственной регистрации лекарственных препаратов;
-
фармацевтические субстанции;
-
радиофармацевтические лекарственные препараты, изготовленные непосред-ственно в медицинских организациях в порядке, установленном уполномоченным феде-ральным органом исполнительной власти;
-
лекарственные препараты, производимые для экспорта.
-
Не допускается государственная регистрация:
-
лекарственных препаратов, отличающихся друг от друга качественным составом действующих веществ, под одинаковым торговым наименованием;
-
одного лекарственного препарата, представленного на государственную регистра-цию в отношении одного и того же держателя или владельца регистрационного удостове-рения лекарственного препарата в виде двух и более лекарственных препаратов под раз-личными торговыми наименованиями.
-
Объясните, почему лекарственные препараты-дженерики зани-мают значительную нишу на лекарственном рынке рф и других стран. Ответ обоснуйте.
Дженерик (англ. generic, воспроизведённое лекарство) — это лекарство-копия, кото-рое совпадает с оригиналом по количеству действующего вещества и влиянию на орга-низм.
Когда изобретают новое лекарство, его долго исследуют и тестируют, а потом оформляют патент. Когда срок патента заканчивается, другие компании тоже могут про-изводить подобные лекарства — дженерики. Но в России права патентообладателей ча-сто нарушаются, и дженерики регистрируются и продаются ещё до того, как закончится патент на оригинальное лекарство.
По закону (ст. 18 федерального закона от 12.04.2010 N 61-ФЗ (ред. от 28.12.2017) «Об обращении лекарственных средств») для регистрации дженерика вместо отчёта о соб-ственных доклинических исследованиях можно предоставить обзор научных работ о ре-зультатах доклинических исследований воспроизводимого препарата, а вместо отчёта о собственных клинических исследованиях — отчёт о результатах исследований биоэквива-лентности воспроизведённого лекарства.
Биоэквивалентность показывает степень и скорость всасывания, время достижения максимальной концентрации в крови, распределение в тканях и жидкостях организма, а также скорость выведения.
Так что исследования, доказывающие эффективность и безопасность нового джене-рика, всё же проводятся, однако они не такие долгосрочные и дорогие, как в случае ори-гинального лекарства.
74
ПРЕИМУЩЕСТВА:
Цена на дженерики значительно ниже, чем на оригинальные препараты, при этом дженерики не отличаются от оригинальных средств по эффективности и безопасности, и производятся в строгом соответствии с установленными регламентами и стандартами ка-чества.
Использование дженериков имеет большое медико-социальное значение, поскольку делает качественное лечение доступным для широких слоев населения. Например, в США в настоящее время более 60% всех выписываемых лекарственных средств состав-ляют дженерики. Сходная статистика наблюдается и в странах Западной Европы: Герма-нии, Австрии, Швейцарии и др.
Широкое применение дженериков позволяет более рационально расходовать национальный бюджет, выделяемый на цели здравоохранения, и, таким образом, созда-вать финансовый резерв для оплаты дорогостоящих медицинских продуктов, процедур и услуг. В свою очередь, ценовая конкуренция со стороны производителей дженериков под-талкивает инновационные компании к созданию принципиально новых, более современ-ных препаратов и методов лечения.
-
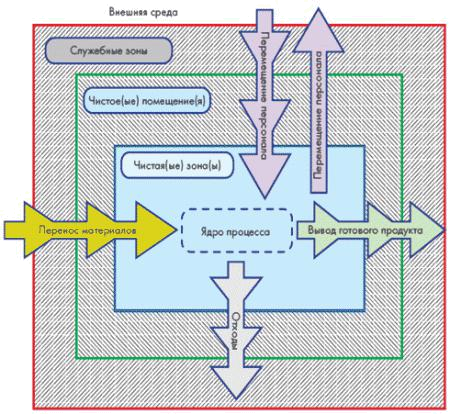
Создание чистого помещения основано на принципе «комната в комнате». Поясните на примере зоны чистоты класса а, каким об-разом образуется рабочая зона чистого помещения.
“Чистое” помещение (ЧП) - производственное помещение и/или зона для изготовления лекарственных средств с чистотой воздуха, нормируемой по содержанию механических частиц определенного размера и жизнеспособных микроорганизмов, сконструированное
-
используемое таким образом, чтобы свести к минимуму проникновение, распростране-ние, образование и сохранение механических частиц и микроорганизмов внутри этих по-мещений.
-
основе архитектурно - строительных решений при создании чистого помещения ле-жит принцип построения «комната в комнате». Рабочая зона чистого помещения образу-ется пространством, ограниченным с помощью герметизированных элементов ограждаю-щих конструкций
• Класс А — локальная зона для операций, представляющих особый риск для качества продукции, например зоны дозирования, закупоривания емкостей, откупоривания ампул и флаконов, смешивания в асептических условиях.
• Класс В — окружающая среда для зоны класса А в случае изготовления и наполнения в асептических условиях.
• Классы C и D — чистые зоны для осуществления менее критичных стадий производ-ства стерильной продукции.
Рабочая зона и производственная среда – классы чистоты?
• Изолирующая технология (А – D)
• Технология «выдувания/наполнения/герметизации (A – C)
• Продукция подвергаемая финишной стерилизации (A – C)
• Асептическое производство (A –B)
Обеспечение класса чистого помещения достигается следующими приемами:
1) обеспечение подачи потока стерильного воздуха в ламинарном, турбулентном или смешанном режиме;
2) создание перепада давления между помещениями разных классов чистоты;
3) использование базовых элементов чистых помещений;
4) использование изоляторов или минизон;
5) Комплекс мероприятий, состоящий из влажной уборки, дезинфекции и возможного УФ-облучения стен, полов и других поверхностей.
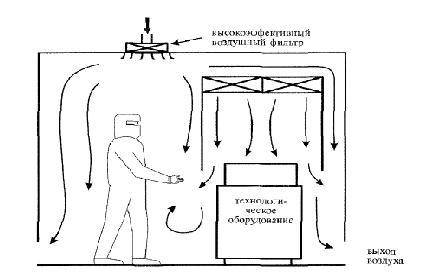
Чистое помещение со смешанным потоком
75
-
Этот тип представляет собой турбулентно вентилируемое чистое помещение, но там, где продукт может подвергнуться загрязнению, используется лабораторный шкаф
(бокс) с однонаправленным воздушным потоком.
Чистая зона (clean zone) - ограниченное пространство, в котором счетная концентрация аэрозольных частиц и концентрация жизнеспособных микроорганизмов в воздушной среде поддерживаются в пределах не выше заданного, соответствующего определенному классу частоты, и в котором, по мере необходимости, контролируются другие параметры (напри-мер, скорость ламинарного воздушного потока). Чистая зона может быть открытой или замкнутой и может находиться как внутри, так и вне "чистого" помещения.
76