Материал: Chast1giper
6.15 Внутрішня енергія системи. Кількість теплоти. Перше начало термодинаміки
Внутрішня енергія – це сума кінетичної енергії атомів і молекул, потенціальної енергії їх взаємодії, атомна, ядерна енергія і т.д. за винятком кінетичної і потенціальної енергії системи як цілого. Внутрішня енергія є функцією стану системи. Це означає, що певному стану системи відповідає єдине значення внутрішньої енергії незалежно від того, як вона потрапила в цей стан. Внутрішню енергію можна змінити трьома процесами:
а) за рахунок виконання системою чи над нею роботи. Наприклад, при стискуванні газу в циліндрі від рухомого поршня молекули будуть відбиватись з швидкістю більшою на подвоєну швидкість поршня, ніж падають (див. розділ 4.8). А це означає збільшення кінетичної енергії хаотичного руху молекул, тобто внутрішньої енергії газу, при виконанні над ним роботи по його стисканню. Аналогічно при розширенні газу, тобто при виконанні ним роботи, молекули будуть відбиватись від поршні з меншою швидкістю, ніж падати. Отже, якщо система виконує роботу, її внутрішня енергія зменшується. Якщо над системою виконується робота, її внутрішня енергія зростає;
б) за рахунок теплообміну, тобто передачі або відбиранні теплової енергії без виконання механічної роботи. Цю енергію називають теплотою. Якщо тепло передається системі, її внутрішня енергія зростає, якщо ж забирається – зменшується;
в) за рахунок зміни кількості частинок системи. Цей процес поки що розглядати не будемо, тобто будемо вивчати системи незмінної кількості частинок.
Таким чином механічна робота і теплота являються мірою зміни внутрішньої енергії. Тому ці три фізичні величини мають однакову розмірність – джоуль (Дж). Одиницею теплоти являється позасистемна одиниця – калорія. Це кількість теплоти, необхідна для нагрівання 1 г води від 19,5оС до 20,5оС. Еквівалентність теплоти і роботи експериментально встановив Джоуль по нагріванню ртуті при її перемішуванні лопатками, які приводились в рух падаючою гирею. Він встановив механічний еквівалент теплоти 1 кал = 4,19 Дж.
Таким
чином із врахуванням знаків роботи,
кількості теплоти і з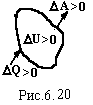 міни
внутрішньої енергії (рис.6.20), можна
сформулювати закон збереження енергії
(перше начало
термодинаміки):
міни
внутрішньої енергії (рис.6.20), можна
сформулювати закон збереження енергії
(перше начало
термодинаміки):
![]() (6.38)
(6.38)
Т![]() епло
∆Q,
передане системі, іде на зміну
∆U
її внутрішньої енергії і на виконання
системою роботи
∆A.
епло
∆Q,
передане системі, іде на зміну
∆U
її внутрішньої енергії і на виконання
системою роботи
∆A.
-
Степені вільності молекул. Розподіл енергії по степеням вільності. Внутрішня енергія ідеального газу
Числом степеней вільності називається мінімальна кількість незалежних величин, якими можна однозначно задати положення системи у просторі.
![]() Для
матеріальної точки (молекула одноатомного
газу) у просторі достатньо задати три
координати x,
y,
z.
Ці координатні степені вільності
називаються поступальними. Для двохатомної
жорсткої молекули можна задати 6 координат
її атомів. Але вимога мінімальності
приводить до того, що положення такої
молекули задають трьома координатами
одного із атомів і два кути (рис.6.21):
меридіальний θ і азимутальний φ. Ці
кутові степені вільності називаються
обертальними. Всього одержали
Для
матеріальної точки (молекула одноатомного
газу) у просторі достатньо задати три
координати x,
y,
z.
Ці координатні степені вільності
називаються поступальними. Для двохатомної
жорсткої молекули можна задати 6 координат
її атомів. Але вимога мінімальності
приводить до того, що положення такої
молекули задають трьома координатами
одного із атомів і два кути (рис.6.21):
меридіальний θ і азимутальний φ. Ці
кутові степені вільності називаються
обертальними. Всього одержали
![]() ,
а не 6 поступальних. Для двохатомної
нежорсткої молекули, тобто коли відстань
між атомами може змінюватись, що має
місце при досить високих температурах,
тобто атоми коливаються, потрібно задати
ще одну степінь вільності. Ця степінь
вільності називається коливальною.
Одержуємо
,
а не 6 поступальних. Для двохатомної
нежорсткої молекули, тобто коли відстань
між атомами може змінюватись, що має
місце при досить високих температурах,
тобто атоми коливаються, потрібно задати
ще одну степінь вільності. Ця степінь
вільності називається коливальною.
Одержуємо
![]() .
.
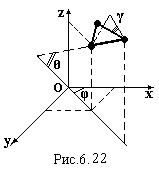 Для
трьохатомної жорсткої молекули необхідно
задати, як і для двохатомної жорсткої
молекули, три координати одного атома
і три кути (рис.6.22). Третій кут γ задає
орієнтацію площини молекули. Одержуємо
Для
трьохатомної жорсткої молекули необхідно
задати, як і для двохатомної жорсткої
молекули, три координати одного атома
і три кути (рис.6.22). Третій кут γ задає
орієнтацію площини молекули. Одержуємо
![]()
![]() .
У випадку нежорсткої трьохатомної
молекули необхідно задати ще 3 відстані
між атомами – 3 коливальні степені
вільності. Всього буде 9. Із збільшенням
кількості атомів буде зростати кількість
коливальних степенів вільності, а
поступальних і обертальних буде по 3.
Таким чином, система із N
частинок має
.
У випадку нежорсткої трьохатомної
молекули необхідно задати ще 3 відстані
між атомами – 3 коливальні степені
вільності. Всього буде 9. Із збільшенням
кількості атомів буде зростати кількість
коливальних степенів вільності, а
поступальних і обертальних буде по 3.
Таким чином, система із N
частинок має
![]() степеней вільності.
степеней вільності.
Теплова
енергія по степеням вільності
розподіляється рівномірно, тобто на
кожну поступальну і обертальну степінь
припадає енергія
![]() ,
а на коливальну
,
а на коливальну
![]() (
(![]() на кінетичну енергію коливань атомів
в молекулі,
на кінетичну енергію коливань атомів
в молекулі,
![]() на потенціальну енергію їх взаємодії).
Кількість половинок kT
теплової енергії молекули позначимо
буквою і. Тоді
на потенціальну енергію їх взаємодії).
Кількість половинок kT
теплової енергії молекули позначимо
буквою і. Тоді
![]() .
(6.39)
.
(6.39)
Досить часто мають справу з невисокими температурами, коли коливальні степені ще не збуджуються. Тоді число і дорівнює числу n кількості степеней вільності. Тому досить часто число і називають кількістю степеней вільності.
Середня
теплова енергія молекули, яку розглядають
не як матеріальну точку, включає не
тільки поступальну енергію, а і обертальну
та коливальну. Тому ![]() .
(6.40)
.
(6.40)
Внутрішня енергія ідеального газу складається тільки із теплової енергії молекул, потенціальна енергія дорівнює нулю, так як молекули не взаємодії між собою.
Отже,
![]() ,
(6.41)
,
(6.41)
де: NA – число Авогадро, m – маса газу, μ – молярна маса, k – стала Больцмана, R – газова стала, Т – абсолютна температура.
Вираз (6.41) показує, що внутрішня енергія даної кількості газу залежить тільки від температури.
-
Робота газу в ізопроцесах

Н![]() ехай
газ, який знаходиться в циліндрі під
поршнем площею S,
розширюючись, переміщує його на відстань
dx
(рис.6.23). Тиск газу Р. За означенням
елементарна механічна робота дорівнює
ехай
газ, який знаходиться в циліндрі під
поршнем площею S,
розширюючись, переміщує його на відстань
dx
(рис.6.23). Тиск газу Р. За означенням
елементарна механічна робота дорівнює
![]()
 ,
(6.42)
,
(6.42)
а
загальна робота
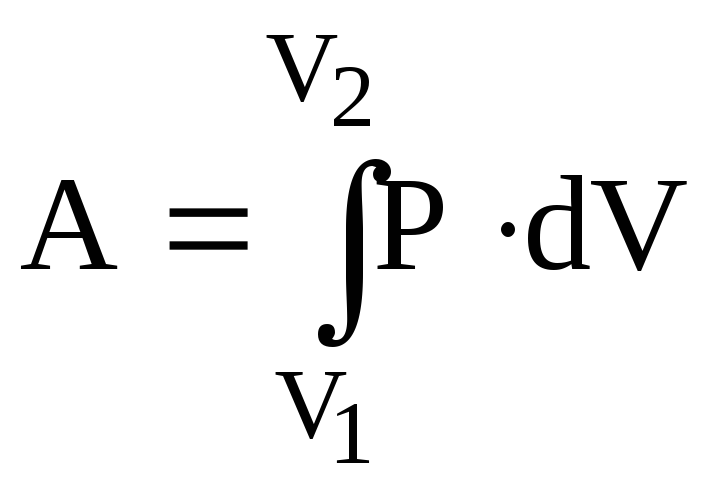 .
(6.43)
.
(6.43)
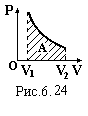
![]() Графічно
в координатах Р-V
робота газу дорівнює площі криволінійної
трапеції, яка обмежена графіком процесу,
віссю об’єму V
і лініями V1
= const,
V2
= const
(рис.6.24).
Графічно
в координатах Р-V
робота газу дорівнює площі криволінійної
трапеції, яка обмежена графіком процесу,
віссю об’єму V
і лініями V1
= const,
V2
= const
(рис.6.24).
Знайдемо роботу газу в різних ізопроцесах:
Ізохорний. Так як V = const, dV = 0. Тому dAV =0 і АV = 0 (6.44)
Ізобарний. Р = const. Взявши до уваги рівняння (6.5) Клапейрона-Менделєєва, одержимо
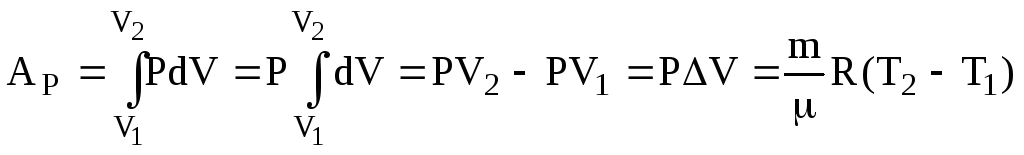 (6.45)
(6.45)
Ізотермічний. Т = const.
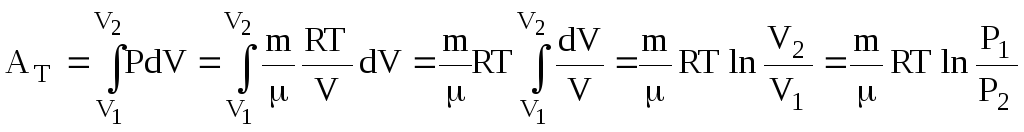 .
(6.46)
.
(6.46)
-
Молекулярно-кінетична теорія теплоємності газів
Питомою теплоємністю називається кількість теплоти, яка необхідна для нагрівання на 1 градус 1 кг речовини
![]() .
(6.47)
.
(6.47)
Молярною теплоємністю називається кількість теплоти, яка необхідна для нагрівання на 1 градус 1 моля речовини
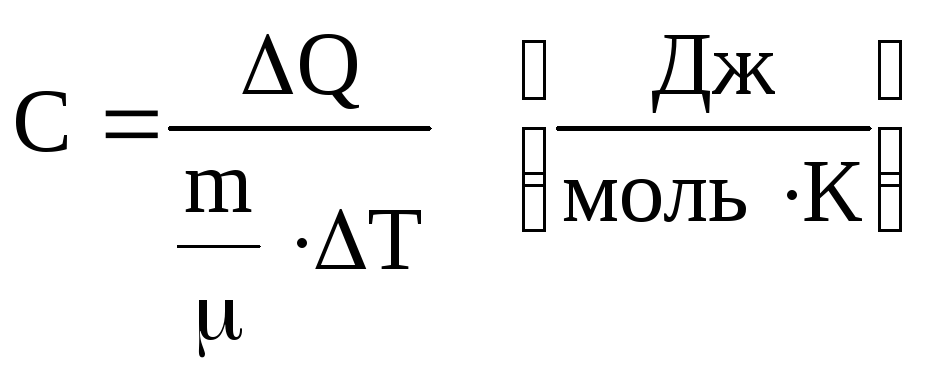 .
(6.48)
.
(6.48)
Ці
теплоємності зв’язані між собою
співвідношенням
![]() .
.
Розглянемо два режими нагрівання газу: ізохорний і ізобарний.
Ізохорний.
Враховуючи (6.38), (6.41) і (6.44) кількість
теплоти, необхідна для нагрівання
![]() молей газу на ∆Т
молей газу на ∆Т
![]() .
Підставляємо в (6.48). Одержуємо
.
Підставляємо в (6.48). Одержуємо
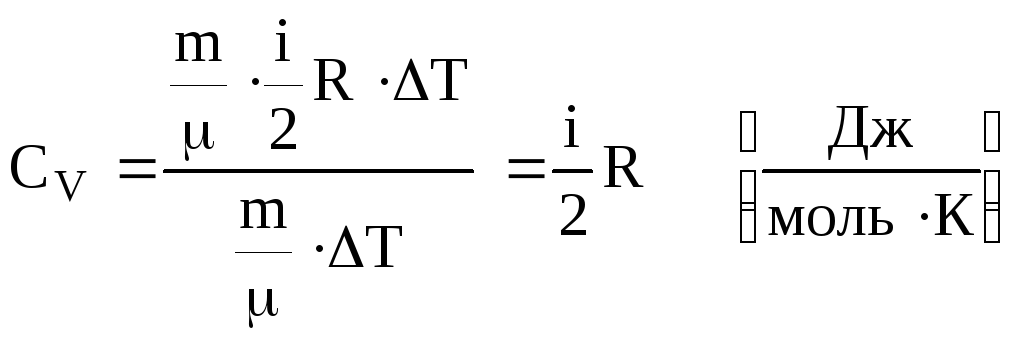 .
(6.49)
.
(6.49)
Ізобарний.
Враховуючи (6.38), (6.41) і (6.45) кількість
теплоти, необхідна для нагрівання
![]() молей газу на ∆Т
молей газу на ∆Т
![]()
. Підставляємо в (6.48). Одержуємо
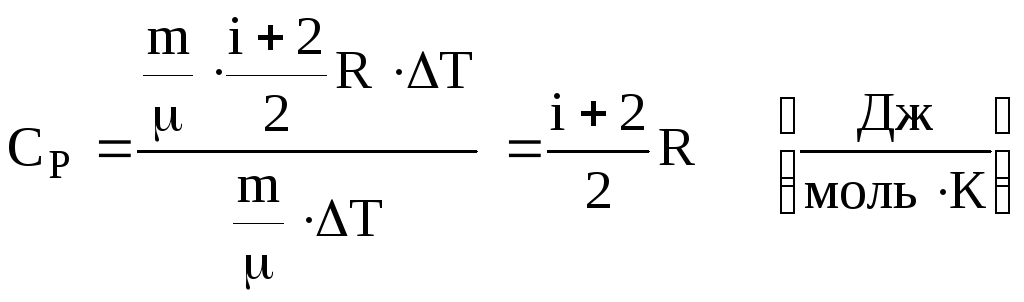 .
(6.50)
.
(6.50)
Бачимо,
що
![]() .
(6.51)
.
(6.51)
Це співвідношення Майєра. Теплоємність Ср > CV тому, що при ізобарному процесі підведене тепло іде не тільки на зміну внутрішньої енергії (як при ізохорному процесі), а і на виконання роботи. Ясно, що в цьому випадку потрібно підвести більше теплоти.
Характерним для кожного газу є відношення теплоємностей
![]()
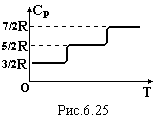 .
(6.52)
.
(6.52)
О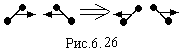
![]()
![]() держані
вирази для теплоємностей газу показують,
що вони не залежать від температури.
Але експеримент дає ступінчату залежність
(рис.6.25) для газів багатоатомних молекул.
Таку залежність неможливо пояснити в
рамках класичної фізики. Вона пояснюється
в рамках квантових уявлень, а саме
дискретним характером зміни фізичних
величин, в нашому випадку обертальної
та коливальної енергії молекул. При
низьких температурах теплової енергії
не вистачає для збудження обертального
руху молекул і коливального руху атомів
в них. Тобто, обертальні і коливальні
степені вільності не збуджуються. Вони
послідовно починають збуджуватись при
підвищенні температури. Наприклад,
двохатомні молекули при зіткненні, як
показано на рис.6.26, не приходять в
обертальний рух. В той час як по класичним
уявлення при такому зіткненні молекули
повинні прийти в обертання. Отже,
залежність (рис.6.25) зумовлена ступінчатою
зміною кількості степеней вільності
(числа і).
держані
вирази для теплоємностей газу показують,
що вони не залежать від температури.
Але експеримент дає ступінчату залежність
(рис.6.25) для газів багатоатомних молекул.
Таку залежність неможливо пояснити в
рамках класичної фізики. Вона пояснюється
в рамках квантових уявлень, а саме
дискретним характером зміни фізичних
величин, в нашому випадку обертальної
та коливальної енергії молекул. При
низьких температурах теплової енергії
не вистачає для збудження обертального
руху молекул і коливального руху атомів
в них. Тобто, обертальні і коливальні
степені вільності не збуджуються. Вони
послідовно починають збуджуватись при
підвищенні температури. Наприклад,
двохатомні молекули при зіткненні, як
показано на рис.6.26, не приходять в
обертальний рух. В той час як по класичним
уявлення при такому зіткненні молекули
повинні прийти в обертання. Отже,
залежність (рис.6.25) зумовлена ступінчатою
зміною кількості степеней вільності
(числа і).
-
Адіабатний процес
Адіабатним називається процес, який протікає без обміну теплотою з оточуючим середовищем, тобто в теплоізольованій системі.
Перше начало термодинаміки (6.38) набуває виду
![]() ,
(6.53)
,
(6.53)
тобто робота при в теплоізольованій системі може бути виконана за рахунок зменшення, що показує знак (-) мінус, внутрішньої енергії. Отже, робота газу при адіабатному процесі
![]() .
(6.54)
.
(6.54)