Материал: Chast1giper
Відношення
![]() , або
, або
![]() (6.15)
(6.15)
уже не залежить і від ширини інтервалу, а являється тільки функцією швидкості. Це і є функція розподілу молекул, в даному випадку по швидкостям. Вона показує ймовірність того, що значення швидкості потрапляє в інтервал від V до V+1, тобто в одиничний інтервал швидкостей. Тому її називають густиною ймовірності.
Функція
![]() (6.16)
(6.16)
Називається повною статистичною функцією розподілу. Вона дає можливість знайти кількість молекул, які мають значення швидкості в певному інтервалі від V1 до V2 шляхом інтегрування
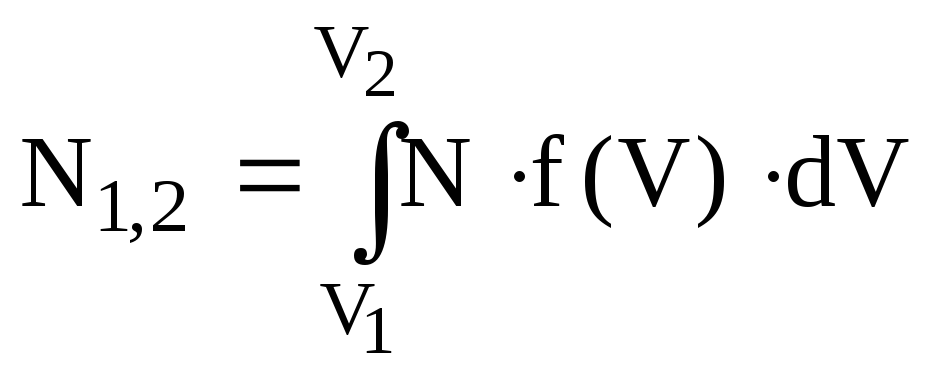 .
(6.17)
.
(6.17)
Ясно, що інтеграл (6.17) у всьому можливому діапазоні швидкостей дає загальну кількість молекул N, тобто
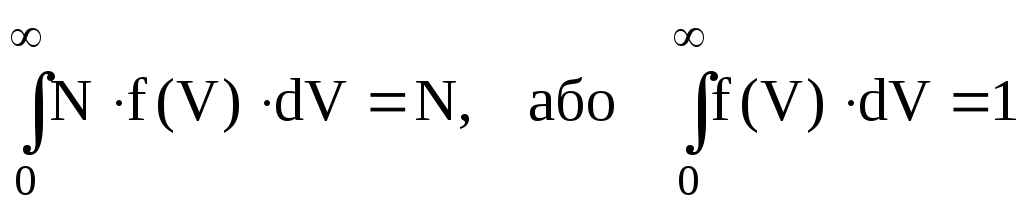 .
(6.18)
.
(6.18)
Це умова нормування функції розподілу. Останній вираз означає, що ймовірність виявити будь-яке значення швидкості, тобто в інтервалі від 0 до ∞, дорівнює 1.Це достовірна подія.
Максвеллівська функція розподілу молекул по швидкостям має вид (її вивід див.у кн. Р.В.Телеснин. Молекулярная физика)
![]() .
(6.19)
.
(6.19)
Тут: А – коефіцієнт, який знайдемо із умови (6.18) нормування функції розподілу, m – маса однієї молекули, k – стала Больцмана, Т – абсолютна температура.
Знайдемо нормуючий коефіцієнт А.
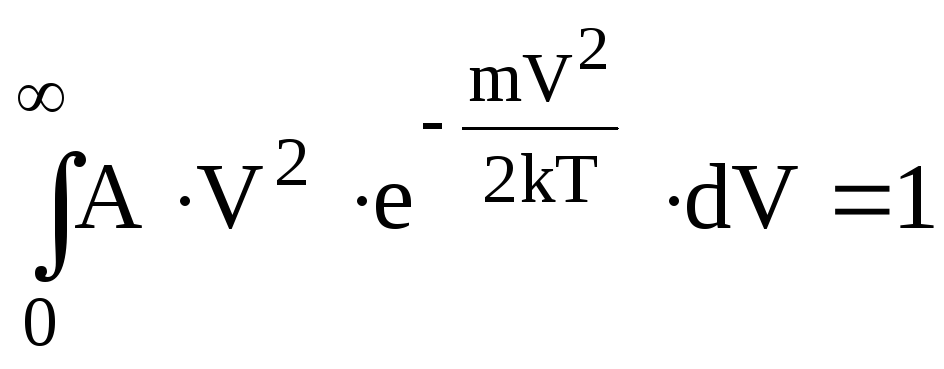 .
Виконаємо заміну аргументу інтегрування.
Позначимо
.
Виконаємо заміну аргументу інтегрування.
Позначимо
![]() Тоді
Тоді
![]() .
Одержимо
.
Одержимо
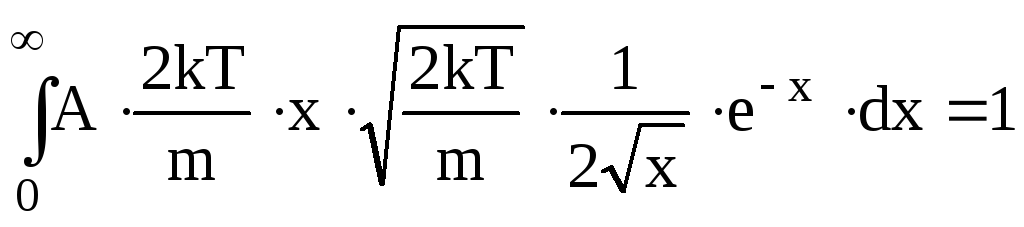
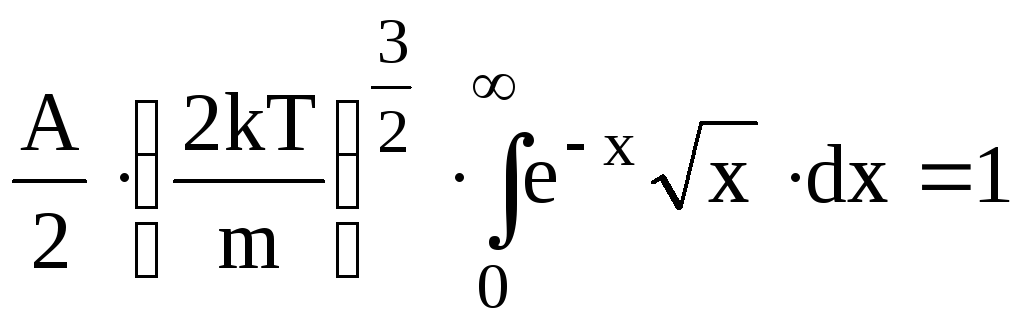 .
Табличний інтеграл
.
Табличний інтеграл
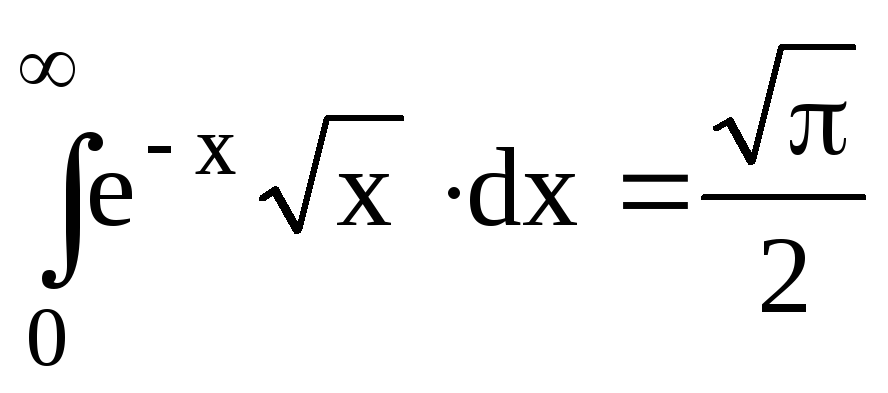 .
Таким чином маємо
.
Таким чином маємо
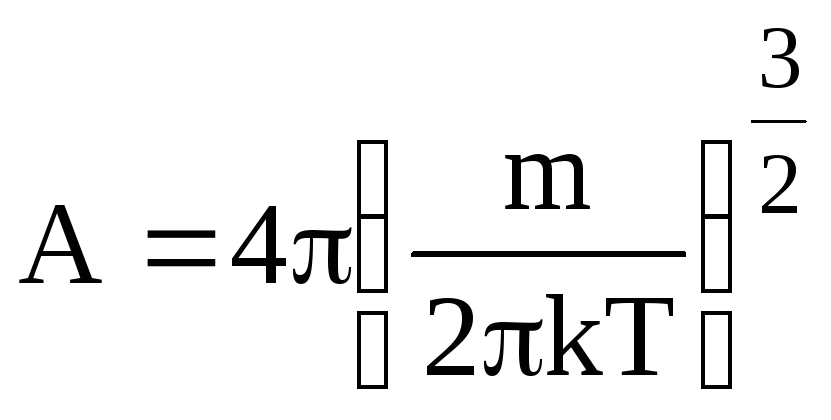 (6.20)
(6.20)
а нормована функція
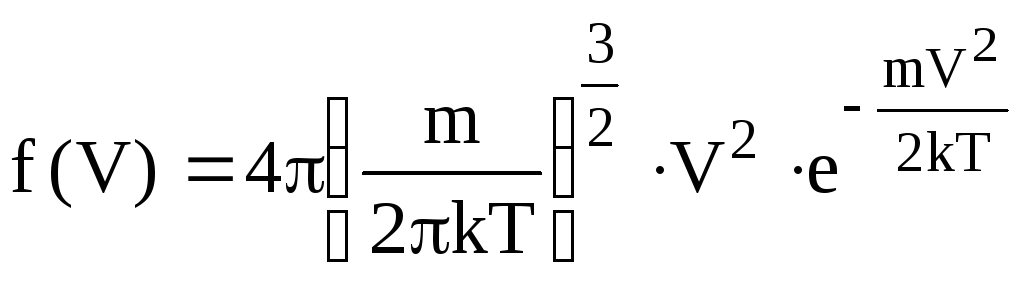
 .
(6.21)
.
(6.21)
6.7 Швидкості молекул. Правило статистичного усереднення
Хаотичний тепловий рух молекул характеризується трьома швидкостями: найбільш ймовірною, середньою арифметичною і середньою квадратичною.
Найбільш ймовірну швидкістьVн.й мають більшість молекул. Це значення аргументу, яке відповідає максимуму функції (6.19). Знайдемо її, дослідивши функцію Максвелла (6.19) на екстремум.
![]() .
.
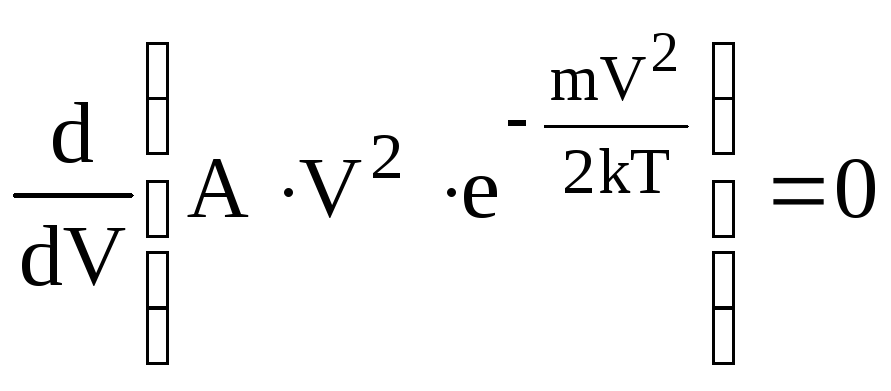 .
.
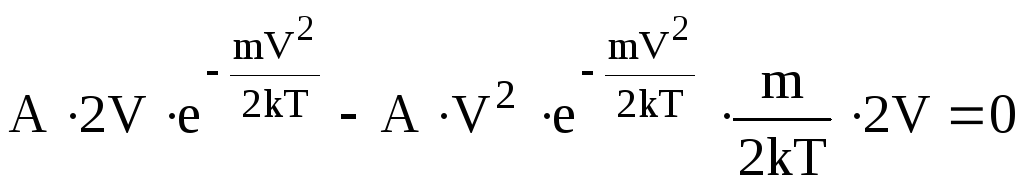 .
Після спрощень маємо
.
Після спрощень маємо ![]() .
(6.22)
.
(6.22)
Тут
враховано що
![]() .
.
Знайдемо середню арифметичну швидкість Vср. ар. з таких міркувань: швидкість V1 мають ∆N(V1) молекул;
швидкість V2 мають ∆N(V2) молекул;
------------------------------------------------
швидкість Vk мають ∆N(Vk) молекул.
Середня арифметична швидкість
 ,
,
або з врахуванням (6.16) одержуємо
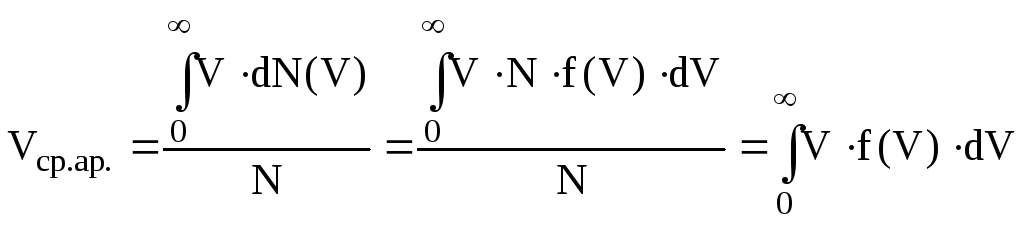 .
(6.23)
.
(6.23)
Одержане співвідношення називається правилом статистичного усереднення. Так знаходяться середні значення фізичних величин при відомій функції розподілу по цій фізичній величині. Наприклад, середня енергія може бути знайдена за виразом
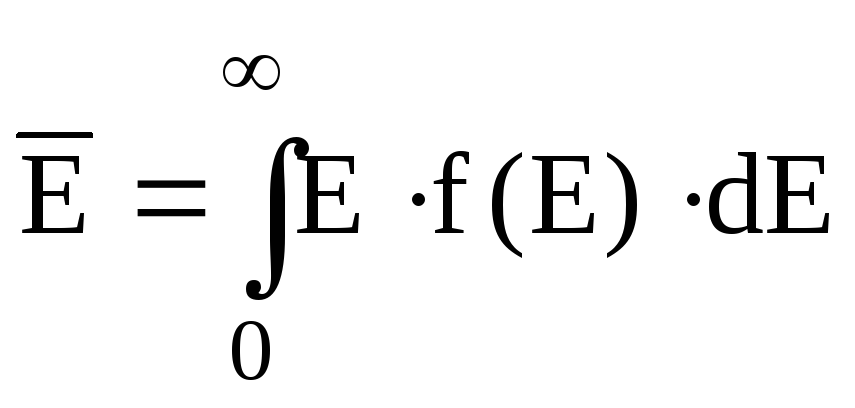 .
.
Розрахуємо середню арифметичну швидкість, скориставшись (6.23) і (6.21).
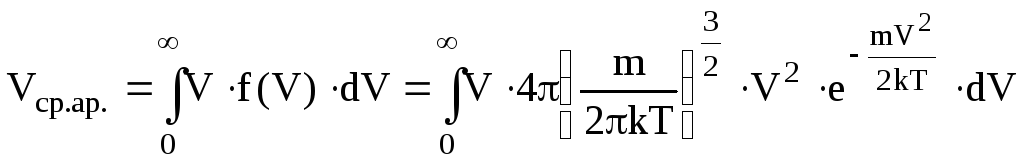 .
Виконаємо заміну аргументу інтегрування
таку ж, як і в розділі 6.6.
.
Виконаємо заміну аргументу інтегрування
таку ж, як і в розділі 6.6.
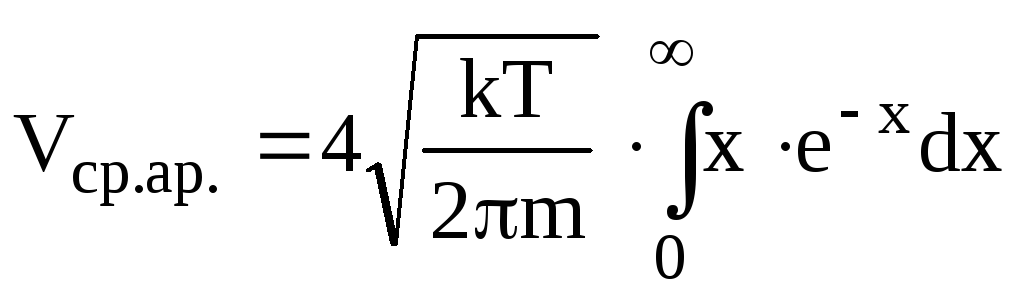 .
Інтегрування по частинам дає
.
Інтегрування по частинам дає
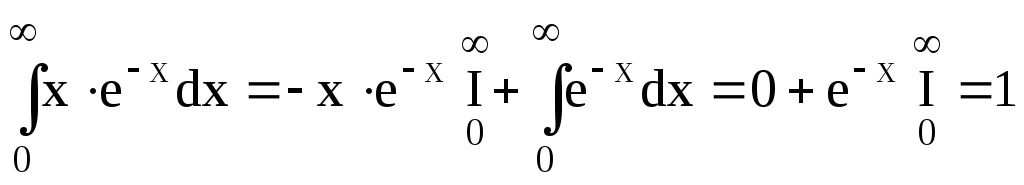 .
Одержуємо
.
Одержуємо
![]() .
(6.24)
.
(6.24)
Знайдемо середню квадратичну швидкість Vср.кв – це квадратний корінь із середнього значення квадратів швидкостей
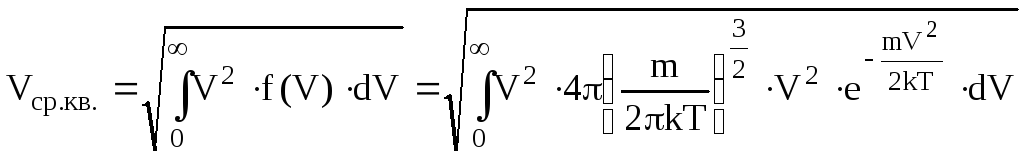 .
.
Аналогічно попередньому, інтегрування по частинам, дає
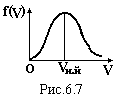
Г![]() рафік
цієї функції показаний на рис.6.7. Це
функція з екстремумом, який відповідає
значенню швидкості, яку мають більшість
молекул. Ця швидкість Vн.й
називається найбільш ймовірною швидкістю.
рафік
цієї функції показаний на рис.6.7. Це
функція з екстремумом, який відповідає
значенню швидкості, яку мають більшість
молекул. Ця швидкість Vн.й
називається найбільш ймовірною швидкістю.
![]() .
(6.25)
.
(6.25)
Можна середню квадратичну швидкість знайти простіше, знаючи середню енергію поступального руху молекул (6.13) і означення (6.11) середньої квадратичної швидкості.
 .
.
Видно
(6.22), (6.24) і (6.25), що всі характерні швидкості
відрізняються числовими коефіцієнтами
і із збільшенням температури зростають
пропорційно
![]() .
.
6.8 Експериментальна перевірка Максвеллівського розподілу молекул по швидкостям (дослід Штерна)
П![]() ерша
експериментальна перевірка Максвеллівського
розподілу молекул по швидкостям була
здійснена німецьким фізиком О.Штерном
(1888-1969) у 1920 р. Схема досліду показана на
рис 6.8. Вздовж осі двох к
ерша
експериментальна перевірка Максвеллівського
розподілу молекул по швидкостям була
здійснена німецьким фізиком О.Штерном
(1888-1969) у 1920 р. Схема досліду показана на
рис 6.8. Вздовж осі двох к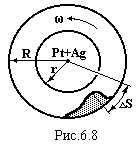 оаксіальних
циліндрів була натягнута платинова
нитка, покрита сріблом. Внутрішній
циліндр мав вузьку щілину. Вся система
була поміщена у вакуум. При нагріванні
нитка срібло випаровувалось. Щілиною
формувався пучок атомів срібла, які
осідали на внутрішній поверхні більшого
циліндра напроти щілини. Коли циліндри
приводились в обертання (~2700 об/хв),
срібна пляма зміщувалась і розмивалась
так як за час прольоту атомів між
циліндрами
оаксіальних
циліндрів була натягнута платинова
нитка, покрита сріблом. Внутрішній
циліндр мав вузьку щілину. Вся система
була поміщена у вакуум. При нагріванні
нитка срібло випаровувалось. Щілиною
формувався пучок атомів срібла, які
осідали на внутрішній поверхні більшого
циліндра напроти щілини. Коли циліндри
приводились в обертання (~2700 об/хв),
срібна пляма зміщувалась і розмивалась
так як за час прольоту атомів між
циліндрами
![]() вони
встигали повернутися на певний кут.
Зміщення
вони
встигали повернутися на певний кут.
Зміщення
![]() .
Тоді швидкість атомів
.
Тоді швидкість атомів
![]() .
По зміщенню максимуму плями знаходили
найбільш ймовірна швидкість (~600 м/с),
яка добре узгоджувалась з розрахованим
по (6.22) значенням. Вимірювання товщини
плівки срібла з різним зміщеннями дали
можливість впевнитись у справедливості
формули (6.19), так як молекули з різними
швидкостями зазнавали різного зміщення:
повільні молекули – більшого, швидкі
– меншого.
.
По зміщенню максимуму плями знаходили
найбільш ймовірна швидкість (~600 м/с),
яка добре узгоджувалась з розрахованим
по (6.22) значенням. Вимірювання товщини
плівки срібла з різним зміщеннями дали
можливість впевнитись у справедливості
формули (6.19), так як молекули з різними
швидкостями зазнавали різного зміщення:
повільні молекули – більшого, швидкі
– меншого.
6.9 Барометрична формула. Больцманівський розподіл молекул в силовому полі
Б![]() арометричною
формулою називається залежність тиску
Р атмосфери Землі в залежності від
висоти h
над її
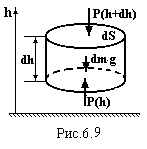
поверхнею. Знайдемо її. Для цього виділимо
нескінченно малий циліндр повітря
висотою dh
і площею основи dS
(рис.6.9). Позначимо тиск на нижню основу
Р(h),
арометричною
формулою називається залежність тиску
Р атмосфери Землі в залежності від
висоти h
над її
поверхнею. Знайдемо її. Для цього виділимо
нескінченно малий циліндр повітря
висотою dh
і площею основи dS
(рис.6.9). Позначимо тиск на нижню основу
Р(h),
на
верхню P(h+dh).
Маса повітря в цьому циліндрі dm
= ρ·g∙dh∙dS.
Густину знайдемо із (6.5) рівняння
Клапейрона-Менделєєва
![]() .
Запишемо умову рівноваги циліндра.
Горизонтальні сили тиску, які діють на
бічну поверхню взаємно компенсуються.
Залишаються вертикальні сили
.
Запишемо умову рівноваги циліндра.
Горизонтальні сили тиску, які діють на
бічну поверхню взаємно компенсуються.
Залишаються вертикальні сили
![]()
![]()
![]() .
Інтегруємо це рівняння з граничними
умовами:
.
Інтегруємо це рівняння з граничними
умовами:
при
h
= 0 P
= Po. ![]()
Одержали барометричну формулу
![]() ,
(6.26)
,
(6.26)
де m – маса однієї молекули, Еп – потенціальна енергія молекули в гравітаційному полі Землі. Формула (6.26) показує, що по мірі збільшення висоти тиск зменшується по експоненті.
Враховуючи
основне рівняння молекулярно-кінетичної
теорії (6.14)
![]() ,
формула (6.25) перейде в формулу
Больцманівського розподілу молекул по
потенціальним енергіям
,
формула (6.25) перейде в формулу
Больцманівського розподілу молекул по
потенціальним енергіям ![]() .
(6.27)
.
(6.27)
В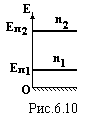
![]() ираз
(6.27) показує, що на більш високому
енергетичному рівні знаходиться менше
частинок (рис.6.10). При Еп2
> Еп1
n2
< n1.
Такий розподіл частинок називається
нормальним. Якщо ж на більш високому
енергетичному рівні знаходиться більше
частинок, тобто при Еп2
> Еп1
n2
> n1,
такий розподіл називається інверсною
заселеністю енергетичних рівнів. Це
термодинамічно нерівноважний стан
системи. Саме таке заповнення рівнів
необхідне для роботи лазерів.
ираз
(6.27) показує, що на більш високому
енергетичному рівні знаходиться менше
частинок (рис.6.10). При Еп2
> Еп1
n2
< n1.
Такий розподіл частинок називається
нормальним. Якщо ж на більш високому
енергетичному рівні знаходиться більше
частинок, тобто при Еп2
> Еп1
n2
> n1,
такий розподіл називається інверсною
заселеністю енергетичних рівнів. Це
термодинамічно нерівноважний стан
системи. Саме таке заповнення рівнів
необхідне для роботи лазерів.
Із виразу (6.27) випливає, що з пониженням температури концентрація молекул на висотах, відмінних від нуля зменшується, і при Т = 0К стає рівною нулю. Це означає, що при Т = 0К всі молекули знаходяться на поверхні Землі, тобто при h = 0. Отже силове поле намагається розмістити частинки в положення з мінімальною потенціальною енергією. Тепловий же рух навпаки намагається розподілити молекули рівномірно. Внаслідок цих протилежних факторів і встановлюється експоненціальний розподіл молекул з висотою.