Материал: Chast1giper
6. Молекулярна фізика і термодинаміка
6.1 Положення молекулярно-кінетичної теорії та її задача
Молекулярна фізика – це розділ, який вивчає фізичні властивості і агрегатні стани речовин в залежності від їх молекулярної будови і сил взаємодії між молекулами. Вона базується на трьох основних положеннях:
– всі тіла складаються з молекул і атомів;
– молекули і атоми хаотично рухаються;
– між молекулами і атомами існують сили взаємодії.
Молекулярно-кінетична теорія пояснює властивості тіл виходячи с характеру руху молекул і сил взаємодії між ними. Враховуючи, що кількість молекул дуже велика (в 1см3 газу при нормальних умовах міститься 2,69∙1019молекул), вивчення систем такої великої кількості частинок не можна звести до вивчення руху кожної молекули. В таких системах проявляються специфічні статистичні закономірності. Наприклад, швидкості молекул можуть бути самими різними і знати всі їх значення неможливо, та і безкорисно, тим більше, що вони весь час змінюються при зіткненнях. А ось середнє значення швидкості залишається сталим і характеризує стан системи.
Н
![]() априклад,
тиск газу зумовлений ударами молекул
об стінки посудини зазнає флуктуацій
з часом (рис.6.1), але його середнє значення
не змінюється і його можна виміряти
експериментально. Таким чином, задача
молекулярно-кінетичної теорії – це
знаходження середніх значень фізичних
величин, які характеризують системи
великої кількості частинок і які можна
виміряти експериментально. Для цього
використовується статистичні методи,
в основі яких лежить теорія ймовірності.
априклад,
тиск газу зумовлений ударами молекул
об стінки посудини зазнає флуктуацій
з часом (рис.6.1), але його середнє значення
не змінюється і його можна виміряти
експериментально. Таким чином, задача
молекулярно-кінетичної теорії – це
знаходження середніх значень фізичних
величин, які характеризують системи
великої кількості частинок і які можна
виміряти експериментально. Для цього
використовується статистичні методи,
в основі яких лежить теорія ймовірності.
Системи великої кількості частинок вивчає іще один розділ фізики – термодинаміка. Це вчення про зв’язок і взаємні перетворення енергії, теплоти і роботи. Термодинаміка наука феноменологічна (описова). Вона не дає пояснення тих чи інших явищ, властивостей на молекулярному рівні, а встановлює зв’язок між параметрами системи, наприклад, тиском, об’ємом, температурою, кількістю теплоти, роботою, ентропією, вільною енергією і т.д.
Обидва розділи доповнюють один одного.
6.2 Поняття ідеального газу та його закони
Ідеальний – це газ, в якому нехтують власним об’ємом молекул і силами взаємодії між ними.
Стан газу характеризується такими величинами: m – маса, P – тиск, V – об’єм, T – абсолютна температура. Закони ідеального газу встановлюють зв’язок між цими параметрами.
Ізотермічний закон (закон Бойля-Маріотта) m = const, T= const: при незмінній масі і температурі добуток тиску на об’єм залишається незмінним
![]() .
(6.1)
.
(6.1)
Г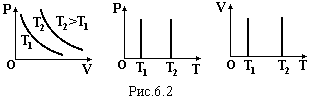 рафіки
цього закону зображені на рис.6.2 в різних
координатах.
рафіки
цього закону зображені на рис.6.2 в різних
координатах.
![]()
Ізобарний закон (закон Гей-Люсака) m = const, P = const: при незмінній масі і тискові об’єм газу прямо пропорційний температурі
![]() .
(6.2)
.
(6.2)
Тут
Vo
– об’єм газу при температурі 0оС,
![]() - температурний коефіцієнт об’ємного
розширення. Він показує відносну зміну
об’єму при зміні температури на 10.
Вимірюється в 1/град, і для всіх ідеальних
газів величина однакова і дорівнює
1/273 (1/град). Тому (6.2) набуває виду
- температурний коефіцієнт об’ємного
розширення. Він показує відносну зміну
об’єму при зміні температури на 10.
Вимірюється в 1/град, і для всіх ідеальних
газів величина однакова і дорівнює
1/273 (1/град). Тому (6.2) набуває виду
![]() ,
,
де Т=273+to – температура по абсолютній шкалі (шкала Кельвіна). Графіки цього закону зображені на рис.6.3.
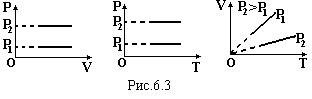
![]()
Ізохорний процес (закон Шарля) m = const, V = const: при незмінній масі і об’ємові тиск газу прямо пропорційний температурі
![]() .
(6.3)
.
(6.3)
Тут
Рo
– об’єм газу при температурі 0оС,
![]() - температурний коефіцієнт тиску. Він
показує відносну зміну тиску при зміні
температури на 10.
Вимірюється в 1/град, і для всіх ідеальних
газів величина однакова і дорівнює
1/273 (1/град). Тому (6.3) набуває виду
- температурний коефіцієнт тиску. Він
показує відносну зміну тиску при зміні
температури на 10.
Вимірюється в 1/град, і для всіх ідеальних
газів величина однакова і дорівнює
1/273 (1/град). Тому (6.3) набуває виду
![]() .
(6.4)
.
(6.4)
Графіки цього закону зображені на рис.6.4.
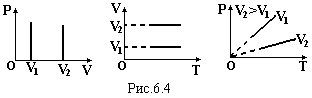
![]()
Зв’язок між усіма чотирма параметрами дає рівняння стану ідеального газу – рівняння Клапейрона-Менделєєва:
![]() .
(6.5)
.
(6.5)
Тут μ – молярна маса газу, R = 8,31 Дж/(моль∙К) – газова стала.
6.3 Закон Дальтона. Рівняння стану для суміші газів
Англійський фізик Дж. Дальтон (1766-1844) 1801-1803 р. експериментально встановив закон, який носить його ім’я (закон Дальтона): загальний тиск суміші хімічно не взаємодіючих газів дорівнює сумі парціальних тисків. Парціальний тиск – це тиск кожного газу, який встановлюється, коли в посудині знаходиться тільки цей газ, а інші відкачані.
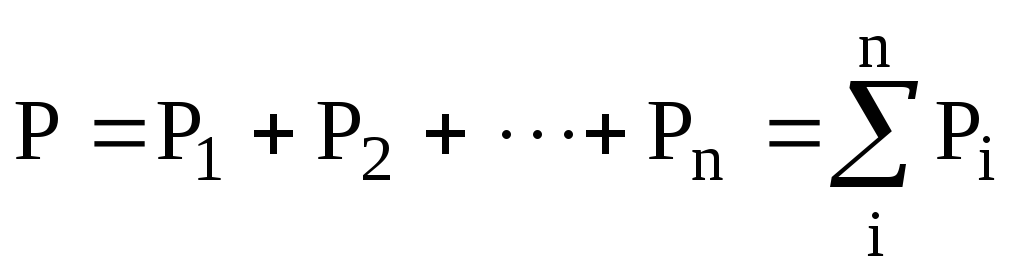 .
(6.6)
.
(6.6)
Одержимо рівняння стану для суміші газів. Запишемо із рівняння Клапейрона-Менделєєва (6.5) парціальні тиски:
![]() ,
,
![]() ,...,
,...,
![]() .
.
Загальний тиск знайдемо по закону (6.6) Дальтона
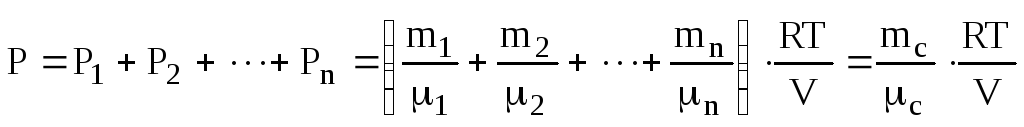 ,
(6.7)
,
(6.7)
де
молярна маса суміші газів
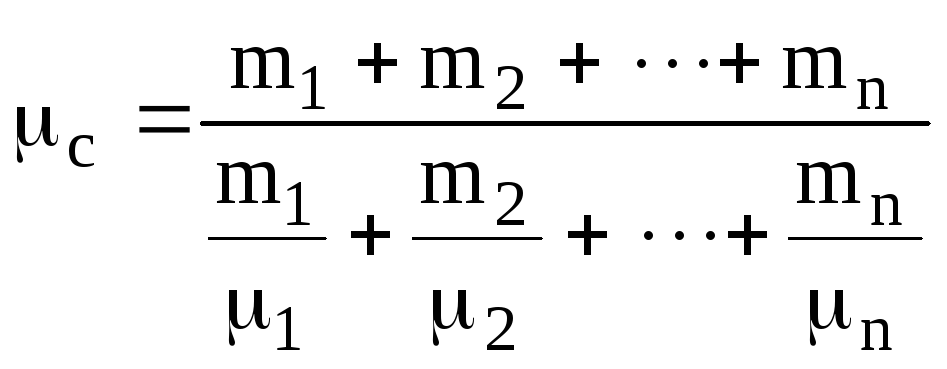 (6.8)
(6.8)
Таким чином рівняння стану для суміші має такий же вид, як і (6.5) для одного газу, якщо замінити масу і молярну масу значеннями для суміші
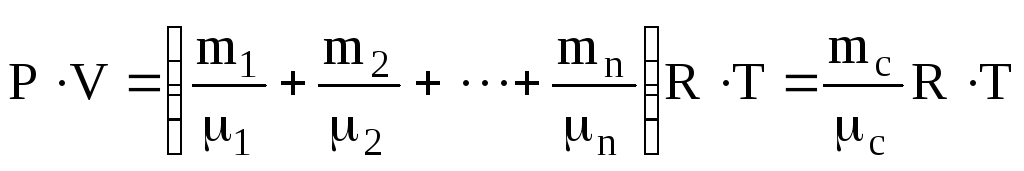 .
(6.9)
.
(6.9)
6.4 Основне рівняння молекулярно-кінетичної теорії
Основним рівнянням молекулярно-кінетичної теорії називається рівняння, яке дає зв’язок між тиском газу і енергією поступального руху молекул. Знайдемо це рівняння в таких припущеннях:
а) всі молекули рухаються з однаковими швидкостями;
б) так як рух молекул хаотичний, то всі напрямки руху рівно ймовірні, тобто можна вважати, що вздовж будь-якого напрям рухється однакова кількість молекул. Тому припустимо, що молекули рухаються тільки вздовж координатних осей х, y, z. Тоді можна вважати, що вздовж кожної осі рухається 1/3 частина всіх молекул.
Тиск газу пояснюється зміною імпульсу молекул при зіткненні і відбиванні їх із стінкою посудини. У відповідності з другим законом Ньютона на молекулу з боку стінки діє сила, а згідно з третім законом Ньютона, на стінку з боку молекули буде діяти така ж за величиною сила. Відношення сили до площі і є тиск.
В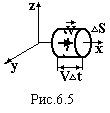
![]() иберемо
на поверхні посудини малу плоску площадку
∆S.
Вісь ох направимо перпендикулярно до
цієї площадки, осі оy
і oz
паралельні їй (рис.6.5). Знайдемо кількість
молекул ∆N,
які за час ∆t
зіткнуться з цією площадкою. Це будуть
молекули, які рухаються до площадки, а
це половина тих молекул, які рухаються
вздовж осі ох, і віддалені від неї на
відстань, не більшу ніж V∙∆t.
иберемо
на поверхні посудини малу плоску площадку
∆S.
Вісь ох направимо перпендикулярно до
цієї площадки, осі оy
і oz
паралельні їй (рис.6.5). Знайдемо кількість
молекул ∆N,
які за час ∆t
зіткнуться з цією площадкою. Це будуть
молекули, які рухаються до площадки, а
це половина тих молекул, які рухаються
вздовж осі ох, і віддалені від неї на
відстань, не більшу ніж V∙∆t.
![]() .
При пружному ударі імпульс молекули
змінюється на 2mV.
Якщо удар не пружний, тобто молекула
прилипає до поверхні, то імпульс зміниться
на mV.
Але після встановлення динамічної
рівноваги, кількість молекул, які
прилипають до стінки і які її покидають
стають однаковими. Молекула, покидаючи
стінку, передає їй імпульс mV.
Таким чином і в цьому випадку загальна
зміна імпульсу теж буде дорівнювати
2mV,
тобто немає різниці, та ж молекула
покинула стінку, чи інша. Запишемо другий
закон Ньютона і знайдемо тиск
.
При пружному ударі імпульс молекули
змінюється на 2mV.
Якщо удар не пружний, тобто молекула
прилипає до поверхні, то імпульс зміниться
на mV.
Але після встановлення динамічної
рівноваги, кількість молекул, які
прилипають до стінки і які її покидають
стають однаковими. Молекула, покидаючи
стінку, передає їй імпульс mV.
Таким чином і в цьому випадку загальна
зміна імпульсу теж буде дорівнювати
2mV,
тобто немає різниці, та ж молекула
покинула стінку, чи інша. Запишемо другий
закон Ньютона і знайдемо тиск
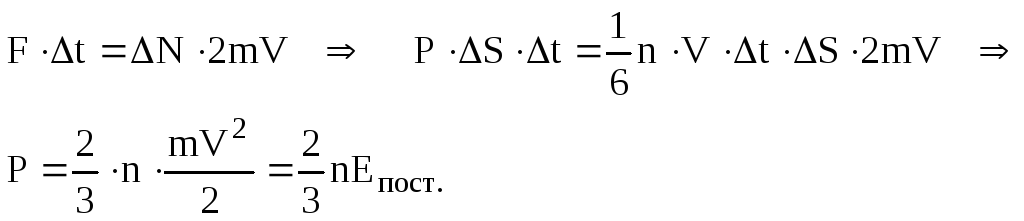 (6.10 Реально
швидкості молекул різні. Розбивши всі
молекули на групи з однаковими швидкостями,
парціальний тиск кожної групи молекул
знаходиться по формулі (6.10). Скориставшись
законом Дальтона, знайдемо загальний
тиск
(6.10 Реально
швидкості молекул різні. Розбивши всі
молекули на групи з однаковими швидкостями,
парціальний тиск кожної групи молекул
знаходиться по формулі (6.10). Скориставшись
законом Дальтона, знайдемо загальний
тиск
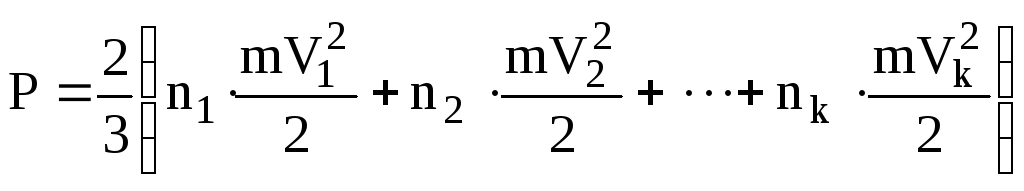 .
У дужках записана загальна енергія
поступального руху всіх молекул. Її
можна знайти ще як добуток концентрації
молекул n
на середню енергію поступального руху
.
У дужках записана загальна енергія
поступального руху всіх молекул. Її
можна знайти ще як добуток концентрації
молекул n
на середню енергію поступального руху
![]() ,
де середня
квадратична
швидкість – це корінь квадратний із
середнього значення квадратів швидкостей
усіх N
молекул (риска зверху означає середнє
значення)
,
де середня
квадратична
швидкість – це корінь квадратний із
середнього значення квадратів швидкостей
усіх N
молекул (риска зверху означає середнє
значення)
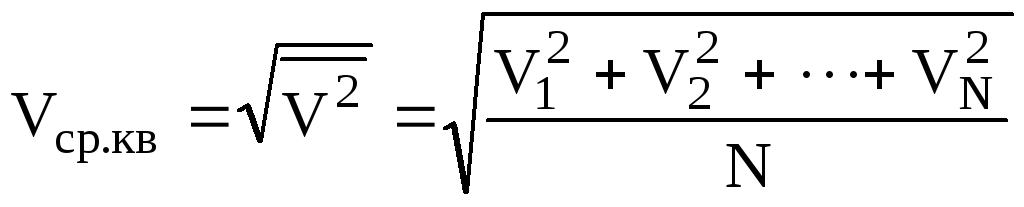 .
(6.11)
.
(6.11)
Таким чином, основне рівняння молекулярно-кінетичної теорії має вид
![]() .
(6.12)
.
(6.12)
6.5 Середня енергія поступального руху молекул. Молекулярно-кінетичне тлумачення температури
Підставимо тиск (6.12) в рівняння (6.5) Клапейрона-Менделєєва
![]() .
Знаходимо середню енергію поступального
руху
.
Знаходимо середню енергію поступального
руху
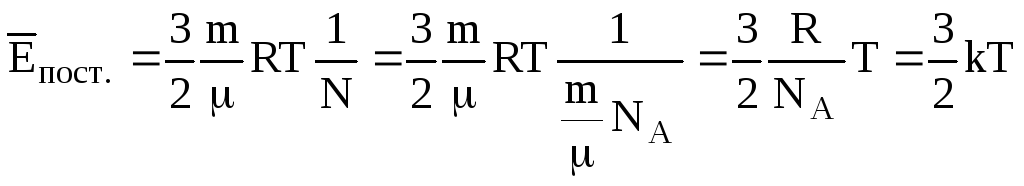 .
(6.13)
.
(6.13)
Тут:
NA
= 6,02∙1023
1/моль –число Авогадро,
![]() –
стала Больцмана.
–
стала Больцмана.
Вираз (6.13) показує, що середня енергія поступального руху молекул залежить тільки від абсолютної температури і не залежить від типу молекул. Тому абсолютну температуру трактують як міру кінетичної енергії теплового руху молекул. Так як кінетична енергія не може бути від’ємною, то і абсолютна температура Т завжди позитивна.
Підстановка (6.13) в (6.12) дає такий вираз основного рівняння молекулярно-кінетичної теорії:
![]() .
(6.14)
.
(6.14)
Видно,
що тиск газу не залежить від маси (типу)
молекул, а визначається тільки їх
концентрацією і температурою. Тому
очевидним стає закон Дальтона
![]() .
.
6.6 Поняття про функцію розподілу. Функція розподілу Максвела
Для вирішення задачі молекулярно-кінетичної теорії, знаходження середніх значень фізичних величин, введемо поняття функції розподілу.
Будемо
цікавитись, наприклад, швидкостями
теплового руху молекул. Ясно, що вони
за величиною будуть самими різними -
від нуля до нескінченності. Але кількість
молекул з дуже малими і дуже великими
швидкостями буде невеликою. Дійсно,
ймовірність того, що якась молекула при
зіткненні з другими молекулами буде
або тільки віддавати частину свого
імпульсу (зменшувати швидкість), або
тільки одержувати (збільшувати швидкість),
при хаотичному русі мала. Деяке значення
швидкості буде зустрічатись найчастіше,
тобто її мають більшість молекул. Уявимо,
що в певний момент часу ми змогли виміряти
значення швидкостей усіх молекул.
Відмітимо ці значення на ч![]() исловій
осі швидкостей (рис.6.6). В якомусь діапазоні
густина точок буде максимальною і
зменшуватись як при малих, так і при
великих
з
исловій
осі швидкостей (рис.6.6). В якомусь діапазоні
густина точок буде максимальною і
зменшуватись як при малих, так і при
великих
з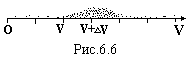 наченнях
швидкості. Маємо н
наченнях
швидкості. Маємо н![]() ерівномірний
розподіл кількості точок по числовій
осі. Очевидно, що при незмінній температурі
цей розподіл не буде змінюватись з
часом, так як при пружних зіткненнях
швидкість однієї молекули може
збільшитись, а іншої зменшитись. А це
буде означати перестановку відмічених
нами точок місцями. Характер же розподілу
не зміниться.
ерівномірний
розподіл кількості точок по числовій
осі. Очевидно, що при незмінній температурі
цей розподіл не буде змінюватись з
часом, так як при пружних зіткненнях
швидкість однієї молекули може
збільшитись, а іншої зменшитись. А це
буде означати перестановку відмічених
нами точок місцями. Характер же розподілу
не зміниться.
Розіб’ємо
числову вісь на однакові довільні
інтервали швидкості ∆V
і підрахуємо кількість точок ∆N,
які потрапили в кожний інтервал. Очевидно,
що ∆N
залежить від ширини інтервалу ∆V,
його положення на числовій осі, тобто
від V
і загальної кількості молекул N,
тобто
![]() .
Для того, щоб виключити залежність від
суб’єктивно вибраних параметрів ∆V
і N,
поділимо ∆N
на N
і ∆V.
Відношення
.
Для того, щоб виключити залежність від
суб’єктивно вибраних параметрів ∆V
і N,
поділимо ∆N
на N
і ∆V.
Відношення
![]() дає долю молекул, або ймовірність того,
що значення швидкості потрапляє в
інтервал від V
до V+∆V,
і не залежить від загальної кількості
молекул N.
дає долю молекул, або ймовірність того,
що значення швидкості потрапляє в
інтервал від V
до V+∆V,
і не залежить від загальної кількості
молекул N.