Материал: Chast1giper
Знайдемо зв’язок між тиском Р, об’ємом V і температурою Т при адіабатному процесі. Для нескінченно малих змін
![]() .
.
Одержуємо
диференційне рівняння
![]() .
Інтегруємо його
.
Інтегруємо його
![]() .
Одержуємо
.
Одержуємо
![]()
![]() .
.
Із
(6.52) виразимо і через γ
![]() .
.
Отже,
![]() .
(6.55)
.
(6.55)
Одержали рівняння адіабатичного процесу, яке зв’язує температуру і об’єм. Можна знайти зв’язок між тиском і об’ємом, а також між температурою і тиском, послідовно виключаючи відповідний параметр із рівняння Клапейрона-Менделеєва (6.5). Одержуємо
![]() ,
(6.56)
,
(6.56)
![]() .
(6.57)
.
(6.57)
Графік адіабатного процесу в координатах P-V має вид гіперболи більш крутої (рис.6.27), ніж ізотерма (див. рис.6.2). Дійсно,
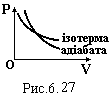
![]()
![]() .
Так як γ >
1,
.
Так як γ >
1,
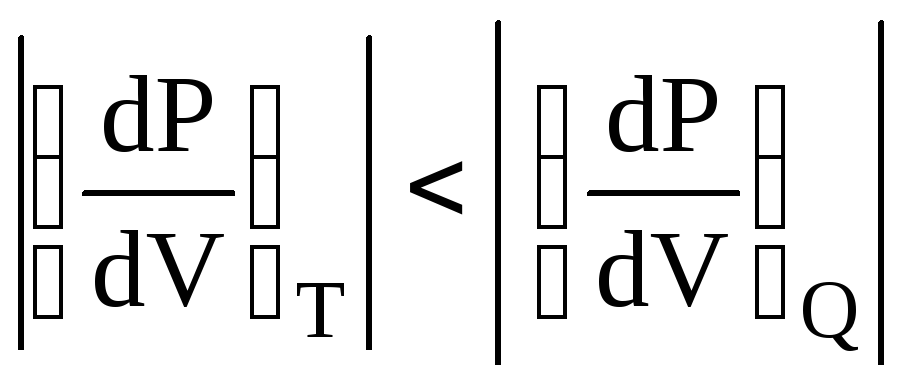 ,
тобто адіабата іде крутіше ізотерми.
,
тобто адіабата іде крутіше ізотерми.
-
Оборотні і необоротні процеси. Цикли
Процес - це перехід системи із одного стану в інший. Є рівноважні і нерівноважні, оборотні і необоротні процеси.
П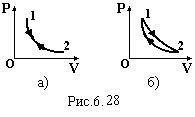 ри
рівноважному
процесі зміни параметрів системи (тиску,
температури і т.ін.) встигають за змінами
зовнішніх умов. Це означає, що в момент
припинення зміни зовнішніх умов зміна
параметрів системи теж відразу
припиняється. Це нескінченно повільні
процеси.
ри
рівноважному
процесі зміни параметрів системи (тиску,
температури і т.ін.) встигають за змінами
зовнішніх умов. Це означає, що в момент
припинення зміни зовнішніх умов зміна
параметрів системи теж відразу
припиняється. Це нескінченно повільні
процеси.
П![]() ри
нерівноважному
процесі після стабілізації зовнішніх
умов параметри системи ще деякий час
продовжують змінюватись. Це швидко
текучі процеси. Наприклад, при швидкому
стискуванні газу поршнем поблизу нього
температура газу вища ( молекули
відбиваються від нього з більшою
швидкістю на подвоєну швидкість поршня,
ніж падають (див. наслідок у розділі
4.8), ніж в об’ємі. Тому після зупинки
поршня температура продовжує змінюватись
(вирівнюватись).
ри
нерівноважному
процесі після стабілізації зовнішніх
умов параметри системи ще деякий час
продовжують змінюватись. Це швидко
текучі процеси. Наприклад, при швидкому
стискуванні газу поршнем поблизу нього
температура газу вища ( молекули
відбиваються від нього з більшою
швидкістю на подвоєну швидкість поршня,
ніж падають (див. наслідок у розділі
4.8), ніж в об’ємі. Тому після зупинки
поршня температура продовжує змінюватись
(вирівнюватись).
Оборотній – це такий процес, який можна провести в зворотному напрямку через ту ж саму сукупність станів системи, що і в прямому (рис.6.28,а). Якщо ж цього здійснити неможливо, процес називається необоротнім (рис.6.28,б). Наприклад, при швидкому стискуванні газу , коли його температура поблизу поршня більша, ніж в об’ємі, зворотній процес розширення газу, із температурою поблизу поршня вищою, ніж в об’ємі, неможливий. Дійсно, в цьому випадку молекула буде мати швидкість відбивання меншу на подвоєну швидкість поршня (див. наслідок у розділі 4.8), ніж швидкість падіння на нього. А це означає меншу температуру газу поблизу поршня, ніж в об’ємі. А це вже інший шлях зворотного процесу ніж прямого.
Цикл – це замкнутий процес, тобто коли система після ряду змін повертається в свій початковий стан. Якщо всі процеси циклу оборотні, цикл теж оборотній. Якщо ж хоч один процес циклу необоротній, цикл теж необоротній.
Робота газу цикл чисельно дорівнює площі, обмеженій циклом в координатах Р-V.
-
Принцип дії теплової і холодильної машин та їх коефіцієнт корисної дії (ккд). Холодильний коефіцієнт. Друге начало термодинаміки
Теплова машина уявляє собою пристрій, який багатократно здійснює деякий цикл, результатом якого є перетворення теплової енергії в механічну роботу. Причому ця робота повинна бути позитивною. Тоді її можна використати і машина буде корисною.
В![]() сяка
теплова машина складається із трьох
невід’ємних частин (рис.6.29): 1) нагрівника
з температурою Т1,
як джерела теплової енергії; 2) робочого
тіла, як носія енергії і посередника
між тепловою і механічною енергіями;
3) холодильника.
сяка
теплова машина складається із трьох
невід’ємних частин (рис.6.29): 1) нагрівника
з температурою Т1,
як джерела теплової енергії; 2) робочого
тіла, як носія енергії і посередника
між тепловою і механічною енергіями;
3) холодильника.
Необхідність перших двох частин не викликає сумніву, а третьої, холодильника, потребує обгрунтування. Доведемо необхідність холодильника, тобто необхідність викидання певної кількості теплоти в холодильник, як правило оточуюче середовище. При розширенні газу він виконує певну позитивну роботу. Щоб машина працювала відносно довго, робоче тіло необхідно повернути в початковий стан, затративши на це меншу роботу. Тільки тоді А>0 і машина буде корисною. Отже зворотний процес стискування робочого тіла повинен пройти нижче, ніж прямий (рис.6.28,б), а значить при нижчій, ніж прямий, температурі (див. рис.6.2). При стискуванні газ нагрівається. Щоб знизити його температуру, необхідно відбирати частину тепла і викидати в холодильник.
Таким чином, ми впевнились, що неможлива теплова машина, яка б повністю перетворювала всю теплоту в роботу. Така машина називається вічним двигуном другого роду і він нгеможливий. В цьому полягає суть другого начала термодинаміки.
Слід зауважити, що процес, при якому все тепло перетворюється в роботу є – це ізотермічний процес. Але ж для роботи теплової машини необхідно проводити замкнутий процес, тобто цикл.
Знайдемо вираз для ККД ( η ) теплової машини. На основі закону збереження енергії робота
![]() ,
(6.58) а затрачена енергія
дорівнює Q1.
За означенням ККД – це відношення
корисної роботи до затраченої енергії
,
(6.58) а затрачена енергія
дорівнює Q1.
За означенням ККД – це відношення
корисної роботи до затраченої енергії
![]() .
(6.59)
.
(6.59)
З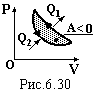 вернемо
увагу, що ККД завжди менший одиниці.
вернемо
увагу, що ККД завжди менший одиниці.
![]() Холодильна
машина, це пристрій, призначенням якого
є відбирання тепла від холодного тіла
і передача його більш гарячому, тобто
охолодження холоднішого тіла. Ця машина
працює по оберненому циклу теплової
машини (рис.6.30). Корисним результатом
роботи холодильної машини є відібране
тепло Q2,
на що витрачається робота
Холодильна
машина, це пристрій, призначенням якого
є відбирання тепла від холодного тіла
і передача його більш гарячому, тобто
охолодження холоднішого тіла. Ця машина
працює по оберненому циклу теплової
машини (рис.6.30). Корисним результатом
роботи холодильної машини є відібране
тепло Q2,
на що витрачається робота
![]() .
Ефективність роботи холодильної машини
характеризує відношення забраної
кількості теплоти Q2
до
роботи А, тобто холодильний коефіцієнт
.
Ефективність роботи холодильної машини
характеризує відношення забраної
кількості теплоти Q2
до
роботи А, тобто холодильний коефіцієнт
![]() .
(6.60)
.
(6.60)
Звернемо
увагу, що холодильний коефіцієнт![]() ,
Він може приймати будь-яке значення, як
менше так і більше одиниці. Чим більший
холодильний коефіцієнт, тим ефективніша
холодильна машина. Але ККД циклу
холодильної машини знаходиться за
виразом (6.59), як і теплової машини.
,
Він може приймати будь-яке значення, як
менше так і більше одиниці. Чим більший
холодильний коефіцієнт, тим ефективніша
холодильна машина. Але ККД циклу
холодильної машини знаходиться за
виразом (6.59), як і теплової машини.
-
Ідеальна теплова машина Карно та її ккд
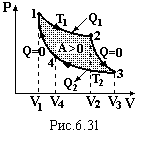
У 1824 році французький інженер С.Карно (1796-1832) запропонував цикл теплової машини, який складається із двох ізотерм 1→2, 3→4, та двох адіабат 2→3, 4→1 (рис.6.31). Для знаходження ККД запишемо перше начало термодинаміки для усіх чотирьох процесів:
![]()
 ;
;
![]() ;
;
![]()
![]() ;
;
![]() .
.
Склавши всі рівняння, знайдемо роботу за цикл та його ККД
![]() .
.
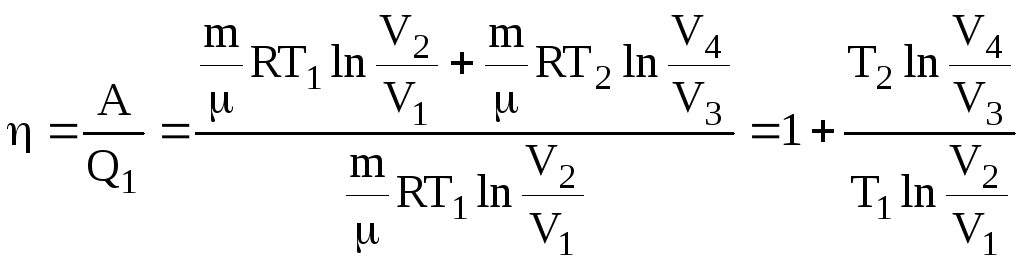 .
(6.61)
.
(6.61)
Запишемо рівняння адіабат (див.6.55)
![]()
![]() .
.
Поділимо ці рівняння одне на друге і спростимо. Одержуємо
![]() .
Отже,
.
Отже,
![]() .
.
Тоді формула (6.61) для ККД ідеальної машини Карно набуде виду
![]() .
(6.62)
.
(6.62)
-
Поняття про ентропію. Властивості ентропії
Вище
були одержані вирази для ККД реальної
(6.59) і ідеальної (6.62) теплової машини.
Ясно, що ККД реальної машини не більший,
ніж ідеальної, тобто маємо нерівність
![]() .
(6.63)
.
(6.63)
Відношення кількості теплоти Q до абсолютної температури Т джерела тепла називається приведеною кількістю теплоти. Враховуючи, що тепло Q2 віддається, тобто Q2 < 0, в лівій частині нерівності (6.63) стоїть алгебраїчна сума приведених кількостей теплот циклу, яка, як видно із (6.63), не боже бути позитивною. Вираз (6.63) можна переписати в інтегральній формі
![]() .
(6.64)
.
(6.64)
Ц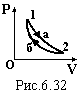 е
співвідношення називається нерівністю
Клаузіуса і являється математичним
записом другого начала термодинаміки.
е
співвідношення називається нерівністю
Клаузіуса і являється математичним
записом другого начала термодинаміки.
Р![]() озглянемо
деякий оборотний цикл (рис.6.32), який
складається із двох процесів: 1а2 і 2б1.
Для оборотного циклу у виразі (6.64) буде
знак рівності. Одержимо
озглянемо
деякий оборотний цикл (рис.6.32), який
складається із двох процесів: 1а2 і 2б1.
Для оборотного циклу у виразі (6.64) буде
знак рівності. Одержимо
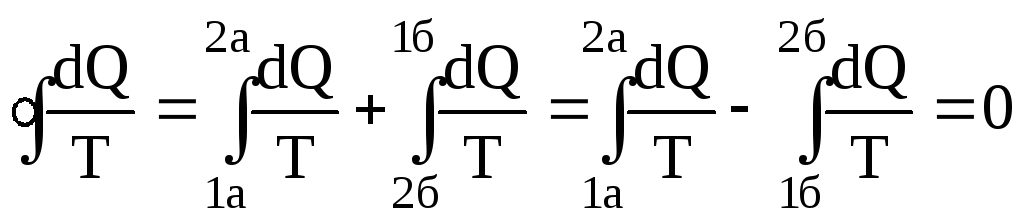 .
(6.65)
.
(6.65)
Тут
враховано оборотність процесу 2б1, тобто
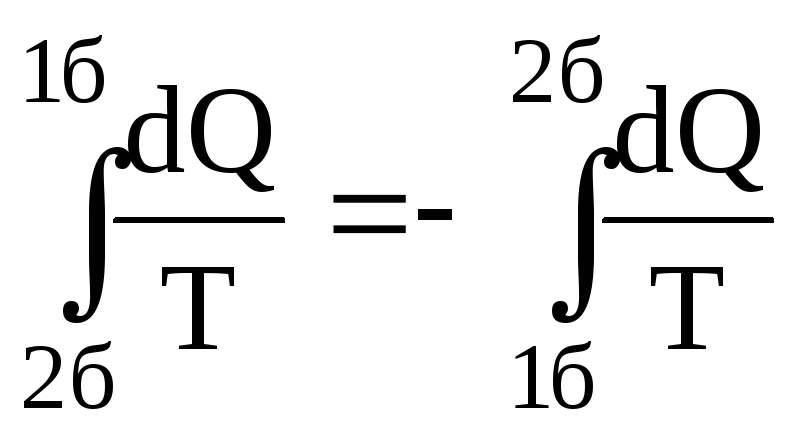 .
.
Рівняння (6.65) показує, що приведена кількість теплоти, одержана системою, не залежить від шляху переходу, а визначається тільки параметрами початкового (1) і кінцевого (2) станів. Цей факт дає можливість ввести певну функцію стану системи, ентропію S, зміна якої
дорівнює алгебраїчній сумі приведених кількостей теплот, тобто
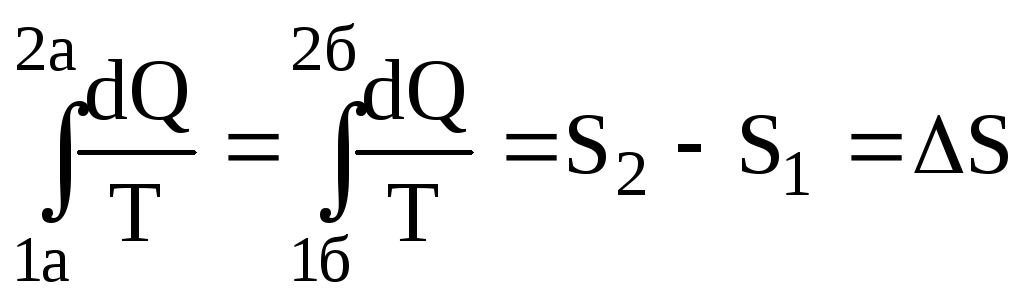 .
(6.66)
.
(6.66)
Якщо в циклі є необоротний процес 1н2 (рис.6.33), то
![]() .
.
Т![]() ак
як для оборотного процесу (2б1)
ак
як для оборотного процесу (2б1)
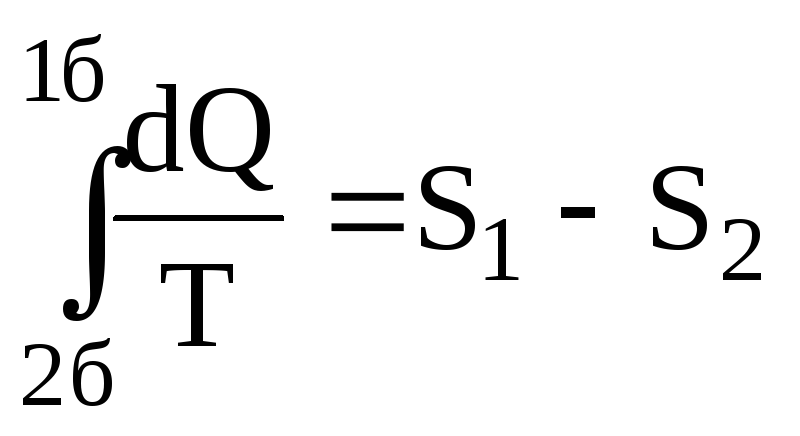 ,
одержуємо
,
одержуємо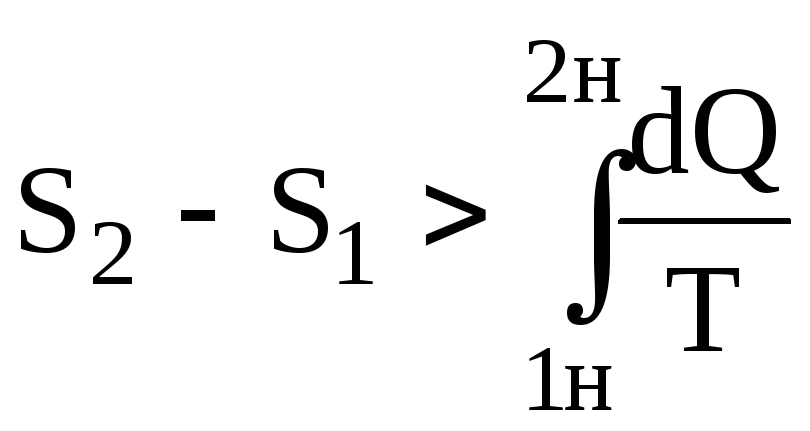 ,
або в загальному випадку
,
або в загальному випадку
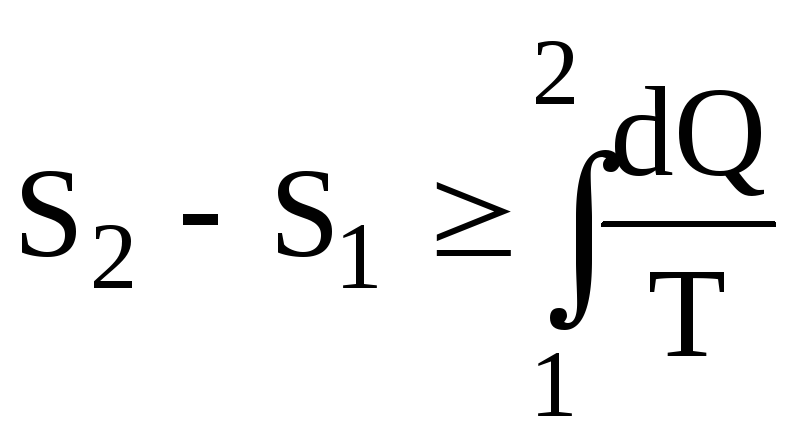 (6.67)
(6.67)
Знак (=) для оборотного знак (>) для необоротного процесу. Для нескінченно малих величин маємо для зміни ентропії
![]() .
(6.68)
.
(6.68)
Які ж властивості ентропії та який її фізичний зміст?
– Ентропія функція стану системи;
– Ентропія величина адитивна. Це означає, що зміна ентропії системи дорівнює алгебраїчній сумі змін ентропії частин системи. Або загальна зміна ентропії в якомусь складному процесі дорівнює алгебраїчній сумі змін ентропії в простих процесах, із яких складається даний процес.
– Для теплоізольованої системи, тобто при адіабатних процесах, коли dQ = 0, із (6.68) випливає, що dS ≥ 0. Ентропія ізольованих систем не може зменшуватись, тобто процеси в таких системах ідуть тільки в напрямку збільшення ентропії. Це дає можливість теоретично прогнозувати протікання різних процесів. Якщо ентропія кінцевого стану більша, ніж початкового, процес може іти без зовнішнього втручання, наприклад, перехід тепла від гарячих до холодних частин системи. Не слід вважати, що ентропія взагалі не може зменшитись. Може, але для цього необхідно виконати певну роботу, тобто система вже буде незамкнутою.