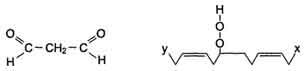Материал: Biokhimia_Bilety_1-1968421400-1498556783
2.Витамин d
Антирахитический витамин. Существуют два витамера:
D2 – эргокальциферол и D3 – холекальциферол.
Витамин D2 содержится в грибах. Витамин D3 синтезируется в организме под действием УФО (ультрафиолетового облучения):
7-дегидрохолестерол → холекальциферол (D3)
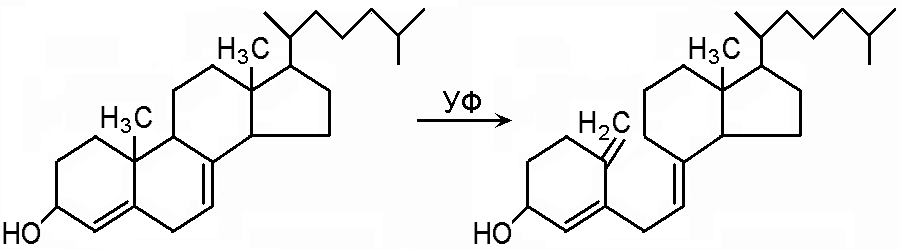
Роль витамина D в обмене веществ:
Витамин D3 (холекальциферол) подвергается в организме превращению. Он поступает в печень, где под действием 25-гидроксилазы превращается в 25-гидроксихолекальциферол, затем в почках под действием ПТГ и 1-гидроксилазы – в 1,25-дигидроксихолекальциферол (гормон кальцитриол)
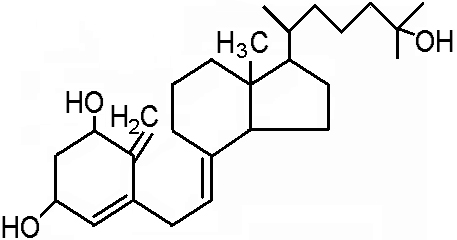
кальцитриол
Функции кальцитриола
1. регулирует всасывание кальция и фосфора в кишечнике путем активации синтеза в энтероцитах кальций-связывающего белка (кальбиндина D);
2. в костях способствует минерализации ткани, поддержанию нормальной концентрации кальция и фосфора в межклеточном пространстве.
(повышает активность щелочной фосфатазы, повышает концентрацию кальций-связывающего белка и остеокальцина)
Гиповитаминоз D приводит к снижению уровня кальция в крови, снижению кальция и фосфора в межклеточном пространстве, нарушению минерализации костной ткани.
Авитаминоз D – рахит. Различают рахит I типа (при недостатке витамина D) и рахит II типа (при недостатке рецепторов). Проявляется рахит деформациями скелета ("рахитические четки", Х-образные или О-образные голени, килевидная грудная клетка).
Недостаток витамина D у взрослых сопровождается остеомаляцией, а в крови увеличивается активность щелочной фосфатазы.
Причины гиповитаминозов D:
- недостаток витамина D в пище
- недостаток УФ (солнечного) облучения
- недостаток парат-гормона
Суточная потребность вит. D 0,012-0,025 мг.
Источники витамина D: яичный желток, рыбий жир, сливочное масло (лучше летнее), печень, молоко.
4.Транспорт кислорода в крови
Основная часть кислорода связана с гемоглобином (оксигемоглобин, HbO2) и истинное содержание кислорода в крови зависит от двух дополнительных параметров – концентрации Hb и сатурации (насыщении) гемоглобина кислородом (HbOsat или SO2).
Оксигемоглобин (HbО2) – процентное содержание в крови, является отношением фракции оксигемоглобина (HbО2) к сумме всех фракций (общему гемоглобину).
Насыщение (сатурация) гемоглобина кислородом (HbOSAT, SО2), представляет собой отношение фракции оксигенированного гемоглобина к тому количеству гемоглобина в крови, который способен транспортировать О2.
4. Субстратное фосфорилирование
Субстратное фосфорилирование [лат. substratum — подстилка, подкладка; греч. phos — свет и phoros — несущий] — синтез богатых энергией фосфорных соединений (в основном АТФ, см. Аденозинтрифосфат, АТФ) за счет энергии окислительно-восстановительных реакций гликолиза (катализируемых фосфоглицеральдегиддегидрогеназой и энолазой) и при окислении ?-кетоглутаровой кислоты в цикле трикарбоновых кислот (под действием a-кетоглутаратдегидрогеназы и сукцинаттиокиназы). При С.ф. происходит перенос фосфорильной группы, образующейся из ортофосфорной кислоты, на аденозиндифосфат (АДФ) с образованием АТФ
№14.
-
Челночные механизмы транспорта через мембрану митохондрий.
Так как сама молекула НАДН через мембрану не проходит, то существуют специальные системы, принимающие атомы водорода от НАДН в цитоплазме и отдающие их в матриксе митохондрий. Эти системы получили название челночные системы.
Определены две основные челночные системы – глицеролфосфатная и малат-аспартатная
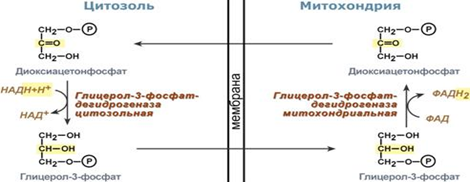
-
Коферменты . Их роль. Связь с витаминами
Коферменты в каталитических реакциях осуществляют транспорт различных групп атомов, электронов или протонов. Коферменты связываются с ферментами: ковалентными связями; ионными связями; гидрофобными взаимодействиями и т.д. Один кофермент может быть коферментом для нескольких ферментов. Многие коферменты являются полифункциональными (например, НАД, ПФ). В зависимости от апофермента зависит специфичность холофермента. Все коферменты делят на две большие группы: витаминные и невитаминные.
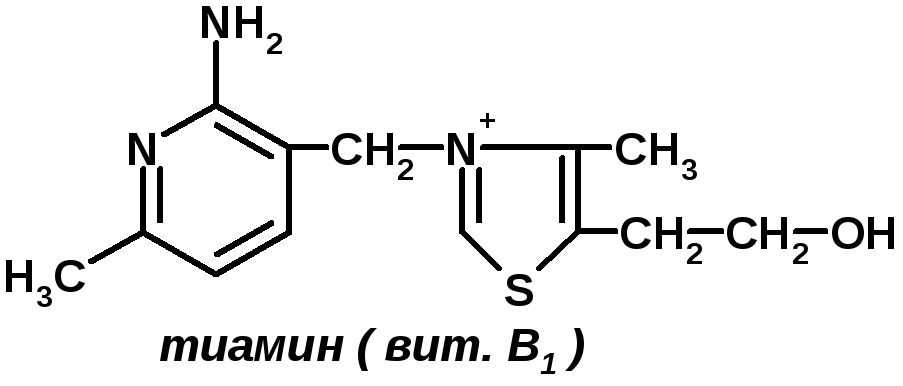
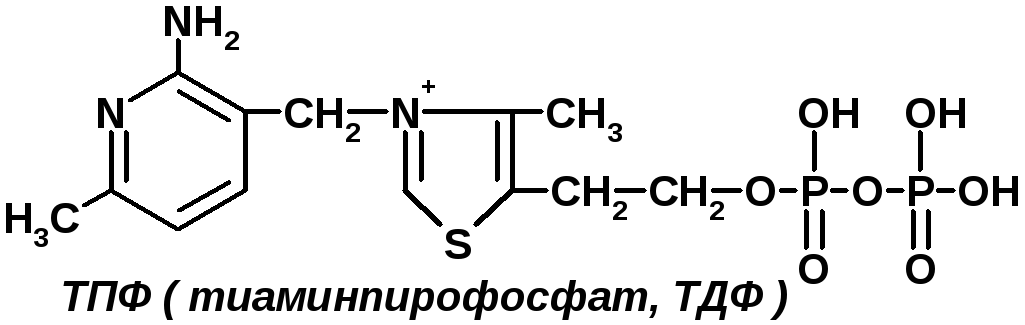
Коферменты витаминной природы – производные витаминов или химические модификации витаминов.
Сюда относят:флавинмононуклеотид (ФМН); флавинадениндинуклеотид (ФАД).Ребитол и изоалоксазин образуют витамин В2. Витамин В2 и остаток фосфорной к-ты образуют ФМН
ФМН в соединении с АМФ образуют ФАД.
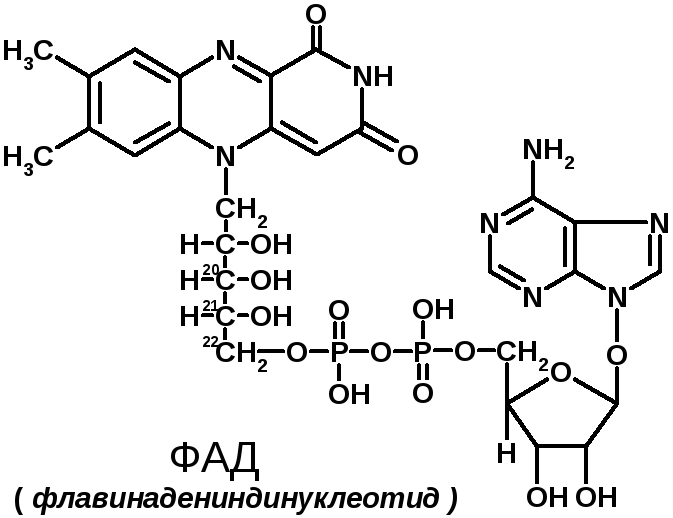
-
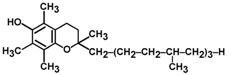
Витамин е
Жирорастваримый
антистерильный витамин, антиоксидантный энзим.
В химическом плане это альфа-, бета-, гамма- и дельта-токоферолы, но преобладающим является альфа-токоферол.
Витамин Е устойчив к нагреванию.
Роль витамина Е в обмене веществ
1. регулирует интенсивность свободно-радикальных реакций. Препятствует перекисному окислению липидов биомембран;
2. повышает активность витамина А.
Суточная потребность витамина Е 20-25 мг. Источники витамина Е: растительные масла (!), а также печень, желток яиц, проросшие зерна; масло облепихи.
-
Гемоглобин
Гемоглобин входит в состав группы белков гемопротеины, которые сами являются подвидом хромопротеинов и подразделяются на неферментативные белки (гемоглобин, миоглобин) и ферменты (цитохромы, каталаза, пероксидаза). Небелковой частью их является гем – структура, включающая в себя порфириновое кольцо (состоящее из 4 пиррольных колец) и иона Fe2+. Железо связывается с порфириновым кольцом двумя координационными и двумя ковалентными связями.
№15
1. АДФ,АТФ
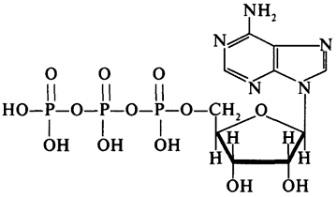
АТФ (Аденозинтрифосфа́т)
Значение АТФ При расщеплении АТФ на АДФ и неорганический фосфат (Фн) высвобождается энергия:
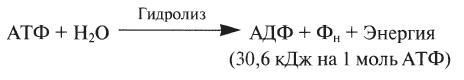
Помимо энергетической АТФ выполняет в организме ещё ряд других не менее важных функций:
-Вместе с другими нуклеозидтрифосфатами АТФ является исходным продуктом при синтезе нуклеиновых кислот.
-Кроме того, АТФ отводится важное место в регуляции множества биохимических процессов. Являясь аллостерическим эффектором ряда ферментов, АТФ, присоединяясь к их регуляторным центрам, усиливает или подавляет их активность.
-АТФ является также непосредственным предшественником синтеза циклического аденозинмонофосфата — вторичного посредника передачи в клетку гормонального сигнала.
-Также известна роль АТФ в качестве медиатора в синапсах и сигнального вещества в других межклеточных взаимодействиях (пуринергическая передача сигнала
Аденозиндифосфат (АДФ) — нуклеотид, состоящий из аденина, рибозы и двух остатков фосфорной кислоты. АДФ образуется в результате переноса концевой фосфатной группы АТФ. АДФ участвует в энергетическом обмене во всех живых организмах.
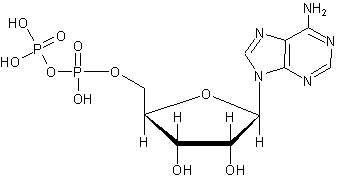
-
Продукты распада гемоглобина
Распад гемоглобина протекает в клетках макрофагов, в частности в звездчатых ретикулоэндотелиоцитах, а также в гистиоцитах соединительной ткани любого органа.
Основная часть желчных пигментов образуется при распаде гема и гемоглобина в клетках ретикулоэндотелиальной системы (РЭС) и представляет собой многоступенчатый процесс: при окислении гемоглобина образуется вердоглобин; после отщепления глобина и железа образуется биливердин, который далее восстанавливается до билирубина.
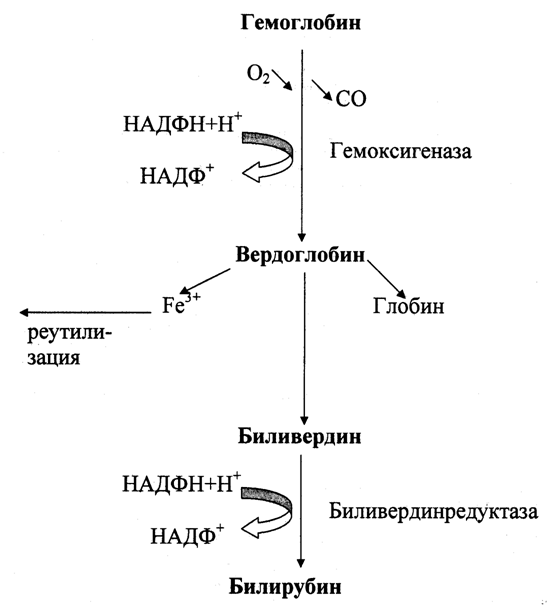
-
Билирубин — желто-красный пигмент, представляющий собой линейный тетрапиррол, токсичное, жирорастворимое вещество, способное нарушать окислительное фосфорилирование в клетках, в первую очередь в нервной ткани. В крови билирубин либо находится в свободном состоянии, либо в комплексе с альбумином (частично в виде альбумин-фосфатидного комплекса), в меньшем количестве — в комплексах с металлами, аминокислотами, пептидами и другими малыми молекулами. Образование таких комплексов предотвращает выделение билирубина с мочой. Такая форма билирубина называется свободной (неконъюгированной, несвязанной, непрямой). Она не дает прямой реакции с диазореактивом Эрлиха.
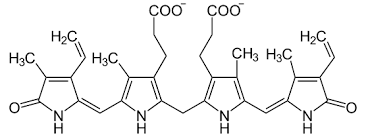
(Билирубин )
-
Витамин к
Жирорастворимый витамин,
Антигеморрагический витамин.
Витамеры: К1 – филлохинон и К2 – менахинон.
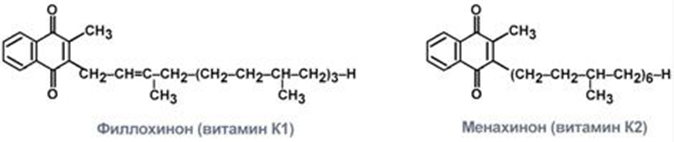
Строение двух форм витамина К
Роль витамина К в обмене веществ
Это кофактор карбоксилирования глутаминовой кислоты (ГЛУ) в белке крови протромбине для его превращения в тромбин.
протромбин → тромбин [карбоксилирование гамма-углеродного звена остатка глутамата]
Антагонист витамина К – варфарин (крысиный яд), он близок по структуре к витамину К, является антикоагулянтом.
Витамин К поступает в организм с зелеными растениями (шпинат, крапива), жирами, а также синтезируется микрофлорой кишечника.
Гиповитаминоз К проявляется геморрагиями.
Авитаминоз К чаще наблюдается при нарушении всасывания его в кишечнике.
{водорастворимая форма витамина К - викасол}
№16
-
Перекисное окисление
ПОЛ - цепные реакции, обеспечивающие расширенное воспроизводство свободных радикалов, частиц, имеющих неспаренный электрон, которые инициируют дальнейшее распространение перекисного окисления.
429
Стадии перекисного окисления липидов
1) Инициация: образование свободного радикала (L•)
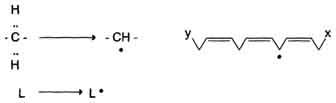
Инициирует реакцию чаще всего гидроксильный радикал, отнимающий водород от СН2-групп полиеновой кислоты, что приводит к образованию липидного радикала.
2) Развитие цепи:
L • + О2 → LOO • LOO• + LH → LOOM + LR•
Развитие цепи происходит при присоединении О2, в результате чего образуется липопе-роксирадикал LOO• или пероксид липида LOOH.
ПОЛ представляет собой свободнорадикальные цепные реакции, т.е. каждый образовавшийся радикал инициирует образование нескольких других.
3) Разрушение структуры липидов