Материал: Biokhimia_Bilety_1-1968421400-1498556783
Цитохром (Cytochrome)
дыхательный пигмент, в состав которого входит белок, связанный сгемом. Цитохромы являются переносчиками электронов в биологических реакциях окисления-восстановления, в частности, в дыхательной цепи митохондрий
Сложные белки построены из двух компонентов - простой белок и небелковое вещество, называемое простетической группой. Простетические группы прочно связаны с белковой частью молекулы.
Классификация сложных белков зависит от строения простетической группы.
-
Гликопротеины (содержат углеводы).
-
Липопротеины (содержат липиды).
-
Фосфопротеины (содержат фосфорную кислоту).
-
Хромопротеины (содержат окрашенную простетическую группу).
-
Металлопротеины (содержат ионы различных металлов).
-
Нуклеопротеины (содержат нуклеиновые кислоты).
2. Алассторические центры и регуляторные ферменты
Ряд ферментов могут содержать аллостерический центр. [рис. фермента с аллостерическим и активным центрами] Эти ферменты относят к аллостерическим ферментам. К аллостерическому центру присоединяются различные вещества, отличные по строению от субстрата. Эти вещества могут изменять конформацию активного центра, т.е. влиять на связывание и превращение субстрата, они называются аллостерическими эффекторами. Все аллостерические эффекторы делятся на положительные – активаторы, и отрицательные – ингибиторы.
Все химические реакции в клетке протекают при участии ферментов. Поэтому, чтобы воздействовать на скорость протекания метаболического пути, достаточно регулировать количество или активность ферментов. Обычно в метаболических путях есть ключевые ферменты, благодаря которым происходит регуляция скорости всего пути. Эти ферменты (один или несколько в метаболическом пути) называются регуляторными ферментами; они катализируют, как правило, начальные реакции метаболического пути, необратимые реакции, скорость-ли-митирующие реакции (самые медленные) или реакции в месте переключения метаболического пути (точки ветвления).
Регуляция скорости ферментативных реакций осуществляется на 3 независимых уровнях:
-
изменением количества молекул фермента;
-
доступностью молекул субстрата и кофер-мента;
-
изменением каталитической активности молекулы фермента.
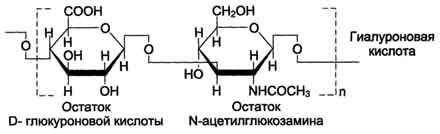
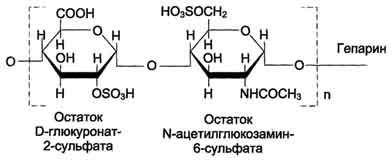
3. 4. Гликозаминогликаны соединительной ткани
Гликозаминогликаны - линейные отрицательно заряженные гетерополисахариды. РаНbше их называли мукополисахаридами, так как они обнаруживались в слизистых секретах (мукоза) и придавали этим секретам вязкие, смазочные свойства. Эти свойства обусловлены тем, что гликозаминогликаны могут связывать большие количества воды, в результате чего межклеточное вещество приобретает желеобразный характер.
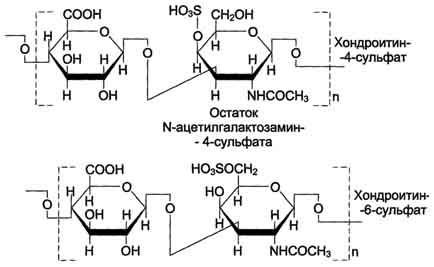
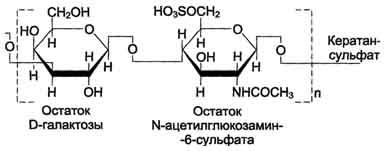
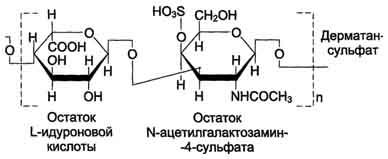
В настоящее время известна структура шести основных классов гликозаминогликанов
№11
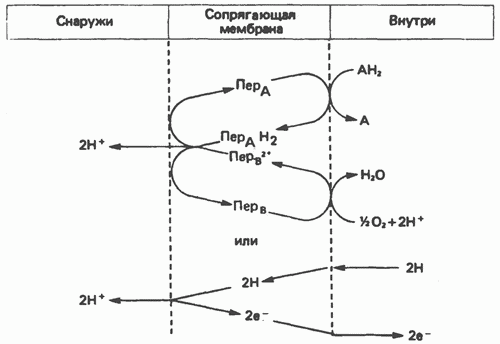
1 Хемиосмотическая теория Митчела.
1. Мембраны митохондрий непроницаемы для протонов.
2. В результате процессов окисления в митохондрии формируется протонный потенциал (электрохимический градиент протонов).
3. Диффузия протонов обратно на внутреннюю поверхность мембраны сопряжено с фосфорилированием, которое осуществляется АТФ-синтетазой.
2. Механизм действия ферментов. Кинетика ферментативного катализа.
Механизм действия:
а) присоединение ингибитора к аллостерическому центру;
б) изменяется конформация фермента;
в) изменяется конформация активного центра;
г) нарушается комплиментарность активного центра фермента к субстрату;
д) уменьшается число молекул ES;
е) уменьшается скорость ферментативной реакции.
Ведущую роль в механизме ферментативного катализа играет образование фермент-субстратного комплекса. По этой теории весь процесс катализа можно разделить на 3 этапа:
1 этап: образование фермент-субстратного комплекса
2 этап: происходит последовательное преобразование первичного фермент-субстратного комплекса в 1 или несколько активированных.
3 этап: отделение продуктов от активного центра фермента и диффузия их в окружающую среду
3. Витамин а
Жирорастворимый витамин
Витамеры: А1 – ретинол и А2 – ретиналь.
Клиническое название: антиксерофтальмический витамин.
По химической природе: циклический непредельный одноатомный спирт на основе кольца β -ионона.
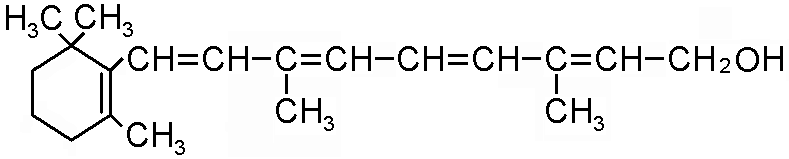
Может разрушаться кислородом, является антиоксидантом.
-
4. Содержание белка в плазме крови. Диагностическое значение.
В плазме крови содержится 7% всех белков организма при концентрации 60 - 80 г/л. Белки плазмы крови выполняют множество функций. Одна из них заключается в поддержании осмотического давления, так как белки связывают воду и удерживают её в кровеносном русле.
№12
-
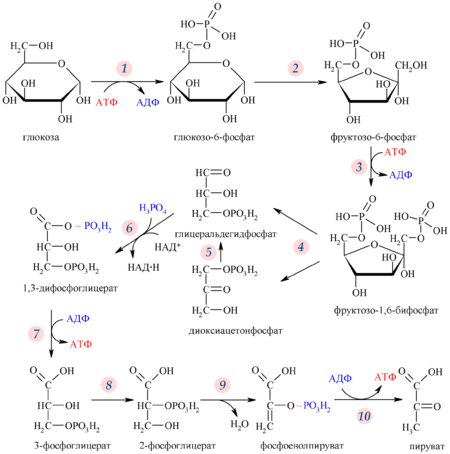
1 Гликолиз-расщепление
-
Витамин к
Жирорастворимый витамин,
Антигеморрагический витамин.
Витамеры: К1 – филлохинон и К2 – менахинон.
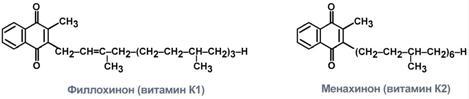
Строение двух форм витамина К
Роль витамина К в обмене веществ
Это кофактор карбоксилирования глутаминовой кислоты (ГЛУ) в белке крови протромбине для его превращения в тромбин.
протромбин → тромбин [карбоксилирование гамма-углеродного звена остатка глутамата]
Антагонист витамина К – варфарин (крысиный яд), он близок по структуре к витамину К, является антикоагулянтом.
Витамин К поступает в организм с зелеными растениями (шпинат, крапива), жирами, а также синтезируется микрофлорой кишечника.
Гиповитаминоз К проявляется геморрагиями.
Авитаминоз К чаще наблюдается при нарушении всасывания его в кишечнике.
{водорастворимая форма витамина К - викасол}
3 женские половые
-
Гонады - яйчники и семенники - железы смешанного типа. По химической природе их гормоны - стероиды. Андрогены (мужские) синтезируются в семенниках и коре надпочечников. Эстрогены (женские) - в яичниках и коре надпочечников. Синтезируются из холестерола, который образуется из Ац-КоА. Ац-КоА→ холестерол→ прегненолон →прогестерон →кортикостероиды. Из прогестерона также образуются андрогены (тестостерон) , а из них - эстрогены. Эстрогены: эстрадиол, эстрон (образуется из эстрадиола в плаценте), эстриол, прогестерон.
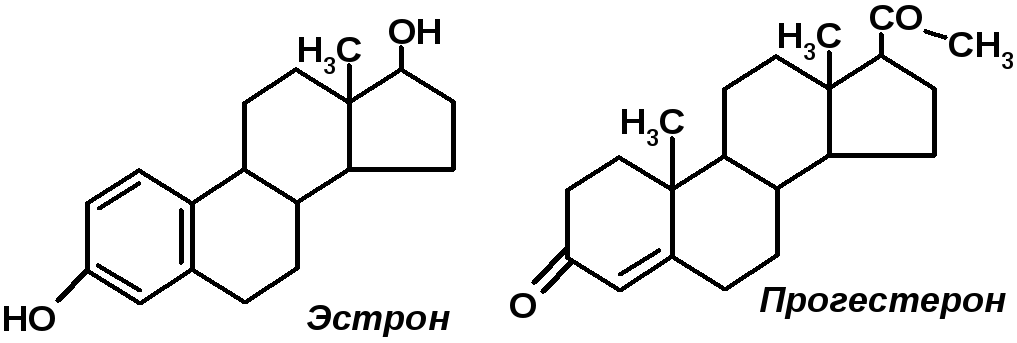
-
Гликолиз
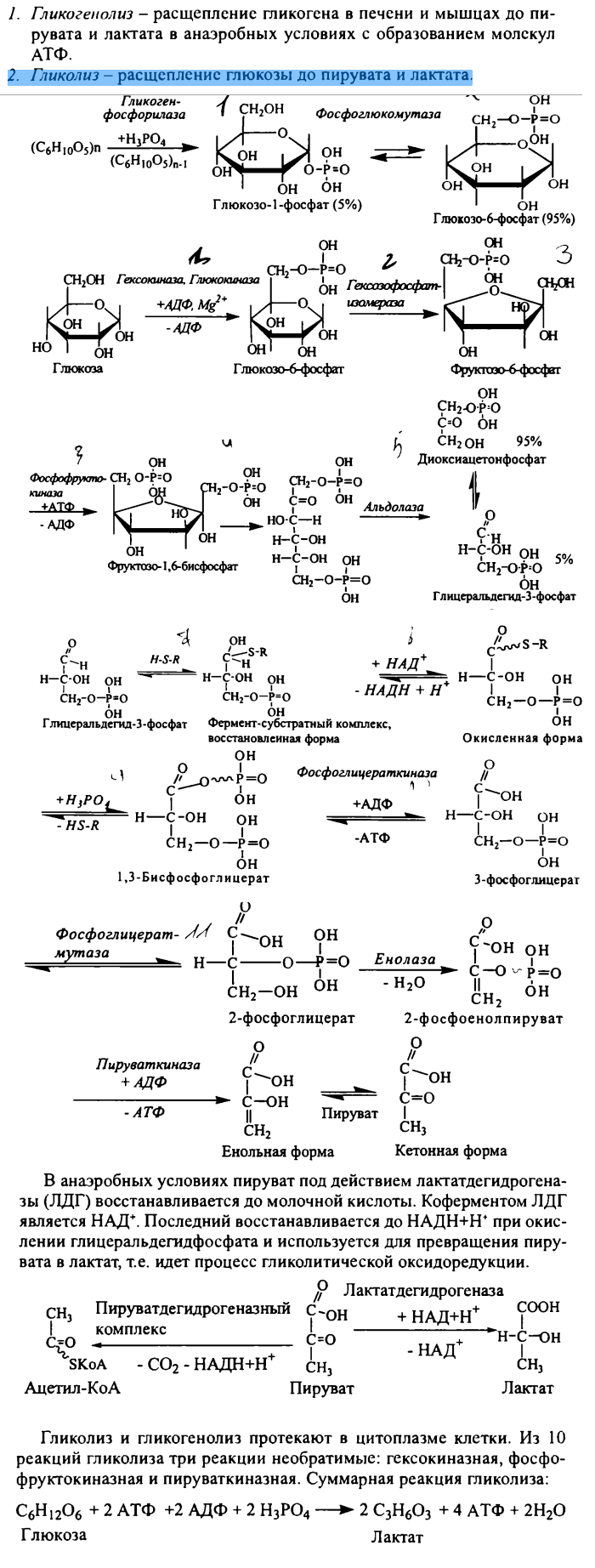
№13
-
1. Конкурентное,неконкурентное ингибирование
По механизму действия выделяют:
- конкурентное ингибирование;
- неконкурентное ингибирование;
- субстратное ингибирование;
- аллостерическое
1) Конкурентное (изостерическое) ингибирование – это торможение ферментативной реакции, вызванное связыванием ингибитора с активным центром фермента. При этом ингибитор имеет сходство с субстратом
2) Неконкурентное ингибирование – торможение, связанное с влиянием ингибитора на каталитическое превращение, но не на связывание фермента с субстратом. В этом случае ингибитор может связываться и с активным центром (каталитический участок) и вне его.