Материал: Biokhimia_Bilety_1-1968421400-1498556783
Значение ЦТК.
1.Интегративное – цикл Кребса объединяет пути катаболизма углево- дов, белков и жиров, т.к. в нем утилизируется молекулы ацетил-КоА, образующиеся при расщеплении этих веществ.
2.Энергетическое. При расщеплении 1 молекулы ацетил-КоА до конечных продуктов (СО2 и Н2О) генерируется 12 молекул АТФ.
3.Амфиболическое (двойственное). В ЦТК происходит не только катаболические про- цессы – окисление ацетил-КоА. Субстраты ЦТК используются и для реакций синтеза (анабо- лические процессы). Так, из оксалоацетата синтезируется аспарагиновая кислота; из α- кетоглутаровой кислоты – глутаминовая; из оксалоацетата - фосфоэнолпируват.
2. Субклеточные ферментативные процессыФЕРМЕНТЫ, органические вещества белковой природы, которые синтезируются в клетках и во много раз ускоряют протекающие в них реакции, не подвергаясь при этом химическим превращениям.
Химические процессы в клетке протекают с большой скоростью благодаря действию биологических катализаторов - ферментов или энзимов. Белковую часть фермента называют апоферментом. Небелковый компонент, прочно связанный, называют простетической группой, слабо связанный, обслуживающий несколько ферментов - коферментом. В состав простетических групп и коферментов входят металлы (железо, медь, цинк), витамины и их производные. Эндоферменты функционируют в клетке, а экзоферменты выделяются из клетки или локализуются в плазмалемме и действуют снаружи от нее.
Ферменты обладают специфичностью как к субстратам (субстратная специфичность), так и к определенным химическим реакциям (специфичность действия). Названия ферментов обычно заканчиваются суффиксом “аза”, за исключением некоторых общепринятых названий, например, пепсин, трипсин и другие. Название, как правило, отражает природу субстрата (хитиназа расщепляет хитин), или функцию фермента (аминотрансфераза переносит аминогруппы), или же то и другое вместе (алкогольдегидрогеназа)
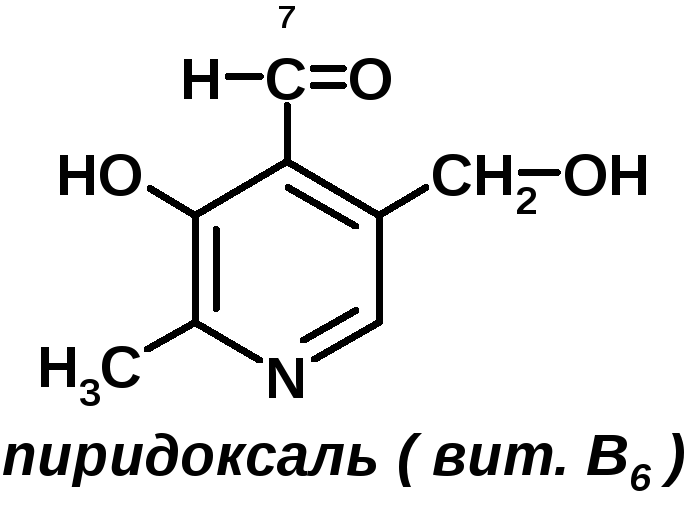
3. Витмин В6Антидерматитный витамин.
Пиридоксин → пиридоксаль → пиридоксамин [нарисовать формулы]
 Роль
витамина
Роль
витамина
1. он необходим для образования ПФ (пиридоксальфосфата) – кофермента амино-ТФ, декарбоксилаз АК, дезаминаз АК;
2. необходим для превращения триптофана в витамин РР;
3. нужен для превращения дельта-аминолевулиновой кислоты в гем.
{Т.е., вит.В6 нужен для обмена аминокислот}
Гиповитаминоз В6: анемия из-за нарушения обмена АК, плюс дерматиты, стоматиты, глосситы, конъюнктивиты.
Суточная потребность в витамине В6 2-3 мг.
Источники: печень, дрожжи, хлеб грубого помола, горох. Также он синтезируется микрофлорой кишечника.
Гиповитаминоз возможен при длительном употреблении антибиотиков, особенно, противотуберкулезных препаратов.
4. Нервная ткань её биоэнергетика, углеводы, липиды, аминокислоты
1. Генерация электрического сигнала (нервного импульса) 2. Проведение нервного импульса. 3. Запоминание и хранение информации. 4. Формирование эмоций и поведения.
5. Мышление.
Особенности химического состава и метаболизма нервной ткани
Специфику нервной ткани определяет гематоэнцефалический барьер (ГЭБ). Гематоэнцефалический барьер имеет избирательную проницаемость для различных метаболитов, а также способствует накоплению некоторых веществ в нервной тканиМетаболизм углеводов и особенности энергетического обеспечения нервной ткани В нервной ткани, составляющей только 2 % от массы тела человека, потребляется 20 % кислорода, поступающего в организм.
Липиды (жиры), как правило составлены из молекулы глицерина, к которой сложно-эфирной связью крепятся от одной (моноглицериды) до трёх (триглицериды) жирных кислот.
Углеводы состоят из мономеров, называемых моносахариды, как например глюкоза (C6H12O6), фруктоза (C6H12O6)[25], и дезоксирибоза(C5H10O4). Во время синтеза молекулы дисахарида из двух молекул моносахаридов образуется молекула воды.
Белки как правило являются крупными молекулами — макробиополимерами. Их мономерами являются аминокислоты.
№8 1. Біоенергетика ЦТК
результате окисления, катализируемого дегидрогеназами ЦТК, на каждую катаболизируемую за период одного цикла молекулу ацетил-СоА образуются три молекулы НАДН и одна молекула ФАДН2. Эти восстановительные эквиваленты передаются в дыхательную цепь, локализованную в митохондриальной мембране.
При прохождении по цепи восстановительные эквиваленты НАДН генерируют три высокоэнергетические фосфатные связи посредством образования АТФ из АДФ в процессе окислительного фосфорилирования. За счет ФАДН2 генерируется только две высокоэнергетические фосфатные связи, поскольку ФАДН2 переносит восстановительные эквиваленты на кофермент Q и, следовательно, в обход первого участка цепи окислительного фосфорилирования в дыхательной цепи. Еще один высокоэнергетический фосфат генерируется на одном из участков цикла лимонной кислоты, то есть на субстратном уровне, при превращении сукцинил-СоА в сукцинат. Таким образом, за период каждого цикла образуется 12 новых высокоэнергетических фосфатных связей
2. Специфічність ферментів
Специфичность - наиболее важное свойство ферментов, определяющее биологическую значимость этих молекул. Различают субстратную и каталитическую специфичности фермента, определяемые строением активного центра (рис. 2-2).
1. Субстратная специфичность
Под субстратной специфичностью понимают способность каждого фермента взаимодействовать лишь с одним или несколькими определёнными субстратами. Различают:
-
абсолютную субстратную специфичность;
-
групповую субстратную специфичность;
-
стереоспецифичность.
Абсолютная субстратная специфичность
Активный центр ферментов, обладающих абсолютной субстратной специфичностью, комплементарен только одному субстрату. Следует отметить, что таких ферментов в живых организмах мало.
 3.
Вітамін С
3.
Вітамін С
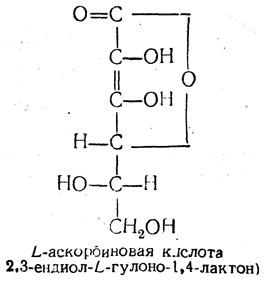
Витамин с
Аскорбиновая кислота, антискорбутный витамин (скорбут = цинга).
Является лактоном. Легко окисляется:
аскорбат дегидроаскорбат
Енольные гидроксилы неустойчивы, особенно в присутствии кислорода. В кислой среде витамин С сохраняется лучше.
Роль витамина с в обмене веществ
1. участвует в реакциях гидроксилирования (ЛИЗ→ОЛИ, ПРО→ОПР), что требуется для "сшивок" молекул коллагена в соединительной ткани;
2. участвует в триптофана и диоксиметила с образованием нейромедиаторов (норадреналин и др.);
3. необходим для синтеза кортикостероидов;
4. необходим для образования нейромедиаторов.
Гиповитаминоз С проявляется поражением соединительной ткани – повышенная хрупкость сосудов, пипехии (точечные кровоизлияния на коже), кровоточивость десен.
Авитаминоз С – цинга (скорбут): кровоизлияния во внутренние органы, более выраженные повреждения соединительной ткани.
Суточная потребность витамина С 100-150 мг. Она возрастает при инфекционных заболеваниях, стрессовых состояниях, лактации, беременности – до 300 мг/сут.
Источники витамина С: овощи, фрукты, зеленые растения; главные – черная смородина, шиповник, грецкий орех, цитрусовые. В России основным источником его является картофель (10 мг/100 г) и квашенная капуста.
Причины гиповитаминоза С:
1. витамин С неустойчив;
2. он необходим в относительно больших количествах;
3. в организме отсутствуют запасы витамина С. 4. Скелетні мязи
4.Белки саркоплазмы: миоген(проявл активность ферментов гликолиза, тканевого дых), миоглобин(соединение с О2), глобулинХ и миоглобулин. Белки миофибрилл: миозин(АТФазная активность) 10 мол миозина=толстые нити, F-актин –тонкие нити. Актомиозин-временное соедиение актина и миозина(в момент сокращения) Тропомиозин возле желобов нити F-актина, соединяется с тропином образ нативный тропомизин и тропонин (тропонин1-связь с тромбином, тропин2 – связывается с актином, блокирует гидролиз АТФ, тропин3- присоед 4иона Са2+ К азотсодерж. Экстрактивным в-вам относ нуклеотиды (адниловые, цитидиловые, уридиловые), среди кот большое значение имеют АТФ,АДФ,АМФ. Это креатин, креатинфосфат, креатинин, глутаминовая и др аминокислоты, глутамин. Дипиптиды(только в мышцах!): карнозин(гистидин+бета аланин) ансерин(метилкарнозин), которые способствуют мышечному сокращению. Углеводы мышечной ткани Гликоген: 0,2-2%, но мышечная масса настолько велика, что содержание гликогена в мышцах в целом в 2 раза больше, чем в печени. Также содержаться гексозомонофосфаты, триозомонофосфаты, ПВК, молочная кислота, следы глюкозы (свободной почти нет). Липиды – около 1%. Представлены нейтральными жирами в соединительно-тканных волокнах. Холестерол и фосфолипиды – компоненты биомембран. Жирные кислоты играют особую роль в миокарде как источник энергии. Минеральные вещества. K+, Na+ участвуют в передаче возбуждения; также содержаться Ca++, Mg++, Fe++ (особенно много в миоглобине). Биохимия мышечного сокращения Теория Хэнсона и Хаксли: укорочение за счет проникновения нитей актина между нитями миозина. При этом необходимо наличие Са2+. В покое кальций находится в трубочках саркоплазматического ретикулума. Са-зависимая АТФ-аза как бы закачивает Са2+ в трубочки за счет распада АТФ. Т.е. если много АТФ, то свободного Са++ мало.Если возникает раздражение нервного волокна, то Са2+ выходит из саркоплазматического ретикулума за счет изменения проницаемости мембраны, и выход его приводит к взаимодействию головки миозина с актином. Если есть Са2+ и АТФ, то белки продвигаются друг между другом. В покое миозин связан с Mg и АТФ. Если нет расщепления АТФ, то спайки не образуются. Выход Са2+ вызывает распад АТФ и образование спаек.1. SR-Ca2+ (нервное возбуждение) SR+ Ca2+ 2. активация актина: А-Тр+ Ca2+ А+ Тр- Ca2+ 3. активация АТФ-азы кальция: Миозин-АТФ +Н2О+Са2+(АТФ-аза) Миозин~Фосфат + АДФ 4. взаимодействие миозина и актина: М~Ф + А (+Са2+, +Н2О)М~А + Фн 5. М~А (сокращение)М-А+ работа
Для расслабления тоже нужна энергия АТФ:
1. М-А + АТФМ-АТФ + А
2. связывание Са2+: Т-Са2++SR+АТФТ+SR- Са2++ АДФ+Фн
3. связывание тропонина с актином: Т+АТ-А
№9
1.Флавінові ферменти.
ФЛАВИНОВЫЕ ФЕРМЕНТЫ, сложные ферменты, простетич. группами к-рых служат производные рибофлавина. У нек-рых Ф. ф. простетич. группой является флавинмононуклеотид (ФМН), к-рый состоит из остатка рибофлавина и фосфорной к-ты. Простетич. группа большинства Ф. ф.— флавинадениндинуклеотид (ФАД), в состав к-рого входит один остаток рибофлавина, два остатка фосфорной к-ты, рибоза и аденин. Ф. ф.— промежуточные переносчики водорода в цепи биологическою окисления.
Флавиновые ферменты осуществляют обратимую реакцию дегидрирования (отщепления- присоединения атомов водорода) от субстрата
2.Сучасна класифікація ферментів
Ферменты – это биологические катализаторы белковой природы.
Согласно Международной классификации, ферментыделят на шесть главных классов, в каждом из которых несколько подклассов: 1) оксидоредуктазы; 2) трансферазы; 3)гидролазы; 4) лиазы; 5) изомеразы; 6) лигазы (синтетазы)
Оксидоредуктазы. К классу оксидоредуктаз относят ферменты, катализирующие с участием двух субстратовокислительно-восстановительные реакции, лежащие в основе биологического окисления.
Трансферазы. К классу трансфераз относят ферменты, катализирующие реакции межмолекулярного переноса различных атомов, групп атомов и радикалов.
Гидролазы. В класс гидролаз входит большая группа ферментов, катализирующих расщепление внутримолекулярных связей органических веществ при участии молекулы воды.
Лиазы. К классу лиаз относят ферменты, катализирующие разрыв связей С—О, С—С, С—N и других, а также обратимые реакции отщепления различных групп от субстратов не гидролитическим путем.
Изомеразы. К классу изомераз относят ферменты, катализирующие взаимопревращения оптических игеометрических изомеров.
Лигазы (синтетазы). К классу лигаз относят ферменты, катализирующие синтез органических веществ из двух исходных молекул с использованием энергии распада АТФ (или другого нуклеозидтрифосфата).
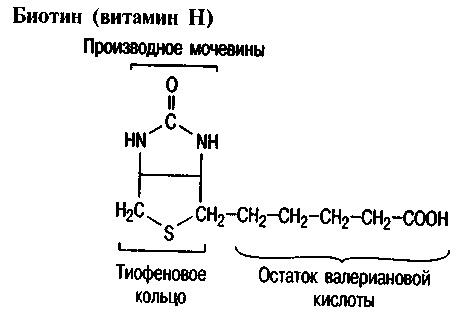
3.Біотин Витамин н (биотин)
Антисеборейный витамин. Структура: тиофен, соединеный с мочевиной+ боковая цепь (валериановая кислота).
Устойчив при нагревании.
Роль биотина в обмене веществ
Биотин – кофермент карбоксилирования (превращение ацетил-КоА в малонил-КоА в синтезе ВЖК) и кофермент транскарбоксилирования в синтезе пуриновых оснований.
Авитаминоз Н – себорея: покраснение и шелушение сальной кожи на волосистой части головы.
Суточная потребность витамина Н 0,010 мг.
Источники: печень, яйца, молоко.
Авитаминоз бывает при употреблении сырых яиц, содержащих авидин (антивитамин Н).
Билет 10 1. ЦИТОХРОМЫ, сложные белки