Материал: ---Готовые билеты---
![]()
![]() т.е.
представлена как разность двух
энергетических величин, относящихся к
прямой и обратной реакциям.
т.е.
представлена как разность двух
энергетических величин, относящихся к
прямой и обратной реакциям.
![]()
Допущения,
сделанные Аррениусом: ![]()
![]()
Здесь
Е1
и Е2
- энергии активации прямой и обратной
реакции. Ранее имели:
,
следовательно ![]()
Рассмотрим график изменения энергии в процессе протекания экзотермической реакции: A + B = C + D
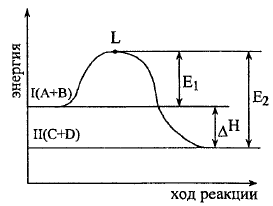 Уровень
L
отвечает тому наименьшему запасу энергии
у молекул, который необходим для их
результативного столкновения. Разность
уровней L
и I
- это энергия активации прямой реакции,
L
и II-
обратной.
Уровень
L
отвечает тому наименьшему запасу энергии
у молекул, который необходим для их
результативного столкновения. Разность
уровней L
и I
- это энергия активации прямой реакции,
L
и II-
обратной.
Для
эндотермической реакции: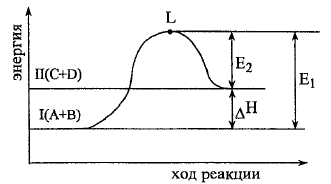
Энергия активации химической реакции. Аналитический и графический метод расчета энергии активации.
С ростом температуры происходит перераспределение энергии между молекулами так, что резко возрастает число активных молекул, обладающих некоторым избытком энергии (энергией активации). Большая часть поступающей в систему энергии тратится на ослабление внутримолекулярных связей, что и делает молекулы активными.
С. Аррениус установил опытным путем зависимость:
![]() где к – константа скорости, А и В –
индивидуальные постоянные, характерные
для данной реакции.
где к – константа скорости, А и В –
индивидуальные постоянные, характерные
для данной реакции.
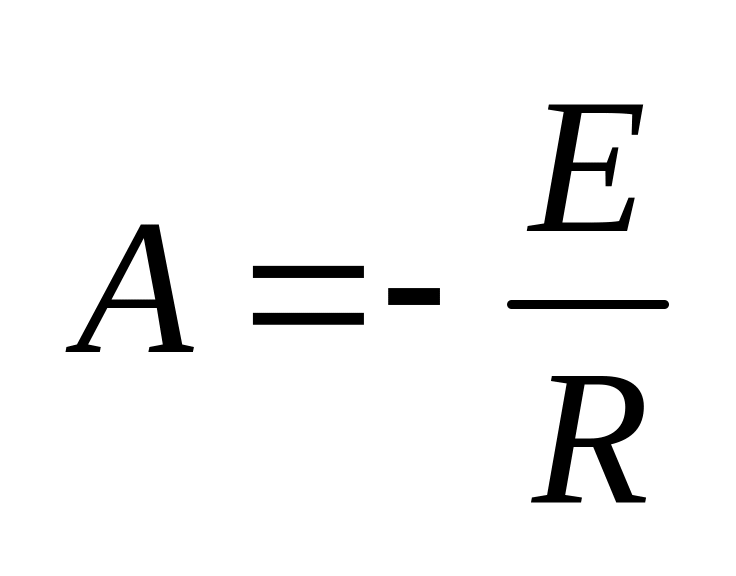 (энергия активации, постоянная – 8,31).
(энергия активации, постоянная – 8,31).
Графический расчет энергии активации.
По опытным данным строят график
зависимости
![]() от обратной температуры. Если закон
выполняется, на графике должна получиться
прямая линия. Тангенс угла, образуемого
Ох и прямой,
от обратной температуры. Если закон
выполняется, на графике должна получиться
прямая линия. Тангенс угла, образуемого
Ох и прямой,
![]()
Аналитический расчет энергии активации.
Полагая, что в небольшом интервале
![]() энергия постоянна, можно написать:
энергия постоянна, можно написать:
![]()
![]()
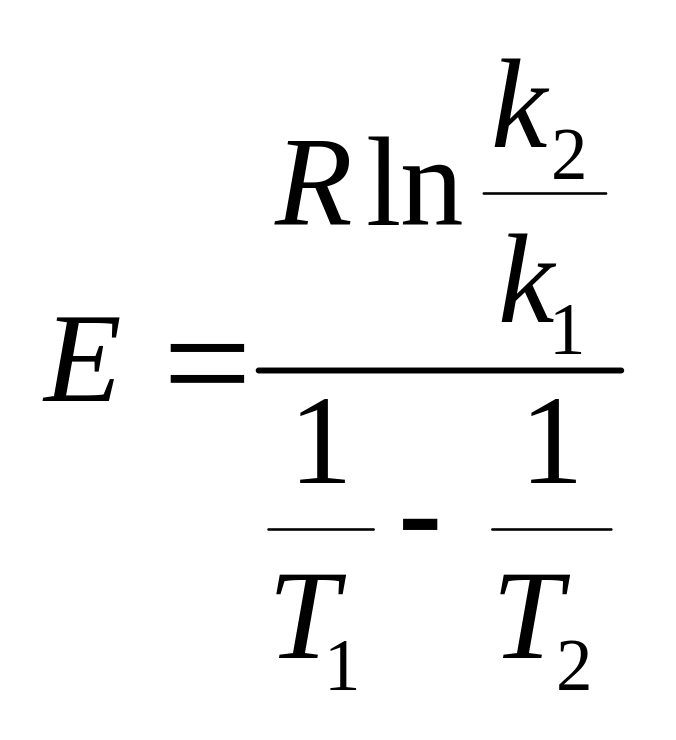
Катализ. Сущность гомогенного и гетерогенного катализа. Стадии гетерогенного катализа.
Катализ изменение скорости реакции под действием некоторых веществ (катализаторов)
Различают положительный катализ (просто катализ) и антикатализ. При катализе скорость реакции увеличивается, при антикатализе - уменьшается.
Вещества, увеличивающие скорость реакции катализаторы, уменьшающие ингибиторы.
Как правило катализатор при реакции не расходуется, ингибитор расходуется.
Существует также и автокатализ в роли катализатора вытсупают продукты реакции.
Катализаторы не оказывают влияния на величину (изменение свободной энергии системы) реакции, следовательно и на константу равновесия. Катализатор лишь ускоряет наступление равновесия реакции, но не смещает его.
Различают гомогенный и гетерогенный катализ. В первом случае реагирующие вещества и катализатор составляют одну фазу.
Скорость реакции прямо пропорциональна количеству катализатора.
Механизм можно объяснить образованием промежуточных нестойких соединений. Реакции идут с меньшей энергией активации => быстрее.
Основная причина ускоряющего действия – уменьшение энергии активации.
Во втором случае – разные фазы.
Имеет значение не количество катализатора, а состояние его поверхности.
Катализатор чаще всего находится в твердой фазе.
Твердые катализаторы – оксиды, сульфиды, металлы и соли.
Согласно теории мультиплетов, существуют определенные закономерности, связывающие расстояния между атомами и расстояния между активными центрами катализатора.
Мультиплет – активный центр на поверхности катализатора, состоящий из нескольких атомов или ионов, имеющий правильную конфигурацию, зависящую от строения всей кристаллической решетки катализатора.
Для протекания определенной реакции молекула должна расположиться особым образом относительно двух активных центров.
Отрицательный катализ вызывается ингибиторами. Они могут расходоваться при протекании процесса. Их действие заключается в том, что они связывают положительные катализаторы либо мешают положительному катализу.
С помощью ингибиторов защищают металл от коррозии в жидких средах, тормозят окислительные процессы в маслах и топливе.
Растворы (разбавленные, концентрированные, насыщенные, пересыщенные). Способы выражения концентраций растворов.
Раствор гомогенная система, в которой одно вещество равномерно распределено в среде другого вещества (или веществ).
Разбавленные растворы: содержание одного компонента мало по сравнению с содержанием другого.
Концентрированные растворы: в них относительные количество растворенного вещества и растворителя одного порядка.
Насыщенный раствор: взятое вещество в нём при заданной температуре более не растворяется даже при продолжительном перемешивании.
Перенасыщенный раствор: содержание растворённого вещества в нём значительно превышает предел насыщения.
Способы выражения концентрации растворов
Молярные доли (дроби) показывают, какую долю составляет число молей данного компонента от общего числа молей всех компонентов раствора.
Процентное выражение концентрации:
![]()
Концентрация, выражаемая через плотность раствора.
Молярная концентрация (СМ) показывает, сколько молей растворённого вещества содержится в 1 л раствора:
![]()
Молялная концентрация (Сm) показывает, сколько молей растворённого вещества находится на 1000 г растворителя:
Энергия активации зависит от температуры.
Чем меньше энергия, тем легче идет реакция и тем больше скорость реакции при данной температуре.
Реакции с энергией меньше
![]() протекают практически мгновенно
протекают практически мгновенно
![]()
Нормальная концентрация (СН) показывает, сколько грамм-эквивалентов растворённого вещества содержится в 1 л раствора.
![]()
Титр это числа граммов растворённого вещества в 1 мл раствора.
Растворимость. Произведение растворимости. Изменение энтальпии и энтропии при растворении.
Растворимость способность веществ растворяться в каком-либо растворителе.
По степени растворимости вещества можно разделить на:
практически нерастворимые (хлорид серебра — 0,0015 г/л);
малорастворимые (гипс — 2 г/л);
хорошо растворимые (сахар — 2000 г/л).
Растворимость кислот, оснований и солей можно определить, пользуясь таблицей растворимости.
Растворимость большинства твёрдых веществ (за исключением немногих, например, гипса, извести) с повышением температуры возрастает.
Коэффициент растворимости — это отношение массы вещества, образующего насыщенный при данной температуре раствор, к объёму растворителя.
Произведением растворимости ПР — постоянная величина, равная произведению концентраций ионов вещества при данной температуре в насыщенном растворе трудно-растворимого электролита.
Изменение энтальпии и энтропии при растворении
Движущими силами образования растворов энтальпийный и энтропийный факторы. Энтропийным фактором объясняется самопроизвольное смешивание двух инертных, практически не взаимодействующих газов гелия и неона (чем слабее взаимодействие молекул, тем больше роль энтропийного фактора в образовании раствора). При растворении газов в жидкости энтропия всегда уменьшается, а при растворении кристаллов возрастает. Знак изменения энтальпии растворения определяется знаком суммы всех тепловых эффектов процессов, сопровождающих растворение, из которых основной вклад вносят разрушение кристаллической решетки и взаимодействие образовавшихся ионов с молекулами растворителя (сольватация).
Физические и химические процессы при растворении. Растворимость твердых тел и жидкостей в жидкостях. Физические и химические процессы при растворении.
Химическое соединение растворителя и растворённого вещества, т.к.:
Одномерный раствор
Присутствует выделение или поглощение теплоты при растворении
Способность измененять объём
Механическая смесь, т.к.:
Состав раствора изменяется в очень широких пределах
Есть возможность обнаружения в свойствах раствора свойств отдельных слагающих его компонентов
Физическая теория растворов:
Растворитель индифферентная среда, в которой равномерно размешиваются молекулы растворённого вещества по всему объёму раствора. Межмолекулярное взаимодействие отсутствует. Растворы рассматриваются как молекулярные смеси.
Химической теории растворов:
Растворитель даёт с растворённым веществом сольваты, молекулы которых образуют с растворителем молекулярную смесь (они менее прочные, легко разрушаются даже при небольшом повышении температуры растворов).
Теплота растворения вещества количество теплоты, поглощаемой (или выделяемой) при растворении одного моля вещества
Растворимость твёрдых веществ в жидкостях
Для идеальных растворов справедливо уравнение Шредера:
![]()
Идеальная растворимость твёрдого вещества увеличивается с повышением температуры.
Давление мало влияет на растворимость твёрдых тел в жидкостях.
Растворимость жидкостей в жидкостях.
Существует неорганическая растворимость жидкости смешиваются друг с другом в любый пропорциях и растворимость до известного предела, когда имеет место расслаивание.
Качественная закономерность гласит: "полярное обычно растворимо в полярном, неполярное - в неполярном".