Материал: ---Готовые билеты---
Донорно-акцепторный механизм ковалентной связи. Комплексные соединения.
Донорно-акцепторная связь (ДАС) – разновидность ковалентной связи.
Выделяют соед.1-го порядка (или валентно-насыщенные соед.)
Пример: H2O,
AgCl, NH3,
HCl, KJ, CuSO4,
FeCl3
и т.д. Реагируя друг с другом дают
соединения высшего порядка (или
комплексные соединений).
![]()
![]() В
комплексных соединениях проявляются
ДАС.
В
комплексных соединениях проявляются
ДАС.
Рассмотрим пример:
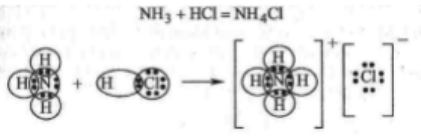
Азот в NH3 – донор, водород в HCl–акцептор.
Комплексные соединения–соединения высшего порядка, возникающие из соединений 1-го порядка без образования новых электронных пар за счет проявления хотя бы одной ДАС.
Основные положения метода молекулярных орбиталей. Связывающие и разрыхляющие орбитали. Энергетические диаграммы.
Основные положения метода молекулярных орбиталей
Образование химических связей является результатом перехода электронов с атомных орбит на новые, называемые МО, и обладающие энергией, определяемой всеми атомами молекулы.
Каждой молекулярной орбитали соответствует определенная энергия, приближенно характеризуемая энергией удаления электрона с данной молекулярной орбитали, энергией ионизации молекулы.
Электроны в молекуле не локализованы в межядерных пространствах, они могут перемещаться в электрическом поле нескольких ее ядер.
Состояние каждого электрона описывается одноэлектронной молекулярной волновой функцией, характеризуемой определенным набором квантовых чисел.
Распределение электронов по новым энергетическим уровням или МО производится в соответствии с принципом наименьшей энергии, правилами Паули и Хунда.
Если переход электронов на МО энергетически выгоден, то химическая связь возникает.
Молекулярная орбита, получающаяся путем вычитания перекрывающихся частей АО, не включает пространства между ядрами. Она имеет более высокую энергию, чем первоначальные АО, и называется разрыхляющей МО.
Молекулярная орбита, которая получается от сложения двух s-орбит, занимает пространство между двумя ядрами; ее называют связывающей МО; ей соответствует энергия, более низкая, чем каждой из двух s-АО, от которых она произошла.
Э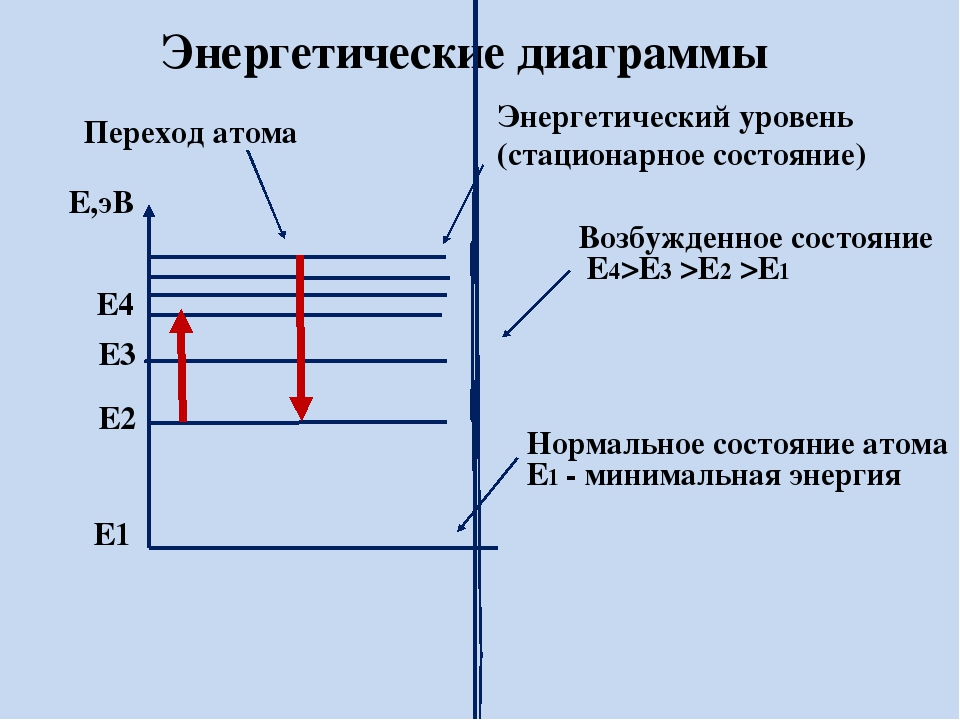 нергетическая диаграмма атома
— это схематическое изображение
орбиталей с учетом их энергии.
нергетическая диаграмма атома
— это схематическое изображение
орбиталей с учетом их энергии.
Металлическая связь. Роль металлической связи в формировании физических и химических свойств металлов.
Металлическая химическая связь— связь между положительными ионами в кристаллах металлов, осуществляемая за счет притяжения электронов, свободно перемещающихся по кристаллу. Добиться состояния одной молекулы металла можно только при очень высоких температурах — когда металл перейдет в газообразное состояние.
Металлическая связь обусловливает характерные свойства металлов:
теплопроводность (перенос теплоты частицами — в данном случае — электронами);
электропроводность;
все вещества — твердые (кроме некоторых щелочных металлов);
высокие температуры плавления и кипения;
характерный металлический блеск
высокая плотность вещества (кроме щелочных металлов);
пластичность — это смещение слоев кристаллической решетки.
Функции состояния: внутренняя энергия и стандартная энтальпия образования химических веществ
Функция состояния
– это термодинамические функции,
значение которых зависит только от
состояния системы, но не зависит от
пути, по которому система пришла в данное
состояние. Для них ![]() ,
где
,
где ![]() – значение данного параметра в начале
процесса, а
– значение данного параметра в начале
процесса, а ![]() – значение в конце.
– значение в конце.
Наиболее важными функциями состояния в термодинамике являются внутренняя энергия U и энтальпия H (теплосодержание)
H=U+PV, где P – давление, а V – объем.
![]() ,
,
![]() .
.
Стандартная энтальпия (теплота) образования вещества – это тепловой эффект реакции образования 1моль химического соединения из простых веществ в стандартных условиях: Т=289 К, Р=1 атм=101325 Па.
Внутренняя энергия представляет собой общий запас энергии системы: энергию поступательного и вращательного движения молекул, энергию колебания атомов, энергию вращения электронов, внутриядерную энергию и так далее, за исключением кинетической энергии системы в целом и потенциальной энергии положения системы.
Теплота q и работа A не являются функциями состояния и их бесконечно малые изменения обозначаются как δq и δA в отличие от полных дифференциалов dU и dH.
Если внутренняя энергия является функцией двух переменных U=f(V,T), то:
![]()
Первое начало термодинамики. Теплота, работа. Закон Гесса. Следствия из закона Гесса. Термохимические расчеты.
Первое начало термодинамики:
В изолированной системе
общий запас энергии сохраняется
постоянным. Поскольку работа является
одной из форм перехода энергии, то,
следовательно, невозможно создание
вечного двигателя первого рода (машины,
совершающей работу без затраты энергии).
Математическая формулировка: ![]()
Различные виды механической работы различного идеального газа
В идеальном газе все виды взаимодействия – это упругие соударения друг с другом (взаимодействия с сохранением импульса)
Уравнения Менделеева – Клайперона: pV=nRT, где R=8,31 Дж/К
p=const (Изобара)
dA=pdV => A=p(V2-V1)
T=const (Изотерма)
![]()
δ-Q=0(Адиабата)
Система. Фаза. Компонент. Параметры системы. Правило фаз Гиббса.
Система – это тело или группа тел, находящихся во взаимодействии, которые мысленно выделены из окружающей среды. Различают гомогенные и гетерогенные системы. В первых из них нет поверхностей раздела, отделяющих друг от друга части системы, различающиеся по свойствам; во-вторых – есть такие.
У изолированных систем нет обмена энергией и веществом с окружающей средой; у закрытых систем нет только массообмена; у открытых систем есть и энерго, и массообмен с окружающей средой.
Фаза – совокупность всех гомогенных частей системы, одинаковых по составу и по всем химическим и физическим свойствам, не зависящим от количества вещества, и отграниченных друг от друга поверхностями раздела, на которых все свойства фазы резко, скачком, меняются.
Гомогенные системы – однофазны, гетерогенные системы – многофазны.
Параметры – величины, определяющие состояние системы. Интенсивные параметры не зависят от массы или числа частиц в системе (давление, температура и другие), экстенсивные – зависят (объем, энергия и другие).
Компоненты — независимые составляющие вещества системы, то есть индивидуальные химические вещества, которые необходимы и достаточны для составления данной термодинамической системы, допускают выделение из системы и независимое существование вне её. Изменения масс компонентов выражают все возможные изменения в химическом составе системы, а масса (количество вещества, число частиц) каждого вещества, выбранного в качестве компонента, не зависит от масс (количеств вещества, числа частиц) других компонентов.
Правило фаз Гиббса-показывает количественную зависимость между числом степеней свободы системы (С), числом независимых компонентов (К) и числом фаз (Ф).
Если на равновесие в системе влияет n внешних факторов, то правило фаз Гиббса запишется следующим образом:
С К Ф n (1)
При С = 0 в равновесии находится наибольшее число фаз. В общем случае, число фаз не может быть больше К + n (при этом С = 0):
Ф К n (2)
Правило фаз Гиббса для однокомпонентной системы:
в равновесной термодинамической системе, на которую из внешних факторов оказывают влияние только температура и давление, число термодинамических степеней свободы равно числу компонентов минус число фаз плюс два.
С К Ф 2 (3)
Для двухкомпонентной системы (К = 2) диаграммы рассматривают без учета газовой фазы, то есть считают, что р = const, а изменяющимся внешним фактором считают только температуру (n=1). Тогда правило фаз Гиббса запишется следующим образом: С 2Ф 1 3Ф (4)
Правилу фаз Гиббса не подчиняются коллоидные системы, в которых дисперсная фаза микроскопических размеров. Правило фаз не применимо к неравновесным метастабильным состояниям (переохлажденная вода, перегретый пар и т.д.).
dA=dU ![]() Дж/К
Дж/К
![]()
V=const (Изохора)
A=0
p=const T=const (Изотерма-Изобара)
![]()
![]() ,
где
,
где ![]()
![]() нтальпия.
Закон Гесса
нтальпия.
Закон Гесса
H=U+pV (Энтропия)
Идеальный газ: ![]() ,
где RT=2,47 кДж
,
где RT=2,47 кДж
Закон Гесса
В условиях постоянства давления или постоянства объема, теплота процесса становится функцией составляющей и не зависит от процесса
p=const
δQ=dU+pdV=d(U+pV) =dH, Q=H (становится функцией составляющей)
V=const
δQ=dU, Q=U
Следствия законов Гесса
Если реакция является суммой или разностью других реакций. По тепловой эффективности этой реакции будет суммой или разностью тепловых эффектов.
Стандартной теплотой i-го вещества
![]()
Зависимость теплового эффекта химической реакции от температуры (закон Кирхгоффа). Теплоемкость.
Теплоемкость
С – количество
теплоты, которое нужно передать, чтобы
нагреть 1 градус Цельсия. ![]() Дж/К
Дж/К
Закон Кирхгоффа
Пересчитывать тепловые эффекты с одной температуры на другую
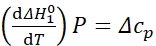 1з.к.г.
1з.к.г.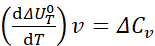 2з.к.г.
2з.к.г.
Температурный коэффициент теплового эффекта процесса равен изменению теплоемкости системы, происходящему в результате процесса
Проинтегрировав вышеприведенные диф. уравнения получим:
![]()
![]()
Второе начало термодинамики. Понятие об энтропии. Расчет энтропии. Изменение энтропии при химических процессах и фазовых переходах.
Невозможен самопроизвольный переход тепла от менее нагретого тела более нагретому.
Невозможно создание вечного двигателя 2-го рода (машины, которая периодически превращает тепло среды при постоянной температуре в работу.)
Термодинамический КПД:
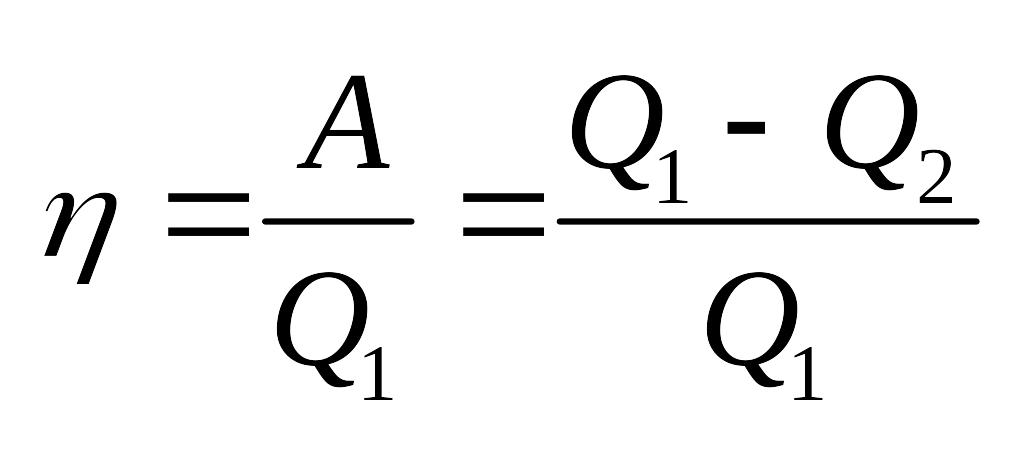 Для
изолированных систем критерием,
позволяющим судить о направлении
процессов и об условиях равновесия,
является функция-S-энтропия.
Для
изолированных систем критерием,
позволяющим судить о направлении
процессов и об условиях равновесия,
является функция-S-энтропия.
Процессы протекают в сторону увеличения энтропии. При равновесии энтропия достигает максимума. Обратное протекание процессов не может быть самопроизвольным – требуется затрата работы извне. Физический смысл функции состояния энтропии легче всего проиллюстрировать на примере кипения жидкости.
При нагреве: Т и U увеличиваются до тех пор, пока жидкость не закипит. При этом поглощается теплота испарения, затрачиваемая на увеличение беспорядка в системе. Таким образом, энтропия – мера упорядоченности состояния системы.
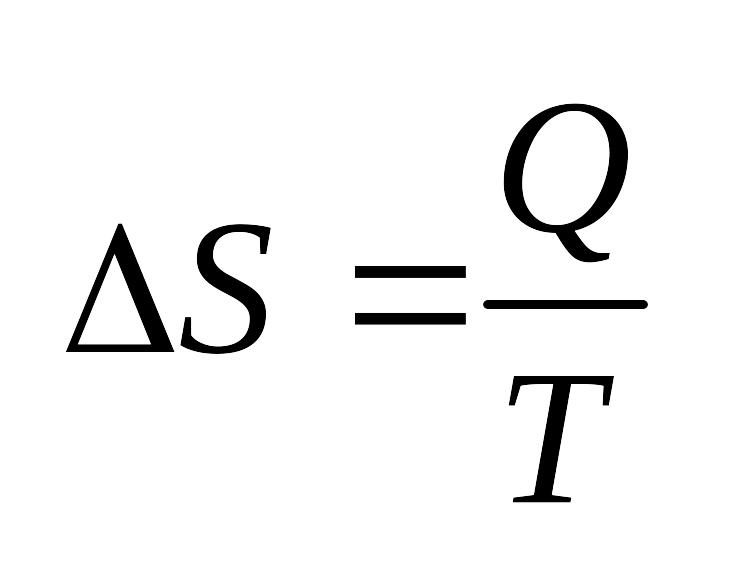 - 2е начало термодинамики
для обратимых процессов.
- 2е начало термодинамики
для обратимых процессов.
В изолированной системе
процессы самопроизвольные, протекают
в сторону увеличения энтропии![]()
В неизолированных–возможно
![]()
Примеры:![]()
![]()
![]()
![]()
Следует отметить, что фазовые переходы (испарение, сублимация и плавление) — это не только физические процессы изменения состояния, но и в значительной степени химические процессы разрыва и образования связей, сопровождающиеся изменением энтальпии и энтропии в системе.
Изменение энтропии в результате протекания химических реакций так же, как и в фазовых переходах, вычисляют как разность между энтропией конечного и начального состояний системы.
Объединенная формула первого и второго начала термодинамики. Свободная энергия Гиббса и Гельмгольца.
Теплота, подведенная к системе, расходуется на приращение внутренней энергии системы и на работу системы над окружающей средой.
![]()
Второй закон. Несколько формулировок, выберем эту:
в изолированных системах самопроизвольно
идут процессы, которые сопровождаются
возрастанием энтропии:![]()