Материал: ---Готовые билеты---
 Стандартный
водородный электрод
— электрод, использующийся в качестве
электрода сравнения при различных
электрохимических измерениях и в
гальванических элементах.
Стандартный
водородный электрод
— электрод, использующийся в качестве
электрода сравнения при различных
электрохимических измерениях и в
гальванических элементах.
Стандартный потенциал (нормальный потенциал), значение электродного потенциала, измеренное в стандартных условиях относительно выбранного электрода сравнения (стандартного электрода). Обычно стандартные потенциалы находят в условиях, когда термодинамич. активности а всех компонентов потенциалопределяющей р-ции, протекающей на исследуемом электроде, равны 1, а давление газа (для газовых электродов) равно 1,01 · 105 Па (1 атм).
Электрохимический ряд активности металлов — последовательность, в которой металлы расположены в порядке увеличения их стандартных электрохимических потенциалов φ⁰, отвечающих полуреакции восстановления катиона металла Meⁿ⁺: Meⁿ⁺ + nē → Me
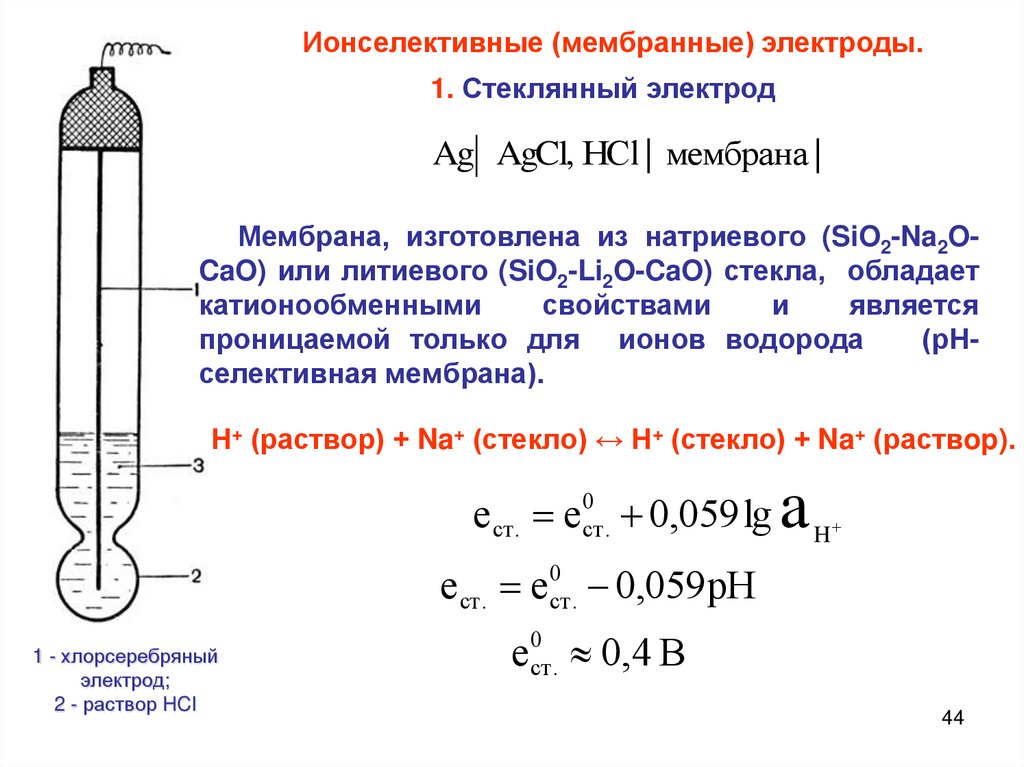
Типы электродов. Стеклянный электрод.
Различают три разновидности так называемых химических электродов. Это электроды первого, второго и третьего рода.
Электроды
первого рода
металлы, погруженные в растворы своих
солей: ![]()
![]() ,
т.е. потенциалопределяющими ионами
являются катионы металлов.
,
т.е. потенциалопределяющими ионами
являются катионы металлов.
Электроды
второго рода
металл погружен в насыщенный раствор
своей малорастворимой соли, к которой
добавлена другая соль с тем же анионом,
но хорошо растворимая, например, ![]() .
.
Процессы на электроде:
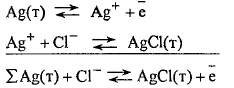
![]() ,
т.е. потенциалопределяющими ионами
являются анионы
,
т.е. потенциалопределяющими ионами
являются анионы ![]() .
Знак "минус" в формуле для
.
Знак "минус" в формуле для ![]() использован потому, что получение аниона
есть результат протекания процесса
восстановления.
использован потому, что получение аниона
есть результат протекания процесса
восстановления.
Электроды третьего рода (газовые электроды).
Известные водородный, кислородный и хлорный электроды.
Для
водородного электрода ![]() ,
,
![]() , т.е. потенциал газового электрода
зависит как от активности ионов в
растворе, так и от парциального давления
газа.
, т.е. потенциал газового электрода
зависит как от активности ионов в
растворе, так и от парциального давления
газа.
Электролиз. Последовательность разряда ионов на катоде и аноде.
Электролиз – ОВ процесс, протекающий в растворе или расплаве при прохождении постоянного электрического тока.
Электролиз HCl:
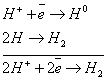
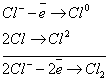
Последовательность катодных процессов. Процесс идет в направлении уменьшения потенциала.
![]()
Металлы можно разбить на 3 группы:
ВСЕГДА восстанавливается на катоде.
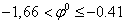 восстанавливаются вместе
с водородом
восстанавливаются вместе
с водородом
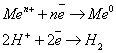
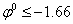 НИКОГДА невосстанавливаются.
НИКОГДА невосстанавливаются.
![]()
![]() в нейтральной или кислой
средах
в нейтральной или кислой
средах
Последовательность анодных процессов.
А) с растворимым анодом, окисляется сам анод
![]()
Б) угольные инертные электроды, процесс идет в порядке увеличение потенциала.
идет окисление бескислородных анионов кислот, за исключением Cl
кислородсодержащие ионы в водных растворах не окисляются (сильная ковалентная связь)
в случае отсутствия бескислородных ионов:
В щелочномрастворе
![]()
В кислой, нейтральнойсреде
![]()
Законы Фарадея. Выход по току
При электролизе данного электролита количество вещества, выделяющегося на электродах пропорционально количеству электричества.
При электролизе разных электролитов одинаковое количество электричества выделяет на электродах количество вещества, пропорциональное их эквиваленту.
При пропускании через электролит электричества в 1Ф=96493Кл на электродах выделяется 1 эквивалентная масса (1 моль-эквивалент)
![]() где
к – электрохимический эквивалент.
где
к – электрохимический эквивалент.
Выход по току:
![]()
Удельный расход энергии:
![]()
Коррозия металлов. Химическая и электрохимическая коррозия
Коррозия – это разрушение металла в результате его физико-химического взаимодействия с окружающей средой. При этом металлы окисляются и образуются продукты, состав которых зависит от условий коррозии.
Химическая коррозия характерна для сред, не проводящих электрический ток. При химической коррозии происходит прямое гетерогенное взаимодействие металла с окислителем окружающей среды.
По условиям протекания:
А) газовая коррозия – в газах и парах без конденсации влаги на поверхности металла, обычно при высоких температурах.
Б) коррозия в неэлектролитах – агрессивных органических жидкостях, таких как сернистая нефть и т.д.
Электрохимическая коррозия – характерна для сред, имеющих ионную проводимость. Процесс электрохимической коррозии включает анодное растворение металла и катодное восстановление окислителя. Может протекать в электролитах (водных растворах солей, кислот, щелочей, в морской воде), в атмосфере любого влажного газа, в почве.
Также существует коррозия за счет внешнего электрического тока, это особый вид электрохимической коррозии.
Основные методы борьбы с коррозией. Почвенная коррозия.
Коррозия – самопроизвольно протекающий процесс поверхностного окисления металла в результате его химического или электрохимического взаимодействия с окружающей средой.
В результате коррозии металл из свободного состояния переходит в связанное.
Методы борьбы различны:
Антикоррозийное легирование металла – введение в металл добавок, чтобы повысить стойкость основного металла.
Защитные покрытия (металлические и неметаллические).
Металлические наносятся под давлением сжатого воздуха. характерно покрытие листового материала тонким слоем другого материала.
Неметаллические – лаки ,краски, битум, солидол.
Ингибиторы коррозии- вещества, замедляющие процесс разрушения металла.
Пример:
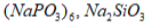
электрозащита- защищаемый металл приводят в контакт с менее благородным металлом (цинк или магний).
Поток электронов направляется к защищаемому металлу- этот вид защиты используется для магистральных труб, корпусов кораблей и т.д.
Почвенная коррозия — разрушение металла под воздействием агрессивной почвенной среды. Этому виду коррозионного разрушения подвергаются металлы и конструкции, находящиеся в почве, то есть различные подземные резервуары, трубопроводы, сваи, кабели и пр.
Кристаллическое состояние вещества. Химическая связь в кристаллах.
Твердые вещества могут находиться в аморфном или кристаллическом состояниях. Кристаллические структуры. Наименьшая структурная единица – элементарная ячейка. В зависимости от решеток и углов между характеристическими осями различают 7 основных видов (кубическая, ромбоэдрическая и пр.). Тип кристаллической системы определяется природой и размерами частиц, видом химических связей между ними, температурой и другими факторами. Многие соединения могут существовать в двух и более кристаллических структурах. Это явление – полиморфизм. Все кристаллы можно разделить по видам химической связи. Стоит отметить, что существуют кристаллы со смешанными связями.
Молекулярная связь. В узлах кристаллических решеток находятся молекулы, между которыми дейтсвуютвандерваальсовы силы, имеющие невысокую энергию.Для кристаллов с молекулярными связями характерны низкие температуры плавления и высокая сжимаемость.
Ковалентная связь. В узлах кристаллов располагаются атомы, образующие прочные ковалентные связи. Это обуславливает высокую энергию решетки. Кристаллы с ковалентной связью - диэлектрики или полупроводники. Типичными примеры: алмаз и кремний.
Ионная связь. Структурные единицы – положительно и отрицательно заряженные ионы, между которыми происходит электростатическое взаимодействие, характеризуемое высокой энергией. Кристаллы с ионной связью при низких температурах являются диэлектриками. При температурах близких к температуре плавления они становятся проводниками электричества.
Металлическая связь. Специфические свойства металлов (высокая проводимость, теплопроводность, ковкость, пластичность, металлический блеск) можно объяснить особым типом связи – металлическая.Во всех узлах кристаллической решётки расположены положительные ионы металла. Между ними беспорядочно движутся валентные электроны, отщепившиеся от атомов при образовании ионов. Эти электроны удерживают вместе положительные ионы, в противном случае решётка распалась бы под действием сил отталкивания между ионами.
Смешанная связь. Тот или иной вид связи встречается редко, обычно – наложение двух или более связей.
Сущность термографического анализа. Основные принципы построения диаграммы плавкости бинарных систем.
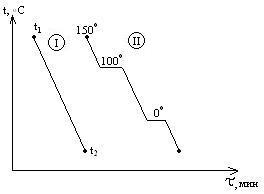 Термографический
анализ – кривые нагревания или кривые
охлаждения системы. Диаграммы плавкости
(частный вид диагарамм состояния) строят
исходя из кривых охлаждения, которые
изображаются в координатах: температура(Оу),
время(Ох). Рассмотрим кривые охлаждения
двух систем. Система I в
интервале t1-t2
не испытывает никаких фазовых превращений,
температура меняется монотонно. Кривая
II отвечают охлаждению
воды от 150 o C
(пар при атмосферном давлении) до 0 o
C и ниже. При 100 o
C наблюдается горизонтальный
участок, отвечающий фазовому переходу
– процессу конденсации пара, температура
поддерживается неизменной, пока не
исчезнет весь пар. Постоянство температуры
обеспечивается за счёт выделения в
процессе конденсации пара теплоты
испарения воды. От 100 o
C до 0 o
C наблюдается монотонный
ход кривой охлаждения – остывает жидкая
вода. При 0 o
C наблюдается второй
горизонтальный участок, отвечающий
фазовому переходу – процессу
кристаллизации. Температура поддерживается
постоянной за счет выделения теплоты
плавления.
Термографический
анализ – кривые нагревания или кривые
охлаждения системы. Диаграммы плавкости
(частный вид диагарамм состояния) строят
исходя из кривых охлаждения, которые
изображаются в координатах: температура(Оу),
время(Ох). Рассмотрим кривые охлаждения
двух систем. Система I в
интервале t1-t2
не испытывает никаких фазовых превращений,
температура меняется монотонно. Кривая
II отвечают охлаждению
воды от 150 o C
(пар при атмосферном давлении) до 0 o
C и ниже. При 100 o
C наблюдается горизонтальный
участок, отвечающий фазовому переходу
– процессу конденсации пара, температура
поддерживается неизменной, пока не
исчезнет весь пар. Постоянство температуры
обеспечивается за счёт выделения в
процессе конденсации пара теплоты
испарения воды. От 100 o
C до 0 o
C наблюдается монотонный
ход кривой охлаждения – остывает жидкая
вода. При 0 o
C наблюдается второй
горизонтальный участок, отвечающий
фазовому переходу – процессу
кристаллизации. Температура поддерживается
постоянной за счет выделения теплоты
плавления.
Р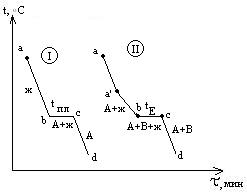 ассмотрим
кривые охлаждения чистого
металла (I) и сплава с так
называемой эвтектикой (II).
На кривой охлаждения (I)
чистого металла А наблюдается одна
площадка bc, отвечающая
процессу кристаллизации металла. При
tпл в
равновесии находятся жидкая и твердая
фазы одинакового состава. Образование
твердой фазы сопровождается выделением
теплоты плавления.
ассмотрим
кривые охлаждения чистого
металла (I) и сплава с так
называемой эвтектикой (II).
На кривой охлаждения (I)
чистого металла А наблюдается одна
площадка bc, отвечающая
процессу кристаллизации металла. При
tпл в
равновесии находятся жидкая и твердая
фазы одинакового состава. Образование
твердой фазы сопровождается выделением
теплоты плавления.
Кривая II отвечает охлаждению сплава А-В. От “а” до “a’ “ температура меняется монотонно, остывает жидкая фаза. При достижении точки a’ из жидкой фазы начинают выпадать кристаллы А – одного из компонентов сплава, при этом жидкая фаза за счет этого начнет обогащаться компонентом В. Таким образом, в интервале a’-b в равновесии находятся жидкая и твердая фазы различного состава, площадки на кривой охлаждения не наблюдается. За счет выделения при кристаллизации А теплоты плавления этого компонента темп охлаждения сплава замедляется, и на кривой наблюдается перелом. Выпадение кристаллов А продолжается до тех пор, пока жидкая фаза не достигнет так называемого “эвтектического состава”. Основной особенностью эвтектического сплава является то, что он кристаллизуется подобно чистому компоненту – на кривой охлаждения наблюдается площадка.
Из жидкой фазы одновременно выпадают кристаллы А и В и, таким образом при tЕ (отрезок bc) в равновесии находятся жидкая и твердая фазы одинакового состава. Отрезок cd отвечают охлаждению твердого сплава.
Остановки в падении температуры могут наблюдаться и на кривой охлаждения уже твердого металла, указываю на переходы металла из одной аллотропной формы в другую
Диаграмма состояния однокомпонентной системы на примере воды.
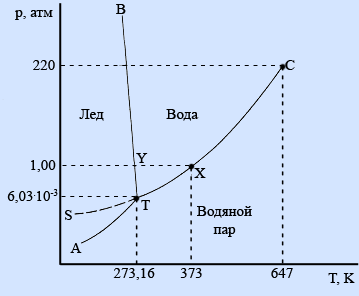
Области фазовой диаграммы, ограниченные кривыми, соответствуют тем условиям (температурам и давлениям), при которых устойчива только одна фаза вещества. Например, при любых значениях температуры и давления, которые соответствуют точкам диаграммы, ограниченным кривыми ВТ и ТС, вода существует в жидком состоянии. При любых температуре и давлении, соответствующих точкам диаграммы, которые расположены ниже кривых АТ и ТС, вода существует в парообразном состоянии.
Кривые фазовой диаграммы соответствуют условиям, при которых какие-либо две фазы находятся в равновесии друг с другом. Например, при температурах и давлениях, соответствующих точкам кривой ТС, вода и ее пар находятся в равновесии. Это и есть кривая давления пара воды. В точке Х на этой кривой жидкая вода и пар находятся в равновесии при температуре 373 К (100°С) и давлении 1 атм (101,325 кПа); точка Х представляет собой точку кипения воды при давлении 1 атм.