Материал: ---Готовые билеты---
Гидролиз солей. Константа и степень гидролиза.
Гидролиз солей – это процесс обменного разложения воды и растворенной в ней соли – электролита, приводящий к образованию малодиссоциирующего вещества. Гидролиз является частным случаем сольволиза – обменного разложения растворенного вещества и растворителя.
Характеризовать гидролиз количественно позволяют такие величины, как
Степень гидролиза и константа гидролиза.
Степень гидролиза — это соотношение количества подвергающейся гидролизу соли nгидр и общего количества растворенной соли nобщ. Обычно, ее обозначают через hгидр (или α ):
hгидр = (nгидр/nобщ)·100 %
Величина hгидр увеличивается с уменьшением силы образующих соль кислоты или основания.
Константа гидролиза
Представим в общем виде процесс гидролиза соли, в котором в роли соли выступает – МА, а НА и МОН — соответственно, кислота и основание, которые образуют данную соль:
MA + H2O ↔ HA + MOH
Применив закон действующих масс, запишем константу, соответствующую этому равновесию:
K = [HA]·[MOH]/[MA]·[H2O]
Известно, что концентрация воды в разбавленных растворах, имеет практически постоянное значение, поэтому ее можно включить в константу
K·[H2O]= Kг,
тогда для константы гидролиза соли Kг будет иметь такой вид:
Kг = [HA]·[MOH]/[MA]
По величине константы гидролиза можно судить о полноте гидролиза: чем больше ее значение, тем в большей мере протекает гидролиз.
Константа и степень гидролиза связаны соотношением:
Kг = С·h2/(1- h), моль/л
Где С – концентрация соли в растворе, h- степень гидролиза
Это выражение можно упростить, т.к. обычно h˂˂1, тогда
Kг = С·h2
Зная, константу гидролиза, можно определить pH среды:
Kг = [HA]·[MOH]/[MA]
Концентрация образовавшейся кислоты равна концентрации гидроксид ионов, тогда
Kг = [OH—]2/[MA]
Используя это выражение можно вычислить pH раствора
[OH—] = (Kг·[MA])1/2 моль/л
[H+] = 10-14/[OH—] моль/л
pH = -lg[H+]
Окислительно-восстановительные реакции. Ионно-электродный метод подбора коэффициентов в окислительно-восстановительных реакциях.
Окислительно -восстановительные реакции (ОВР) - реакции, протекающие с изменением степени окисления одного или нескольких элементов.
Порядок действий при подборе коэффициентов методом полуреакций:
Записывают схему реакции в молекулярной и ионно-молекулярной формах и определяют ионы и молекулы, которые изменяют степень окисления.
Определяют среду, в которой протекает реакция (Н+ - кислая; ОН- - щелочная; Н2О – нейтральная)
Составляют ионно-молекулярное уравнение каждой полуреакции и уравнивают число атомов всех элементов.
Количество атомов кислорода уравнивают, используя молекулы воды или ионы ОН-.
Если исходный ион или молекула содержат больше атомов кислорода, чем продукт реакции, то
избыток атомов кислорода в кислой среде связывается ионами Н+ в молекулы воды
в нейтральной и щелочной среде избыток атомов кислорода связывают молекулами воды в группы ОН-
Если исходный ион или молекула содержит меньшее число атомов кислорода, чем продукт реакции, то
недостаток атомов кислорода в кислых и нейтральных растворах компенсируется за счёт молекул воды
в щелочных растворах – за счёт ионов ОН-.
Составляют электронно-ионные уравнения полуреакций.
Для этого в левую часть каждой полуреакции добавляют (или вычитают) электроны с таким расчётом, чтобы суммарный заряд в левой и правой частях уравнений стал одинаковым. Умножаем полученные уравнения на наименьшие множители, для баланса по электронам.
Суммируют полученные электронно-ионные уравнения. Сокращают подобные члены и получают ионно-молекулярное уравнение ОВР
По полученному ионно-молекулярному уравнению составляют молекулярное уравнение.
примеры по ссылке
Возникновение скачка потенциала на границе раздела "металл-раствор".
Если пластину любого металла погрузить в воду или раствор электролита, содержащий ионы этого металла, то небольшая часть металла перейдет в раствор, в форме положительно заряженных ионов, а сама пластина, концентрируя на себе избыток свободных электронов, приобретает отрицательный заряд. Такому переходу содействует связывание ионов металла с молекулами воды (растворителя).В итоге устанавливается равновесие
Me ↔ Me2+ + 2e
Me2+ + m H2O ↔ Me2+ · m H2O
Me + m H2O ↔ Me2+ · m H2O +2e
Положительно заряженные ионы Me+2, перешедшие в раствор, концентрируются у поверхности пластины, приобретающей отрицательный заряд, в результате возникает двойной электрический слой (ДЭС), обусловливающий резкий скачок электрического потенциала на границе металл - раствор электролита.
Эту разность электрических потенциалов или скачок потенциала на границе металл-раствор электролита называют электродным потенциалом.
Величина электродного потенциала зависит от природы металла, концентрации, точнее активности ионов металла в растворе и температуры.
Математически эта зависимость выражается уравнением В.Г.Нернста (1888).
EMe = E0Me + (R ∙T/n · F) / ln аMen+,
а в случае разбавленных растворов полностью диссоциирующих солей данного металла
ЕMe = E0Me + (R∙T/n · F) / ln [Men+ ],
где E0Me- стандартный электродный потенциал, R- универсальная газовая постоянная, F- постоянная Фарадея, n - заряд иона металла, аMe,n+ , [ Men+] – активность или концентрация ионов металла (моль\л)
После перехода от натурального логарифма к десятичному и подстановки значений
R=8,314Дж\моль· К
T=298,15 К
F=96500 Кл, точнее 96487 Кл уравнение примет вид EMe = E0Me + 0,0592/n ·lg [Men+]
Равновесный электродный потенциал.
Потенциал, отвечающий состоянию равновесия, когда скорость перехода ионов в раствор равна скорости их осаждения – равновесный потенциал. Для всех металлов, погружаемых в чистую воду, качественно наблюдается одинаковая картина: металл заряжается отрицательно, прилегающий слой жидкости – положительно. Данный скачок можно
охарактеризовать реакцией:
![]() Рассмотрим
погружение в раствор активного и
неактивного металла.
Рассмотрим
погружение в раствор активного и
неактивного металла.
Активный металл посылает большое число ионов в раствор, равновесная концентрация его ионов трудно достижима => металл будет заряжаться отрицательно.
Равновесная концентрация очень мала => электроду сообщается положительный заряд, а оставшиеся анионы создают отрицательный заряд у прилегающего слоя.
Медно-цинковый гальванический элемент Якоби-Даниеля. Процессы на электродах. Понятие об эдс.
Гальванической элемент илюбое устройство, дающее возможность получать электрический ток за счёт проведения той или иной химической реакции.
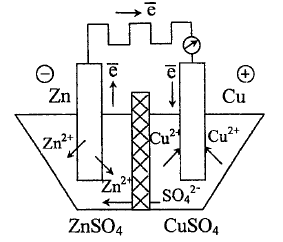 Рассмотрим
систему, в которой медь и цинк в воде
пластинок помещены в растворы своих
солей, разделённых пористой керамической
перегородкой
диафрагмой.
При разомкнутой внешней цепи на обоих
электродах устанавливаются равновесные
потенциалы, различающиеся по величине
и по знаку. При замыкании внешней цепи
на некоторое сопротивление электроны
от цинкового электрода получают
возможность перемещаться по внешнему
проводнику к медному электроду.
Рассмотрим
систему, в которой медь и цинк в воде
пластинок помещены в растворы своих
солей, разделённых пористой керамической
перегородкой
диафрагмой.
При разомкнутой внешней цепи на обоих
электродах устанавливаются равновесные
потенциалы, различающиеся по величине
и по знаку. При замыкании внешней цепи
на некоторое сопротивление электроны
от цинкового электрода получают
возможность перемещаться по внешнему
проводнику к медному электроду.
Равновесие
![]() на цинковом электроде нарушается, и для
пополнения убыли электронов получает
развитие процесс:
на цинковом электроде нарушается, и для
пополнения убыли электронов получает
развитие процесс: ![]() ,
при этом в раствор переходит ионы
,
при этом в раствор переходит ионы ![]() .
.
Электроны,
проходящие к медному электроду,
восстанавливают ионы ![]() по
реакции:
по
реакции: ![]() Равновесие нарушается и на медном
электроде, поэтому из раствора к медному
электроду поступают все новые порции
.
Равновесие нарушается и на медном
электроде, поэтому из раствора к медному
электроду поступают все новые порции
.
Таким образом, в системе получают развитие два территориально разобщённых процесса:
на
отрицательном электроде - ![]() (окисление);
(окисление);
на
положительном электроде - ![]() (восстановление).
(восстановление).
Суммарная
реакция ![]() ,
а в молекулярной форме:
,
а в молекулярной форме: ![]()
Гальванический элемент, основанный на такой реакции, был предложен русским учёным Б.С.Якоби. Создателем этого элемента является также и английский учёный Даниэль.
Причина возникновения электрического тока - разность потенциалов, возникающих на пластинках.
Гальваническая цепь последовательная совокупность всех скачков потенциала на различных поверхностях раздела, отвечающих данному гальваническому элементу.
Гальваническая цепь медно-цинкового элемента записывается следующим образом:
![]()
Граница "электрод-электролит" обозначается одной вертикальной чертой, двумя обозначается граница двух электролитов, на которой устранён диффузионный потенциал. Электроны перемещаются по внешнему проводнику слева направо, и в том же направлении переносится ионами положительное электричество внутри элемента. При такой записи гальванической цепи ЭДС элемента всегда считается положительной, поскольку эта запись отвечает направлению самопроизвольного протекания реакции, сопровождающегося уменьшением изобарно-изотермического потенциала.
![]()
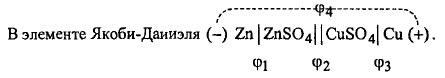
![]() - скачки потенциалов на границах
"электрод-электролит",
- скачки потенциалов на границах
"электрод-электролит", ![]() - на границе двух электролитов,
- на границе двух электролитов, ![]() - на границе двух металлов. Величиной
можно пренебречь.
- на границе двух металлов. Величиной
можно пренебречь.
Зависимость эдс гальванического элемента от природы реагирующих веществ, температуры и концентрации. Стандартная эдс.
ЭДС гальванического элемента зависит от природы реагирующих веществ, их концентрации и температуры.
Влияние природы реагирующих веществ
Пусть в гальваническом элемента протекает реакция 1:
![]() .
.
![]() .
.
Здесь
![]() - максимальная
полезная работа реакции.
- максимальная
полезная работа реакции.
При протекании реакции 2 имеем:
![]() .
.
Влияние температуры на ЭДС элемента
Уравнение
Гиббса-Гельмгольца: ![]() .
сделаем подстановки в это уравнение:
.
сделаем подстановки в это уравнение:
![]() ,
,
![]()
![]() .
Обозначим второе слагаемое через
.
Обозначим второе слагаемое через ![]() , получаем
, получаем ![]() ,
поскольку
,
поскольку ![]() .
.
![]() - теплота реакции, которая выделяется
или поглощается при её необратимом
проведении.
- теплота реакции, которая выделяется
или поглощается при её необратимом
проведении.
q характеризует связанную энергию, определяет количество теплоты, неизбежно выделяющейся или поглощающейся при обратимой работе элемента.
Поскольку
![]() Таким образом, определив температурный
градиент ЭДС, можно вычислить изменение
энтропии для реакции, протекающей в
элементе.
Таким образом, определив температурный
градиент ЭДС, можно вычислить изменение
энтропии для реакции, протекающей в
элементе.
Зависимость ЭДС от концентрации реагирующих веществ
Пусть в гальваническом элементе протекает реакция A + B = 2D.
![]() - уравнение
Нернста.
- уравнение
Нернста.
Стандартный водородный электрод. Формула Нерста. Стандартный потенциал. Ряд напряжений металла.