Материал: ---Готовые билеты---
Длина связи - межъядерное расстояние в невозбуждённой молекуле (обычно 1-2 Ангстрема, 1А=10-8 см)
Энергия связи – энергия, выделяющаяся при образовании данного вида связи (150-1000 кДж/моль).
Типы химических связей:
Ковалентная неполярная связь химическая связь между атомами неметаллов с равными или близкими значениями электроотрицательности. При этом общая электронная пара одинаково принадлежит обоим атомам, смещения электронной плотности не наблюдается.
Связь, образованная элементами-неметаллами с разной электроотрицательностью, называется ковалентной полярной. При этом происходит смещение электронной плотности в сторону более электроотрицательного элемента.
Ионная связь образована за счет сил электростатистического притяжения между разноименно заряженными ионами катионами и анионами.
Металлическая связь химическая связь между атомами в металлическом кристалле, возникающая за счёт перекрытия (обобществления) их валентных электронов.
Водородная связь – связь между положительно заряженным атомом водорода одной молекулы и отрицательно заряженным атомои другой молекулы.
Механизм возникновения водородной связи – частично электростатический и частично донорно-акцепторный.
Характерной чертой водородной связи является расстояние между атомом водорода и другим атомом, её образующим. Оно должно быть меньше, чем сумма радиусов этих атомов.
Водородная связь подразделяется:
Межмолекулярная водородная связь образуется между молекулами веществ, в состав которых входят водород и сильно электроотрицательный элемент – фтор, кислород, азот, хлор, сера. Сильно смещенная общая электронная пара от водорода к атому отрицательно заряженного элемента, при этом положительный заряд водорода сконцентрирован в малом объеме, приводит взаимодействие протона с неподеленной электронной парой другого атома или иона, обобществляя её.
Внутримолекулярная водородная связь присутствует в многоатомных спиртах, углеводах, белках и других органических веществах.
Вещества с водородной связь имеют молекулярные кристаллические решетки, в узлах которой находятся молекулы.
Несмотря на свою электронейтральность, молекулы способны взаимодействовать между собой. Это взаимодействие называют межмолекулярным или ван-дер-ваальсовым.
Различают три составляющие межмолекулярного взаимодействия:
взаимодействие между полярными молекулами (диполями). Это взаимодействие называют ориентационным или диполь-дипольным;
индукционное взаимодействие, которое реализуется между полярной и неполярной молекулами вследствие того, что в неполярной молекуле под действием электрического поля полярной молекулы также возникает (индуцируется) диполь;
дисперсионное взаимодействие; это взаимодействие так называемых мгновенных диполей, которые возникают в неполярных молекулах вследствие флуктуации (колебаний) электронной плотности (в какой-то момент времени в одной области атома или молекулы электронная плотность увеличивается, что приводит к появлению мгновенных диполей не только в данной, но и в соседних молекулах). Такое взаимодействие имеет место и между полярными молекулами, но в случае неполярных молекул — это единственный вид межмолекулярного взаимодействия.
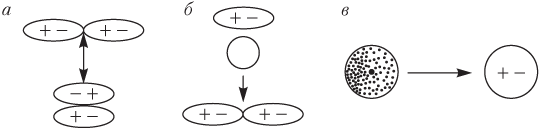
Ковалентная (атомная) связь. Метод валентных связей. Возбужденные состояния атомов.
Ковалентная связь – наиболее общий вид химической связи, возникающий за счет обобществления электронной пары посредством обменного механизма, когда каждый из взаимодействующих атомов поставляет по одному электрону. Классический пример неполярной ковалентной связи (разность электроотрицательностей равна нулю) наблюдается у гомоядерных молекул: H–H, F–F. Если соединение образуется между двумя различными неметаллами, то такое соединение называется ковалентной полярной связью. Если атомы, образующие простую ковалентную связь, одинаковы, то истинные заряды атомов в молекуле также одинаковы, поскольку атомы, образующие связь, в равной степени владеют обобществлённой электронной парой. Такая связь называется неполярной ковалентной связью. Метод объяснения механизма возникновения ковалентной связи: метод валентных связей (МВС)
В основе МВС лежит 3 положения:
1.Химическая связь образуется двумя электронами с противоположно направленными спинами. При этом имеет место взаимное перекрытие электронных орбиталей. Между атомами возникает зона повышенной электронной плотности, к которой притягиваются ядра с остальными электронами.
Связь имеет ориентацию в направлении, обеспечивающем максимально возможное перекрывание орбиталей.
Чем больше взаимное перекрывание электронных орбиталей, тем прочнее связь. Возбужденное состояние атома энергетически нестабильное состояние, в которое атом переходит, получая энергию извне. В возбужденном состоянии атом может пребывать лишь короткое время. Возбужденный атом, отдавая энергию, возвращается в основное состояние.
Валентность и степень окисления. Способы определения степени окисления. Основные окислители и восстановители. Уравнять окислительно-восстановительную реакцию ионно-электронным методом.
Валентность – это способность атомов присоединять к себе определенное число других атомов.
Валентность – определяется номером группы (число химических связей в структурной формуле вещества).
Степень окисления – это условный заряд, который получает атом в результате полной отдачи (принятия) электронов, исходя из условия, что все связи в соединении ионные.
F0 + 1ē → F-1 (нейтральный атом принимает один отрицательный электрон и приобретает степень окисления «-1», превращаясь в отрицательно заряженный ион - анион)
Правила определения степени окисления атома в периодической системе химических элементов Д.И. Менделеева:
Водород обычно проявляет степень окисления (СО) +1 (исключение, соединения с металлами (гидриды) – у водорода СО равна (-1) Me+nHn-1)
Кислород обычно проявляет СО -2 (исключения: О+2F2, H2O2-1 – перекись водорода)
Металлы проявляют только +n положительную СО
Фтор проявляет всегда СО равную -1 (F-1)
Для элементов главных подгрупп:
Высшая СО (+) = номеру группы Nгруппы
Низшая СО (-) = Nгруппы–8
Правила определения степени окисления атома в соединении:
I. Степень окисления свободных атомов и атомов в молекулах простых веществ равна нулю - Na0, P40, O20
II. В сложном веществе алгебраическая сумма СО всех атомов с учётом их индексов равна нулю = 0, а в сложном ионе его заряду.
Основные восстановители:
металлы;
водород H2;
уголь C;
оксид углерода(II) CO;
сероводород H2S, сульфиды K2S;
Основные окислители:
галогены F2, Cl2;
кислород O2, озон O3;
соединения марганца KMnO4;
азотная кислота HNO3 и её соли KNO3;
концентрирована серная кислота H2SO4;
ионы металло
Направленность ковалентной связи. Σ и π-связи. Гибридизация атомных орбиталей.
Направленность ковалентной связи возникает между элементами с одинаковым или близким значениями энергии сродства к электрону. Перекрывание облаков при обр. ков. св. возможно только при определенной их взаимной ориентации в пространстве – отсюда направленность связей, приводящая к определенной форме молекул. При этом область перекрывания располагается определенным образом по отношению к взаимодействующим атомам.
Молекулы типа AA, BB, АВ. Характерны для водорода, галогенов и соед. «галоген+водород». Молекулы имеют линейчатую структуру. Хим. св. действует по кратчайшему расстоянию(сигма-связь).
Молекулы типа A2B. Характерны для соед., образованных эл. главной подгруппы 6-ой группы: Н2О, Н2S. H2O-валентный угол 105.
Молекулы типаA3B. Характерны для соед., образованных эл. гл. подгр.5-й группы (N, P, As, Sb, Bi). Молекула аммиака (NH3) имеет форму пирамиды с треугольником в основании.
Молекулы типа A4B. Главной подгруппы 4-й гр. (Si,C,Ge,Sn, Pb) Молекула метана имеет форму тетраэдра (по вершинам – атомы водорода, атом углерода –в центре).
Молекулы типа AB3. Гл.подгруппа 3-ей гр.(B,Al,Ga,In, Tl). Молекула BCl3 имеет вид равностороннего треугольника.
Молекулы типа AB2. Характерны для некоторых соед., образованных элемкнтами гл. подгруппы 2 гр. ВеCl2 (линейная структура, угол–180).
Если в молекуле имеется кратная связь между атомами (2-ная или 3-ная), то только одна связь является прочной-пи-связью. Остальные–сигма-связи. Пример. Рассм. молекулу этилена (С2Н4). неполная гибридизация
![]()
![]()
Между атомами углерода одна из связей «пи». Все остальне– «сигма».
Полярность связи. Ионная (электронная) связь. Полярность молекул и их дипольный момент.
Ионная (электронная связь). В случае возникновения ионной связи между атомами или группами атомов преобладает электростатическое взаимодействие. Оно возникает между атомами элементов, значительно отличающихся по величине электроотрицательности. Элементы, входящие в состав ионного соединения, всегда существуют в виде ионов, а не нейтральных атомов. Также нужно отметить, что полного разделения зарядов нет и имеет место частичная ковалентность. Валентность в ионных соединениях равна числу электронов, отданных или присоединённых атомом при превращении его в ион. Ионы проводят эл. ток в растворах и расплавах и являются проводниками второго рода. Ионная (электронная связь) Ионы это заряженные частицы, в которые превращаются атомы в результате отдачи или присоединения электронов. Химическая связь между ионами, осуществляемая за счет электростатического притяжения, называется ионной связью.
Предположим, что мы имеем соединение
АB. Оба элемента с большими значениями
электроотрицательности (![]() ).=>
общая электронная пара в молекуле
смещена от атома B к атому А.
Электронейтральность нарушается, в
молекуле появляется положительное (B)
и отрицательный (A) полюса. Такая система
называется диполь–полярная
молекула (система из 2-х разноименных,
одинаковых по величине зарядов,
находящихся на малом расстоянии).
Ковалентная связь–полярная. Основная
характеристика диполя–дипольный
момент.
).=>
общая электронная пара в молекуле
смещена от атома B к атому А.
Электронейтральность нарушается, в
молекуле появляется положительное (B)
и отрицательный (A) полюса. Такая система
называется диполь–полярная
молекула (система из 2-х разноименных,
одинаковых по величине зарядов,
находящихся на малом расстоянии).
Ковалентная связь–полярная. Основная
характеристика диполя–дипольный
момент.
![]() ,
, ![]() –напряженность поля, созд. диполем.
l–плечо диполя.
–напряженность поля, созд. диполем.
l–плечо диполя.
Полярность связи– вектор, направленный от отрицательного полюса к положительному, происходит взаимное уничтожение векторов.