Материал: ---Готовые билеты---
Второе начало термодинамики. Понятие об энтропии. Расчет энтропии. Изменение энтропии при химических процессах и фазовых переходах.
Невозможен самопроизвольный переход тепла от менее нагретого тела более нагретому.
Невозможно создание вечного двигателя 2-го рода (машины, которая периодически превращает тепло среды при постоянной температуре в работу.)
Термодинамический КПД:
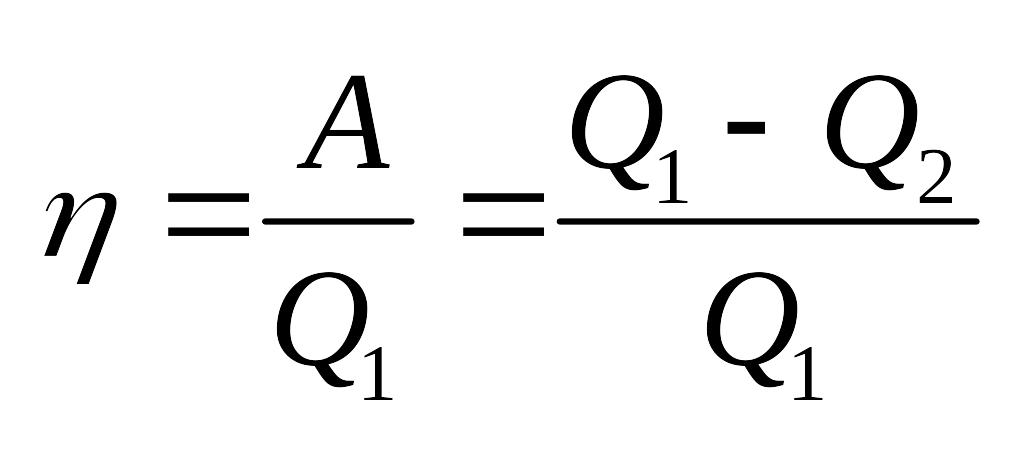 Для
изолированных систем критерием,
позволяющим судить о направлении
процессов и об условиях равновесия,
является функция-S-энтропия.
Для
изолированных систем критерием,
позволяющим судить о направлении
процессов и об условиях равновесия,
является функция-S-энтропия.
Процессы протекают в сторону увеличения энтропии. При равновесии энтропия достигает максимума. Обратное протекание процессов не может быть самопроизвольным – требуется затрата работы извне. Физический смысл функции состояния энтропии легче всего проиллюстрировать на примере кипения жидкости.
При нагреве: Т и U увеличиваются до тех пор, пока жидкость не закипит. При этом поглощается теплота испарения, затрачиваемая на увеличение беспорядка в системе. Таким образом, энтропия – мера упорядоченности состояния системы.
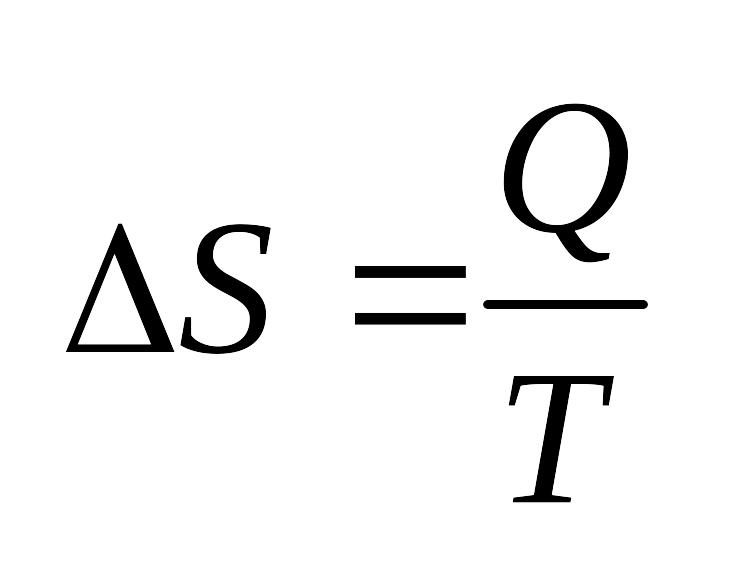 - 2е начало термодинамики
для обратимых процессов.
- 2е начало термодинамики
для обратимых процессов.
В изолированной системе
процессы самопроизвольные, протекают
в сторону увеличения энтропии![]()
В неизолированных–возможно
![]()
Примеры:![]()
![]()
![]()
![]()
Следует отметить, что фазовые переходы (испарение, сублимация и плавление) — это не только физические процессы изменения состояния, но и в значительной степени химические процессы разрыва и образования связей, сопровождающиеся изменением энтальпии и энтропии в системе.
Изменение энтропии в результате протекания химических реакций так же, как и в фазовых переходах, вычисляют как разность между энтропией конечного и начального состояний системы.
Объединенная формула первого и второго начала термодинамики. Свободная энергия Гиббса и Гельмгольца.
Теплота, подведенная к системе, расходуется на приращение внутренней энергии системы и на работу системы над окружающей средой.
![]()
Второй закон. Несколько формулировок, выберем эту:
в изолированных системах самопроизвольно
идут процессы, которые сопровождаются
возрастанием энтропии:![]()
Энтропия – термодинамическая функция, характеризующая меру неупорядоченности состояния системы. Она используется для суждения о направлении самопроизвольно протекающих процессах.
Обобщенный закон. Для каждой изолированной термодинамической системы существует состояние термодинамического равновесия, которого она при фиксированных внешних условиях с течением времени самопроизвольно достигает.
Энергия Гельмгольца. Максимальная
работа, которую может совершить система
при равновесном проведении процесса,
равна изменению энергии Гельмгольца
реакции
![]()
![]() Энергия
Гельмгольца равна
Энергия
Гельмгольца равна
![]() называют связанной энергией.
Она характеризует предел самопроизвольного
течения реакции, которое возможно при
называют связанной энергией.
Она характеризует предел самопроизвольного
течения реакции, которое возможно при
![]()
Энергия Гиббса. Энтальпийный
и энтропийный факторы, характеризующие
процессы, объединены функцией - энергия
Гиббса.![]()
Поскольку энергию Гиббса можно превратить
в работу, то ее называют свободной
энергией.
![]() Химическая
реакция возможна, если энергия Гиббса
уменьшается (<0).
Химическая
реакция возможна, если энергия Гиббса
уменьшается (<0).
Третий закон термодинамики. Постулат Планка.
Третий закон термодинамики:
При нулевой абсолютной температуре энтропия любых веществ, находящихся в равновесном состоянии, имеет одинаковое значение, не зависящее от фазы вещества.
В изотермических
процессах, происходящих при ![]() ,
энтропия не зависит ни от обобщенных
сил, ни от обобщенных координат.
,
энтропия не зависит ни от обобщенных
сил, ни от обобщенных координат.
Поскольку на основе второго начала термодинамики можно определить только изменение энтропии:
![]()
М. Планк показал, что третий закон термодинамики равносилен следующему условию
Постулат Планка
Энтропия всех тел в состоянии равновесия стремится к нулю по мере приближения температуры к абсолютному нулю (т.е. константу интегрирования S0 можно за ноль)
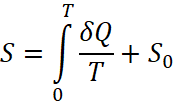
Следствия:
Недостижимость абсолютного нуля температур
Абсолютного нуля температуры нельзя достичь ни в каком конечном процессе, связанном с изменением энтропии, к нему можно лишь асимптотически приближаться
Поведение термодинамических коэффициентов:
При ![]() должны стремиться к нулю теплоёмкости
при постоянном давлении и при постоянном
объёме, коэффициенты теплового расширения
и некоторые аналогичные величины.
должны стремиться к нулю теплоёмкости
при постоянном давлении и при постоянном
объёме, коэффициенты теплового расширения
и некоторые аналогичные величины.
Условия самопроизвольного протекания химических реакций.
В химических системах вещества стремятся к минимуму внутренней энергии. Экзотермические реакции протекают самопроизвольно, так как вещества при их окончании достигают своего минимума внутренней энергии. Но также самопроизвольно протекают и эндотермические реакции — это растворение солей. Макросостояние системы тем более вероятно, чем большим числом микросостояний оно может быть описано.
Условия самопроизвольного протекания реакций:
1. Стремление системы к достижению минимального значения внутренней энергии
2. Стремление системы к более вероятному своему состоянию.
Но часто происходит столкновение этих двух определяющих факторов, и возникает состояние, называемое химическим равновесием. Функция, которая учитывает оба этих фактора – энергия Гиббса. Самопроизвольно протекают те процессы, энергия Гиббса которых равна отрицательному значению. Если температура мала, то энтальпия равна энергии Гиббса и самопроизвольно протекают экзотермические реакции. Если высокая температура, то отрицательное значение имеет энергия Гиббса и реакции протекают самопроизвольно. Необратимые реакции протекают до полного израсходования одного из реагентов. Обратимые протекают во взаимопротивоположных направлениях. В состоянии химического равновесия система достигает своего минимального значения энергии и энергия Гиббса, как и константа химического равновесия, равна нулю.
Константа химического равновесия. Расчет кр и кс.
Рассмотрим гомогенную химическую
реакцию:![]() Реакции
протекают до полного исчезновения
исходных веществ, а останавливаются
при достижении определенного состояния
равновесия Условия химического
равновесия:
Реакции
протекают до полного исчезновения
исходных веществ, а останавливаются
при достижении определенного состояния
равновесия Условия химического
равновесия:
![]()
Равновесные давления участников реакции:
![]()
Согласно закону действующих масс:
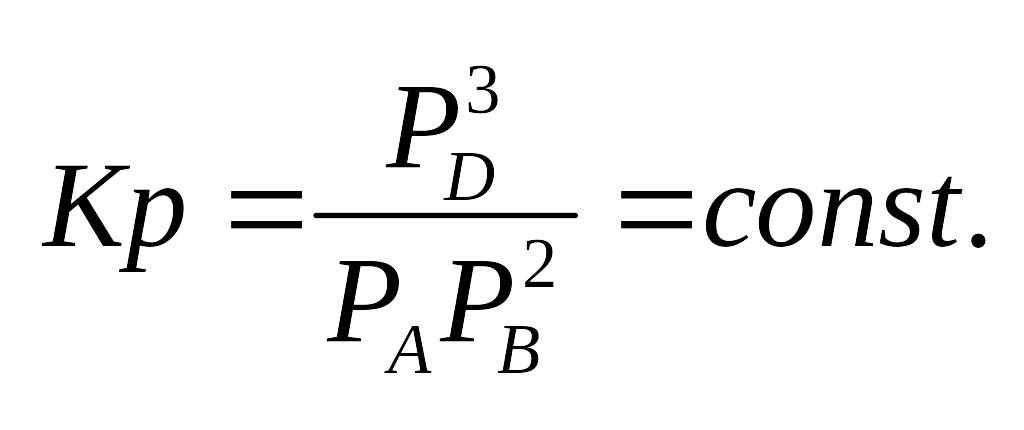
![]() константа равн- я, выраженная через
парциальные давления.
константа равн- я, выраженная через
парциальные давления.
Размерность
![]()
![]() изменение числа молей при протекании
реакции. При написании константы
равновесия гетерогенных реакции
учитываются парциальные давления только
газообразных участников реакций,
поскольку давления пара конденсированных
фаз малы по сравнению с газообразными
компонентами.
изменение числа молей при протекании
реакции. При написании константы
равновесия гетерогенных реакции
учитываются парциальные давления только
газообразных участников реакций,
поскольку давления пара конденсированных
фаз малы по сравнению с газообразными
компонентами.
Пример.
![]()
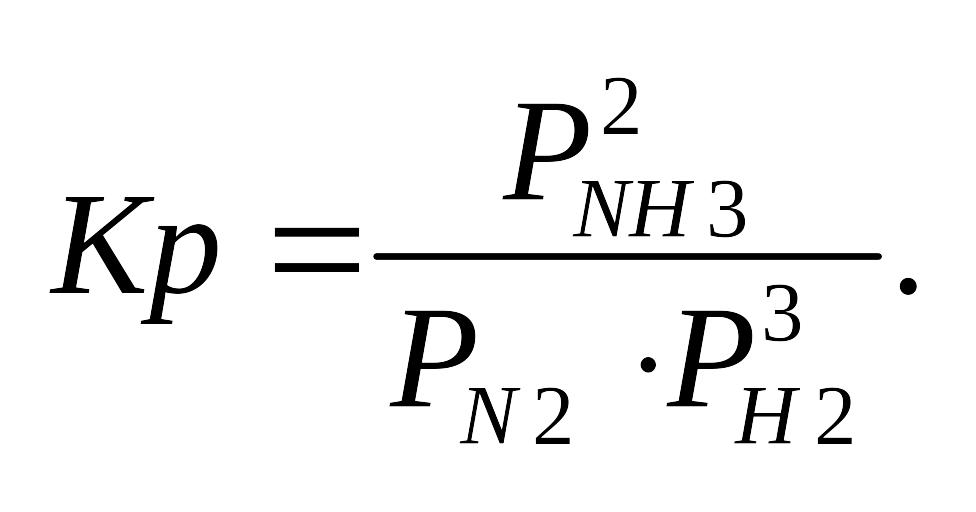
![]() константа равновесия, выраженная
через концентрации.
константа равновесия, выраженная
через концентрации.
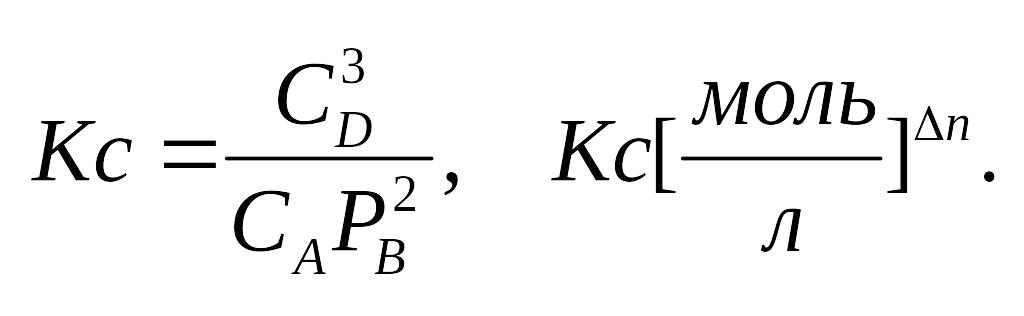
еще![]()
Соотношения между константами равновесия:
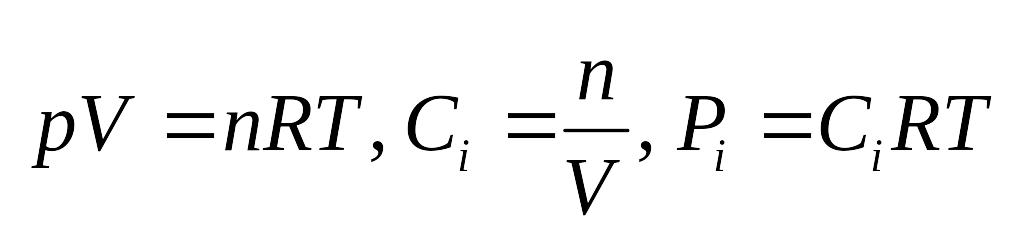
![]()
![]()
Скорость химической реакции. Закон действующих масс. Константы скорости гомогенной и гетерогенной химических реакций. Связь константа скорости с константой равновесия
Скорость гомогенной (однофазной) реакции зависит от природы реагирующих веществ, их концентрации и температуры.
Скорость гетерогенных (многофазных) процессов зависит от размеров и состояния поверхности раздела фаз.
Закон действующих масс (з.Д.М.)
При постоянной температуре скорость химической реакции пропорциональна произведению концентраций реагирующих веществ.
A + B = D, v = k[A][B], где k - константа скорости реакции, зависящая от природы реагирующих веществ, в квадратных скобках - концентрации участников реакции.
Если
положить [A]
= 1 ![]() и [B]
=
, то v
= k,
следовательно, константа скорости
численно равна скорости реакции для
того случая, когда концентрации каждого
из реагирующих веществ равны единице.
и [B]
=
, то v
= k,
следовательно, константа скорости
численно равна скорости реакции для
того случая, когда концентрации каждого
из реагирующих веществ равны единице.
"k" не зависит от концентрации в каждый момент времени.
Константа равновесия отношение констант скорости прямой и обратной реакции. Отсюда вытекает физический смысл константы равновесия: она показывает, во сколько раз скорость прямой реакции больше скорости обратной при данной температуре и концентрациях всех реагирующих веществ, равных 1 моль/л.
Кинетическая классификация по степени сложности. Молекулярность и порядок реакции. Обратимые и необратимые реакции. Классификация реакций по степени сложности
Изолированные реакции при их протекании образуются продукты только одного типа.
Параллельные реакции в ходе них взятые вещества одновременно реагируют в двух или более направлениях.
Схематично:
![]()
Наблюдаемая
скорость реакции: ![]()
Для параллельной мономолекулярной реакции:
![]()
можно
написать ![]() ,
где х - количество молей А, израсходованных
к моменту времени, "а"
число молей А в начальный момент.
,
где х - количество молей А, израсходованных
к моменту времени, "а"
число молей А в начальный момент.
После интегрирования:
Сопряженные реакции - совместные реакции вида:
![]()
Последовательные (многоступенчатые) реакции:
![]()
Обратимые и необратимые реакции.
Наблюдаемая
скорость обратимой реакции ![]()
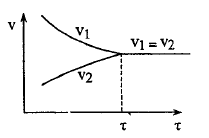 Существуют
реакции, в которых доминирует процесс,
идущий в одном направлении, поскольку
продукты реакции быстро удаляются из
системы: выпадение осадка, газа и т.д.
Существуют
реакции, в которых доминирует процесс,
идущий в одном направлении, поскольку
продукты реакции быстро удаляются из
системы: выпадение осадка, газа и т.д.
В какой-то мере эти реакции все же обратимы, их можно считать лишь практически необратимыми.
Для
совершенно необратимых реакций скорости
прямого и обратного процессов несоизмеримы:
![]()
Когда скорости сравниваются, устанавливается подвижное равновесие
![]()
При неизменных условия химическое равновесие может сохраняться сколь угодно долго.
Зависимость скорости реакции от температуры. Правило Вант-Гоффа. Уравнение Аррениуса. Зависимость скорости реакции от температуры.
Согласно эмпирическому правилу Вант-Гоффа, повышение температуры на каждые 10 увеличивает скорость реакции в 2-4 раза.
Увеличение скорости реакции нельзя объяснить увеличением скоростей движения молекул и учащением вследствие этого столкновений.
С ростом температуры происходит перераспределение энергии между молекулами таким образом, что резко возрастает число активных молекул, обладающих некоторым избытком энергии (энергией активации).
С.
Аррениус установил: ![]() , где к - константа скорости реакции, а
А и В - индивидуальные постоянные,
характерные для данной реакции.
, где к - константа скорости реакции, а
А и В - индивидуальные постоянные,
характерные для данной реакции.