Материал: Возбудитель Холеры
21
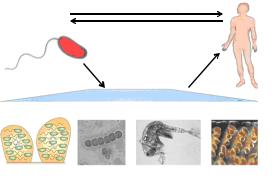
резервуар - загрязненная вода; источник инфекции – больной человек с первых дней заболевания и бактерионоситель. Опасность представляют как больные с типичной формой холеры, так и больные со стертыми, субклиническими и атипичными формами заболевания, а также реконвалесценты после типичной или субклинической формы холеры (вибриовыделители – реконвалесценты). При холере имеет место так называемый феномен “айсберга”, когда на 1 больного приходится до 100 носителей. Продолжительность вибриононосительства у реконвалесцентов редко превышает 2-4 недели, иногда длится до 3 лет. Известно транзиторное здоровое носительство, когда заболевание не развивается, но в фекалиях в течение длительного времени обнаруживается возбудитель (характерно для инфекции, обусловленной биоваром Эль-Тор). В литературе описан случай носительства холерного вибриона в течение 13 лет (“холерная” Долорес). Основные механизмы передачи - фекально-оральный и контактный. Факторы передачи – вода, пищевые продукты, объекты окружающей среды. В воде открытых водоемов холерный вибрион часто находится в ассоциациях с зоопланктоном (в частности, с веслоногими рачками) и водными растениями. Пути заражения холерой – водный (через воду, используемую для питья, купания и хозяйственно-бытовых нужд), алиментарный (пищевой) и контактно-бытовой. Определённую роль могут играть мухи, способные переносить возбудителя с испражнений больного человека на пищевые продукты. Пути и факторы заражения человека холерным вибрионом представлены на рисунке 24.
Восприимчивый
организм
Планктонные
V. cholerae
Экологические резервуары
|
Цианобактерии |
Яйца комаров |
Биопленки |
Ракообразные |
|
Рисунок 24 – Пути и факторы заражения человека холерой.
Все крупные эпидемии и пандемии холеры были связаны с водой. Больной холерой человек выделяет во внешнюю среду в 1 мл испражнений от 10 млн. до 1 млрд. вибрионов, а бактерионоситель – до 100 тыс. микробных клеток. Переболевшие лица выделяют холерный вибрион в течение 7-10 дней после клинического выздоровления. Примерно у 4-5% переболевших формируется хроническое носительство, при котором холерный вибрион сохраняется в желчном пузыре. Заражающая доза составляет около 1 млн. микробных клеток. Заражение человека от человека не происходит.
22
Факторы патогенности холерного вибриона
К факторам патогенности холерного вибриона относятся:
-подвижность и хемотаксис (способность бактерий двигаться по направлению к аттрактантам, то есть к питательным веществам);
-факторы адгезии и колонизации: токсин-корегулируемые пили (toxin coregulated pilus, TCP); гемагглютинины; белки внешней мембраны;
-токсины: экзотоксин – холероген (СТ – cholera toxin) и эндотоксин;
-ферменты агрессии: фибринолизин, гиалуронидаза, нейраминидаза, муциназа, протеаза и др.
Благодаря подвижности за счет жгутиков и хемотаксису холерный вибрион преодолевает слой слизи на поверхности энтероцитов кишечника и вступает во взаимодействие с эпителиальными клетками. У мутантов холерных вибрионов, утративших подвижность или способность к хемотаксису, вирулентность резко снижается.
Основными компонентами микробной клетки, обеспечивающими адгезию (прикрепление) возбудителя холеры к энтероцитам, являются токсинкорегулируемые пили, гемагглютинины и белки внешней мембраны.
Токсин-корегулируемые пили (ТСР) или фимбрии представляют собой тонкие гибкие нитевидные образования на поверхности бактериальной клетки. Они состоят из белковых повторяющихся субъединиц с молекулярной массой 20,5 кД. С помощью ТСР холерные вибрионы прикрепляются к энтероцитам. После адгезии вибрионы утрачивают подвижность и интенсивно размножаются, колонизируя микроворсинки тонкого кишечника. ТСР кодируются кластером генов, входящих в состав островка патогенности VPI. Непосредственно за синтез ТСР отвечают гены tcpA-F, причем за биосинтез основной субъединицы пилей отвечает ген tcpA.
Вместе с ТСР в колонизации энтероцитов принимают участие белки внешней мембраны холерного вибриона. Основная роль при этом принадлежит белку OmpU, который защищает микробную клетку от бактерицидного действия содержимого кишечника. Кроме того, белки ТСР и OmpU являются важными протективными антигенами возбудителя холеры. Антитела к ним прекращают инфекционный процесс, предотвращая адгезию и колонизацию энтероцитов.
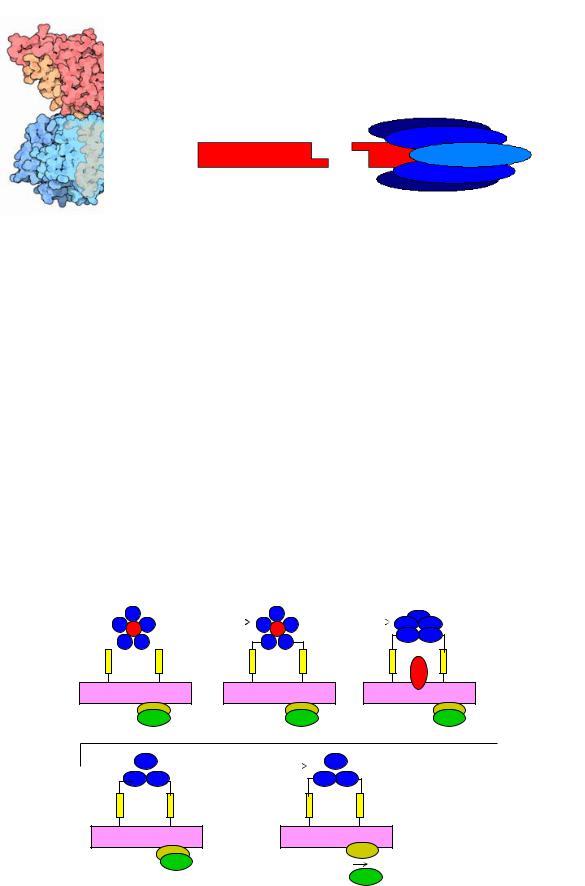
Вслед за адгезией и колонизацией происходит синтез холерного экзотоксина холерогена – СТ (cholera toxin) и его секреция в окружающую среду. Холероген является главным фактором патогенности возбудителя холеры. Он секретируется в окружающую среду системой секреции II типа. СТ состоит из компонентов А и В. Компонент А имеет молекулярную массу 27,2 кД и состоит из 2 пептидов – А1 и А2, связанных дисульфидными мостиками. Пептид А2 служит для связи фрагментов А и В. Компонент В имеет молекулярную массу 58 кД и состоит из пяти кольцевидно соединенных субъединиц. Компонент В выполняет функцию связывания вибриона с энтероцитами, а компонент А – каталитическую (токсическую) функцию (рисунок 25).
23
A1 |
|
|
A2 |
B |
|
|
|
|
|
|
|
|
|
|
|
|
|
S |
|
S |
|
||
|
|
||||
а |
б |
|
|||
Рисунок 25 – Кристаллическая структура (а) и схематическое строение (б) двухкомпонентного токсина V. cholerae. Компонент А обозначен красным цветом, компонент В – синим.
Компонент В через 1-3 минуты после выделения токсина из микробной клетки распознает на поверхности энтероцита специфический рецептор (ганглиозид Gm1), связывается с ним и формирует внутримембранный канал для прохождения компонента А внутрь клетки. Внутри клетки белок А1 взаимодействует с протеином G, располагающимся на внутренней стороне мембраны энтероцита. Образующаяся АДФ-рибоза связывается с регуляторной субъединицей аденилатциклазы, в результате чего внутри клетки происходит повышение концентрации циклического аденозинмонофосфата (цАМФ). Эти изменения происходят в течение 30 минут после контакта токсина с клеточным рецептором. Механизм действия холерного экзотоксина на эпителиальные клетки представлен на рисунке 26.
Холерный |
|
|
токсин |
|
Проникновение |
B |
Связывание |
компонента А |
B A B |
|
|
B B |
|
|
Gm1 |
Gm1 |
|
Клеточная мембрана
G протеин
Диссоциация компонента А на фрагменты А1 и А2
Активация аденилатциклазы, 
 накопление цАМФ
накопление цАМФ 
А1
 А2
А2
АТФ цАМФ
Рисунок 26 – Механизм действия холерного токсина на энтероциты.
Гиперпродукция цАМФ приводит к выходу из энтероцитов в просвет кишечника изотонической жидкости с низким содержанием белка и высокой
24
концентрацией катионов и анионов (Na+, НСО3-, К+, Сl-). Все это приводит к развитию диареи, обезвоживанию и обессоливанию организма. Кроме того, в результате этого в просвете кишечника создается идеальная щелочная среда для размножения возбудителя.
Эндотоксин V. cholerae представляет собой термостабильный липополисахарид (ЛПС). Он отвечает за общую интоксикацию организма и рвоту. Антитела, образующиеся против эндотоксина, обладают выраженным вибриоцидным действием (растворяют вибрионы в присутствии комплемента) и являются важным компонентом постинфекционного и поствакцинального иммунитета.
Ферменты агрессии разрушают вещества, содержащиеся в слизи и облегчают продвижение вибрионов к эпителиальным клеткам. В частности, муциназа разрушает муцин, облегчает проникновение вибрионов к поверхности эпителия и открывает доступ к рецептору – ганглиозиду Gm1. Нейраминидаза (сиалидаза), отщепляя от гликопротеинов эпителия сиаловую кислоту, способствует адгезии вибрионов на поверхности энтероцитов. Кроме того, она увеличивает количество рецепторов для холерогена путем модификации три- и дисиалоганглиозидов в моносиалоганглиозид Gm1, который служит рецептором для экзотоксина-холерогена. Ген nan, определяющий синтез нейраминидазы (NanH), входит в состав островка патогенности VPI-2.
Основные факторы патогенности холерного вибриона детерминируются генами, расположенными на мобильных генетических элементах (МГЭ). К числу МГЭ относятся умеренный профаг СТХφ, два острова патогенности (VPI-1 и VPI-2), два острова пандемичности (VSP-1 и VSP-2), интегронный остров. Биосинтез холерного токсина определяется генами ctxAB, входящими в состав профага СТХφ. Бактериофаг фи вызывает лизогенную конверсию холерного вибриона. При этом холерные вибрионы классического биовара продуцируют холерный токсин 1-го типа, а вибрионы биовара eltor – холерный токсин 2-го типа. У нетоксигенных штаммов элемент СТХ отсутствует.
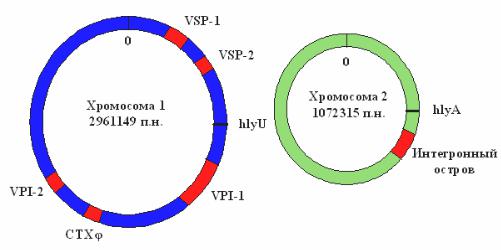
МГЭ присутствуют на двух хромосомах V. cholerae: большой и малой (рисунок 27).
Рисунок 27 – Локализация на хромосомах V. cholerae генов, связанных с вирулентностью возбудителя.
Основные гены патогенности холерного вибриона располагаются в составе
25
МГЭ на большой хромосоме: два острова патогенности (VPI-1 и VPI-2), два острова пандемичности (VSP-1 и VSP-2), элемент СТХφ. В состав этих МГЭ входят гены ctxAB, кодирующие синтез холерного токсина (СТ); гены tcpA-F, кодирующие продукцию токсин-корегулируемых пилей (ТСР); ген zot, кодирующий токсин Zot (zonula occludens toxin), который действует на плотные межклеточные контакты (zonula occludens); ген ace, кодирующий добавочный холерный энтеротоксин Ace (accessory cholera enterotoxin); гены, необходимые для биосинтеза клеточной стенки и О-антигена. В частности, гены ctxA, ctxB, zot и ace входят в состав элемента СТХφ, представляющего собой геном умеренного бактериофага СТХφ (бактериофага фи). В составе генома фага находится также последовательность RS2, кодирующая репликацию фага и его интеграцию в хромосому.
Биосинтез О1-антигена определяется кластером генов wbe, а биосинтез О139-антигена – кластером генов, обозначаемых wbf.
Образование холерного экзотоксина, токсин-корегулируемых пилей, гемагглютининов и других факторов патогенности регулируют белки, кодируемые генами toxS, toxT и toxR. В зависимости от внешних условий эти белки изменяют экспрессию генов, кодирующих факторы патогенности.
На малой хромосоме локализуются структурные гены hlyA, отвечающие за синтез термолабильного гемолизина, а также интегронный остров, содержащий гены антибиотикоустойчивости и участвующий в приобретении новых генов. Ген hlyA присутствует в хромосоме всех штаммов холерного вибриона, но в гене hlyA холерного вибриона классического биовара имеется делеция, в результате которой гемолитическая активность у этого биовара отсутствует.
Потеря или приобретение новых МГЭ приводит к формированию новых патогенных клонов холерного вибриона. В последнее время выделяются штаммы V. cholerae eltor, содержащие классический профаг СТХφ и продуцирующие холерный токсин 1-го типа. Такие штаммы отличаются повышенной вирулентностью. В то же время, утрата профага СТХφ приводит к снижению вирулентности, но повышает выживаемость вибрионов во внешней среде.
Патогенез холеры
Входными воротами инфекции при холере является пищеварительный тракт. Попав в организм человека, значительная часть вибрионов погибает в желудке под действием соляной кислоты. Оставшаяся часть возбудителя достигает тонкой кишки, щелочная среда которой является благоприятной для размножения холерного вибриона.
Холера является неинвазивной инфекцией, так как вибрионы локализуются на поверхности слизистой оболочки и в просвете тонкого кишечника, не проникая внутрь энтероцитов. Но энтероциты тонкой кишки являются мишенью для холерного экзотоксина. Для достижения клеток-мишеней холерному вибриону необходимо преодолеть слой слизи на поверхности энтероцитов. Преодолению этого барьера способствует подвижность возбудителя, его способность к хемотаксису, образование гемагглютинина-протеазы и муциназы. Гемагглютинин-