Материал: Сыровая А.О. и др Аминокислоты глазами химиков, фармацевтов, биологов. Т. 2
клеточном уровне. Необходим для построения и развития мышечной ткани,
синтеза протеина организмом, для укрепления иммунной системы.
Понижает содержание сахара в крови и способствует быстрейшему заживлению ран и срастанию костей.
Предотвращает перепроизводство серотонина и наступление усталости,
связанное с этим процессом.
Метаболизм
Метаболизм L-лейцина играет важнейшую роль в цепи превращений свободных аминокислот в организме человека. В отличие от других аминокислот,
метаболизируемых главным образом в печени, L-лейцин утилизируется в мышцах и почках. Образующиеся в процессе его катаболизма глутаминовая кислота,
глутамин и аланин являются основными предшественниками в реакциях глюконеогенеза. Катаболизм L-лейцина происходит по пути трансаминирования и окислительного декарбоксилирования [14].
Биосинтез L-лейцина в растениях и бактериях осуществляется из 2-оксо-3-
метилбутановой кислоты через 2-оксо-4-метилпентановую кислоту, из которой в результате переаминирования образуется лейцин. В организме животных лейцин метаболизирует до 2-оксо-4-метилпентановой кислоты, из которой в результате дальнейших превращений образуется 3-гидрокси-3-метилглутарилкофермент А
(промежуточное соединение в синтезе стероидов), а затем ацетоуксусная кислота и ацетилкофермент А (Участвует в цикле трикарбоновых кислот и биосинтезе жирных кислот) [14, 26].
Биологические свойства Отсутствие Лейцина в пище приводит к отрицательному балансу азота и
прекращению роста у детей 8 . Суточная потребность в Лейцине у взрослых – 31
мг/кг веса, у младенцев – 425 мг/кг. Один из продуктов распада Лейцина в организме – b-окси-b-метилглутаровая кислота (в виде ацилкофермента А),
является важным промежуточным соединением при биосинтезе холестерина и др.
116
стероидов. Лейцин вместе с глутаминовой кислотой, метионином и др.
аминокислотами применяется для лечения болезней печени, анемий, а также при некоторых психических заболеваниях [7].
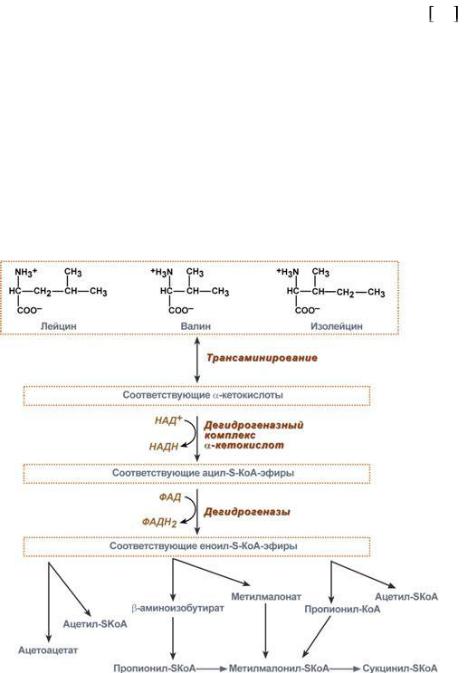
Катаболизм углерода: лейцин, валин и изолейцин (рис. 7) 26 . Учитывая структурное сходство L-лейцина, L-валина и L –изолейцина их начальные реакции катаболизма одинаковы. Затем пути их расходятся и скелет каждой аминокислоты трансформируется по собственному пути с образованием амфиболических интермедиатов. В зависимости от природы этих амфиболических конечных продуктов аминокислоты относят к типу гликогенных
(валин), кетогенных (лейцин) или к обоим типам (изолейцин). Учитывая сходство начальных реакций катаболизма все три аминокислоты рассматриваются вместе.
Рис. 7. Пути катаболизма лейцина, валина и изолейцина Первый этап катаболизма – трансаминирование. Эта реакция обратима и
катализируется одной и той же трансаминазой. Продуктами переаминирования являются α-кетокислоты: из лейцина – α-кетоизокапронат, из валина – α-кето-
117

изовалерат, из изолейцина – α-кето-β-метилвалерат. Обратимость этой реакции объясняется, возможность замены в диете L-α-аминокислот соответствующими α-
кетокислотами, если организму доступны адекватные источники азота 22 .
Окислительное декарбоксилирование с образованием ацил-CoA-тиоэфиров.
Эта реакция аналогична окислению пирувата до ацетил-CoA и CO2
пируватдегидрогеназой и окислению α-кетоглутарата до CO2 и сукцинил-CoA α-
кетоглутаратдегидрогеназой. Эти продукты подобного пируватдегирогеназе и состоящего из таких же продуктов и коферментов. Активность этого комплекса ингибируется при помощи протеинкиназы и активируется путем дефосфорилирования фосфопротеинфосфатазой. Кетокислоты являются регуляторами протеинкиназы. Дегидрогеназа разветвленных α-кетокислот проводится митохондриальным мультиферментным комплексом,
катализирующим окислительное декарбоксилирование α-кетоизокапроата (из лейцина), α-кето-β-метилвалерата (из изолейцина) и α-кетоизовалерата (из валина). Перевод фермента в фосфорилированное состояние может регулировать катаболизм аминокислот с разветвленной цепью. Протеинкиназа ингибируется
ADP, α-кетокислотами с разветвленной цепью, гиполипидемическим агентом клофибратом и дихлорацетатом а также тиоэфирами кофермента А (например,
ацетоацетил-CoA). Из разветвленных α-кетокислот самым сильным ингибитором является α-кетоизокапроат (α-кетолейцин) 30 .
В. Дегидрогенирование с образованием α, β- ненасыщенных тиоэфиров ацил-CoA. Эта реакция аналогична дегидрогенированию линейных ацил-CoA
тиоэфиров в процессе катаболизма жирных кислот.
Пока неизвестно, катализирует ли одна и та же дегидрогеназа дегидрогенирование всех трех разветвленных ацил-CoA тиоэфиров 15 .
Косвенные данные указывают на участие по крайней мере двух ферментов; они основаны на обследовании пациентов с изовалериановой ацидемией, у которых после приема обогащенной белком пищи в крови накапливается изовалерат; при
118
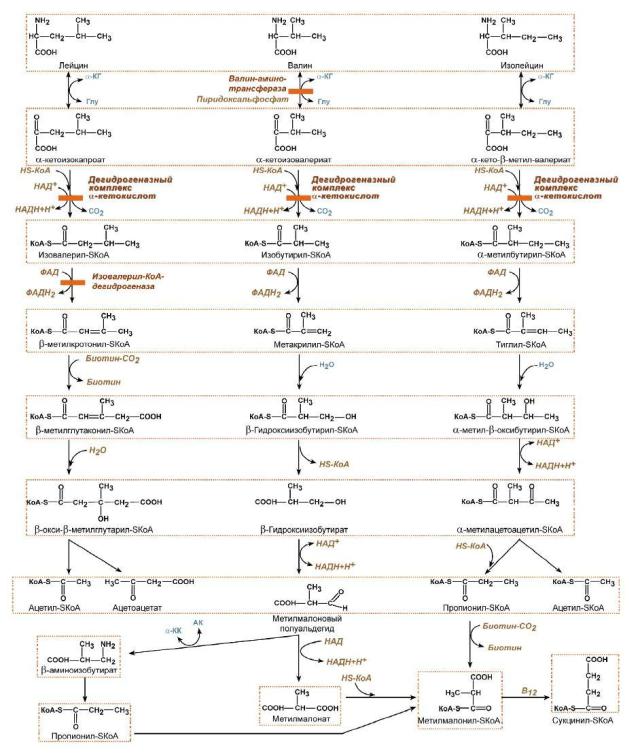
этом содержание других разветвленных α-кетокислот не повышается. Изовалерат образуется путем деацилирования изовалерил-CoA, который является субстратом упомянутой выше дегидрогеназы. Нарушение распада лейцина, валина,
изолейцина представлено на рис. 8.
Рис. 8. Нарушение распада лейцина, валина, изолейцина [27]
119
Лейцин в спорте Лейцин для спортсменов играет особую роль. Существуют исследования
[13], которые предполагают, что использование лейцина может быть очень эффективным. Лейцин выполняет важную роль в создании новых мышечных тканей в организме, способствует увеличению синтеза белка. В то же время лейцин подавляет разрушение белковых молекул, что очень важно для мышечного роста. Таким образом, можно уменьшить распад белков после интенсивных тренировок при увеличении потребления лейцина, что в конечном итоге приводит к гораздо более позитивному азотистому балансу, чем при использовании плацебо. Лейцин также обеспечивает и другие различные репаративные процессы в организме [26].
Лейцин немаловажен и в процессах получения энергии [28]. Он косвенно экономит запасы глюкозы и подавляет их разрушение. Лейцин предотвращает мышечный катаболизм. Другие аминокислоты с разветвленными боковыми цепями, изолейцин и валин, служат в первую очередь как субстрат для глюконеогенеза и также проявляют, таким образом, свой антикатаболический эффект. По этой причине комбинированный прием всех трех этих аминокислот особенно эффективен 28 .
Тем не менее, процессы окисления не обязательно следует рассматривать как нечто негативное. Окисление аминокислот во время физических упражнений может быть нужно для обеспечения высокой скорости анаболических процессов в мышце. Таким образом, метаболизм лейцина стимулирует рост мышц и одновременно подавляет дальнейшую потерю мышечной массы [29].
Еще одним анаболическим свойством лейцина является его способность стимулировать секрецию инсулина. Лейцин обладает наибольшим инсулиногенным эффектом по сравнению с двумя другими аминокислотами
BCAA (изолейцином и валином). Инсулин –гормон, напрямую участвующий в транспорте глюкозы и аминокислот в клетки. Таким образом, поступление
120