Материал: Сыровая А.О. и др Аминокислоты глазами химиков, фармацевтов, биологов. Т. 2
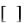
мозге. Вместе с лейцином и изолейцином служит источником энергии в мышечных клетках, а также препятствует снижению уровня серотонина. Валин повышает мышечную координацию и понижает чувствительность организма к боли, холоду и жаре [17, 18].
Недостаток валина действует угнетающе на нервную систему человека. У
людей, страдающих от нехватки этой аминокислоты, может возникнуть раздражение, быстрая утомляемость, депрессия, множественный склероз. У
людей, борющихся с вредными привычками – курением, наркоманией,
алкоголизмом, вследствие нехватки валина может произойти срыв [19].
Медики применяют данную аминокислоту для лечения болезненных пристрастий.
Чрезмерно высокий уровень валина может привести к таким симптомам, как парестезии (ощущение мурашек на коже), вплоть до галлюцинаций [19].
Используется для лечения болезненных пристрастий и вызванной ими аминокислотной недостаточности, наркоманий, депрессий (несильное стимулирующее соединение); множественного склероза, так как защищает миелиновую оболочку, окружающую нервные волокна в головном и спинном мозге 9 .
Также необходим для поддержания нормального обмена азота в организме.
Пути катаболизма валина Продукт реакции дегидрирования метилакрилил-КоА быстро
гидратируется спонтанно или под влиянием кротоназы, которая катализирует реакции с участием b-гидроксиацил-КоА, которые содержат 4-9 атомов углерода.
Образующийся b-гидроксиизобутирил-КоА сначала деацилируется при помощи деацилазы в b-гидроксиизобутират, который затем окисляется при помощи НАД зависимой дегидрогеназы с образованием метилмалонового альдегида. Реакция легко обратима. Дальнейший метаболизм метиламалонового полуальдегида в тканях млеокпитающих может идти по двум путям: или путем переаминирования он превращается в b-амино-изобутират или окисляется в метилмалонат с
106
последующим образованием метилмалонил-СоА и изомериза-цией последнего в сукцинил-СоА. Переаминирование с образованием b-аминоизомасляной кислоты,
которая в норме присутствует в моче, – осуществляется в различных тканях млекопитающих, в том числе в почках. Изомеризация протекает при участии аденозилко-баламинового кофермента и она катализируется метилмалонил-КоА-
мутазой. Эта реакция важна для катаболизма не только валина, но и пропионил-
КоА-катаболита изолейцина (рис. 3) 14 .
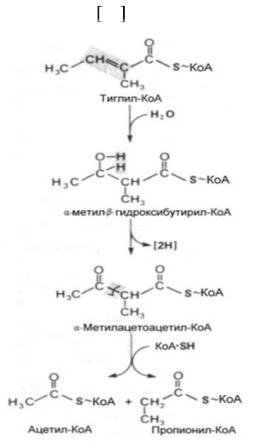
Рис. 3. Образование пропионил-КоА Пропионил-СоА, который образовался из изолейцина как и из других
источников превращается в сукцинил-КоА. Это превращение включает биотинзависимое карбо-ксилирование с образованием метилмалонил-КоА. Это соединение образуется также непосредственно из валина (без предварительного образования пропионил-КоА). В результате изомеризации под действием конфермента (произодное витамина В12) метилмалонил-КоА превращается в сукцинил-КоА как промежуточный метаболит цикла лимонной кислоты (рис. 4).
107
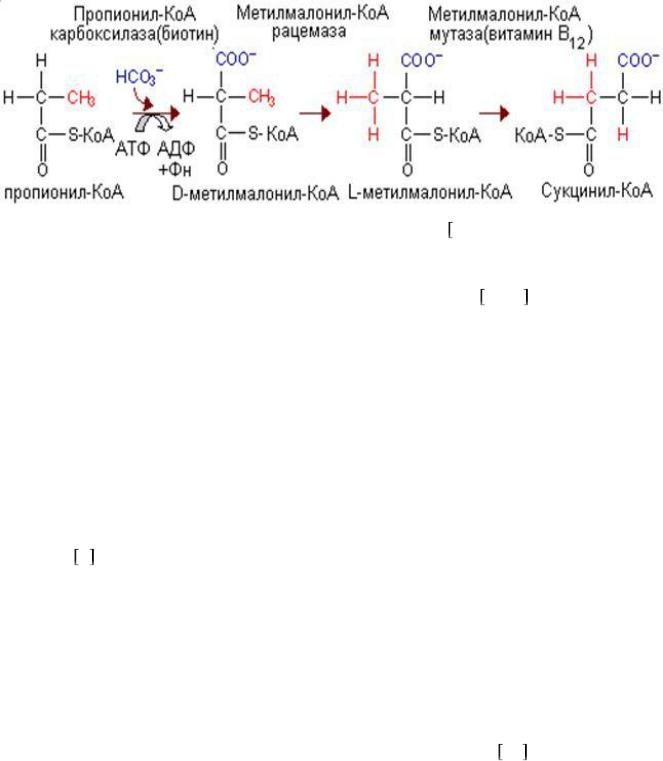
Рис. 4 Пути метаболизма валина 14
Нарушение декарбоксилирования аминокислот с разветвленной цепью приводит к болезни Гипервалинемия и «кленового сиропа» 9, 15 .
Гипервалинемия
Гипервалинемия (греческий hyper- + валин + греческий haima кровь) –
наследственная болезнь, обусловленная нарушением обмена аминокислоты валина. Проявляется отставанием в физическом развитии и нервно-психическими нарушениями. Гипервалинемия наследуется по аутосомно-рецессивному типу.
Впервые описана Вадой, Тадой и Минагавой (Y. Wada, К. Tada, A. Minagawa) в 1963 год 9 .
В основе заболевания лежит дефицит фермента валинтрансферазы,
катализирующего превращение валина в α-кетоизовалериановую кислоту.
Переаминирование других аминокислот с разветвлѐнной цепью (лейцина,
изолейцина) не нарушено. Вследствие энзиматического блока повышается концентрация валина в крови (более 3 миллиграмм%) и его выделение с мочой.
При этом уровень α-кетокислот в крови и моче не изменяется 15 .
Симптомы. Наибольшее токсическое (отравляющее) действие оказывается на центральную нервную систему, что проявляется в виде рвоты, вялости,
мышечных подергиваний, нистагма (движений глазных яблок). Ребенок отстает в
108

росте и весе, поздно начинает держать голову, сидеть. Без лечения наступает неуклонное снижение интеллекта 9, 15 .
Клиническая картина Гипервалинемия проявляется в первые месяцы жизни рвотой, обезвоживанием организма и развитием комы. В дальнейшем развивается гипотрофия, появляется неврологический симптоматика – нистагм, общая мышечная гипотония, сухожильная гиперрефлексия, гиперкинезы, судорожные припадки. С возрастом выявляются признаки отставания в психическом развитии 9 .
Диагноз основывается на данных хроматографического выявления повышенного содержания валина в крови и экскреции его с мочой.
Дифференцируют Гипервалинемия с аргининянтарной аминоацидурией (смотри Аминоацидурия аргинин янтарная), гипераммониемией (смотри),
гиперглицинемией (смотри Глицинемия), декарбоксилазной недостаточностью
(смотри), лизинемией, цитруллинемией 16 .
Лечение. Принцип лечения состоит в том, чтобы доза валина в продуктах питания не превышала 75—100 мг на 1 кг массы тела ребенка. На фоне такого лечения быстро исчезает рвота, ребенок начинает прибавлять в весе и нормально развиваться. Исследования электрической активности мозга в динамике могут служить критерием эффективности такой диеты. Прогноз неблагоприятный.
Большинство больных погибает в раннем детском воздасте 9 .
Болезнь «кленового сиропа». Наиболее ярким отличительным признаком этой наследственной болезни является характерный запах мочи больного,
напоминающий запах кленового сиропа или жженого сахара. В плазме и в моче сильно повышается содержание аминокислот с разветвленной цепью – лейцина,
изолейцина и валина, а также соответствующих им α-кетокислот. Поэтому болезнь «кленового, сиропа» иногда называют кетонурией разветвленных кетокислот. Отмечено также присутствие в моче разветвленных α-
гидроксикислот, образующихся при восстановлении α-кетокислот 9, 16 .
109

Характерные признаки болезни проявляются в конце первой недели после рождения. Наряду с описанными выше биохимическими нарушениями возникают трудности при кормлении ребенка, может наблюдаться рвота. Иногда наблюдается летаргия.
Диагноз ранее конца первой недели возможен только с помощью ферментного анализа. У выживших детей отмечены выраженные нарушения мозговой деятельности. При отсутствии лечения летальный исход наступает к концу первого года жизни.
Биохимической причиной болезни является отсутствие или сильное снижение активности декар-боксилазы α-кетокислот, катализирующей превращение всех трех разветвленных α-кетокислот в ацил-СоА-тиоэфиры с выделением СО2. Это было установлено путем ферментного анализа лейкоцитов и клеток культуры фибробластов кожи больных детей. Механизм токсического действия накапливающихся соединений неизвестен 15 .
Больным назначают диету с заменой белков на смесь очищенных аминокислот, не содержащую лейцина, изолейцина и валина. После того как содержание этих трех аминокислот в плазме снизится до нормального уровня,
можно вводить их в пищу, например, в составе молока и других продуктов, но лишь в таком количестве, чтобы обеспечить (но не превысить) потребности в аминокислотах с разветвленной цепью. Нет сведений о том, можно ли впоследствии ослабить ограничения в диете и когда именно. Если лечение было начато в первую неделю жизни ребенка, удается значительно смягчить тяжелые проявления болезни 9 .
Лекарственные средства
D-валин входит в состав некоторых антибиотиков, например,
валиномицина [7]. Валиномицин представляет собой полимер, повышающий проницаемость мембраны для ионов калия. Он имеет кольцеобразную структуру.
Наружная гидрофобная часть его молекулы состоит из боковых цепей валина и
110