Материал: Сыровая А.О. и др Аминокислоты глазами химиков, фармацевтов, биологов. Т. 2
26.Ellaway CJ. Outcome of Tyrosinemia Type III. / Ellaway CJ., Holme E, Standing S. et al. // J. Inherit. Metab. Dis. – 2001.– vol. 24. – P. 824-32. (Итоги тирозинемия типа III. Дж. Наследовать. Metab.)
27.Banderet L.E. Treatment with tyrosine, a neurotransmitter precursor, reduces environmental stress in humans./ Banderet L.E., Lieberman H.R. // Brain Res Bull.
–1989. – vol. 22. – P. 759-762/ (Лечение тирозина, нейромедиатор предшественником, снижает нагрузку на окружающую среду в организме человека. Brain Res Bull)
28.Кормление и питание грудных детей и детей раннего возраста. Методические рекомендации для Европейского региона ВОЗ с особым акцентом на республики бывшего Советского Союза, UNISEF (Фонд ООН помощи детям).
–ВОЗ, 2003. – № 87
29.Инструкция по организации питания детей в дошкольных учебных заведениях
/ пр. МОН Украины, МЗУ 17.04.2006 г № 298/227 – режим доступа
http://www.moz.gov.ua/ua/
30.Аткинс Р. Биодобавки: Природная альтернатива лекарствам. /Р.С.Аткинс; перевод Г.Левитан. – Минск: Попурри, 2012. – 800 с. –ISBN 978-985-15-1748- 6.
31.Лечение БАДами. Режим доступа – http://www.lechenie-badami.ru/amino
32.Компендиум 2012 – лекарственные препараты. – МОРИОН, 2012. Режим доступа – http://compendium.com.ua/
33.Официальный сайт РЛС Росиии. Режим доступа http://www/rlsnet.ru
34.Официальный сайт компании Нутритек (Россия): http://www.nutritek.ru
35.Официальный сайт МЗ Украины. Режим доступа – http://www.moz.gov.ua/ua/
36.Богатырев В.Г., Маринчук А.Т. К дифференциальной диагностике эрозивно-
язвенных поражений желудка и двенадцатиперстной кишки ишемического (атеросклеротического) генеза./ В.Г. Богатырев; А.Т. Маринчук // г. Ростов-на-
Дону : РостГМУ. – 2013. – №2 (33) – С. 55-60.
71

ГЛАВА 11
ПРОЛИН И ОКСИПРОЛИН
ЛЕВАШОВА ОЛЬГА ЛЕОНИДОВНА кандидат фармацевтических наук
ассистент кафедры медицинской и биоорганической химии ХНМУ
72
СПИСОК СОКРАЩЕНИЙ
АDP − аденозин дифосфорная кислота
ATP − аденозин трифосфорная кислота
Gly – Глицин
NADPH – никотинамид адениндинуклеотидфосфамт а.е.м. – атомная единица массы АК – амнокислота Ала – аланин
АФК – активные формы кислорода ГАМК – г-аминомасляная кислота Гис – гистидин ЖКТ – желудочно-кишечный тракт
МАА – металлопротеины антиоксидантной активности МПА – металлопротеины проантиоксидантной активности ПБП-1 – пролин богатый полипептид -1
ПМР – протонный магнитный резонанс ПОЛ – перекисное окисление липидов Про – пролин Сер – серин
США – Соединенные Штаты Америки ЦНС – Центральная нервная система
73
Пролин – это L-пирролидин-б-карбоновая кислота – гетеро-циклическая аминокислота (точнее, иминокислота); химическая формула C9H9NO2.
молекулярная масса (в а.е.м.): 115,13 [1].
Оксипролин – гидроксипролин, 4-гидроксипирролидин-α-карбоновая кислота, Hyp, отличающаяся от пролина наличием гидроксильной группы у одного из атомов, химическая формула C5H9NO3, молекулярная масса. (в а.е.м.):
131,13 1 .
Пролин существует в виде 3 стереоизомеров: L-(натуральная) форма
пролина, D-(синтетическая) форма и рацемат D, L–пролин.
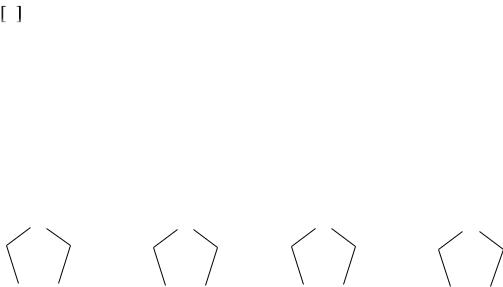
Для оксипролина возможно существование 4 оптически активных стереоизомеров оксипролина (О): L-форма оксипролина (формула I), алло-L-О.
(II), D-О. (III) и алло-D-О. (IV).
|
H |
|
|
H |
|
|
H |
|
COOH |
|
H |
COOH |
|
|
N |
|
|
N |
|
|
N |
|
|
N |
|||
|
|
|
|
|
|
|
|
|
|
||||
|
OH |
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
COOH |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
OH |
|
|
|
|
|
|
||
|
I |
|
|
II |
|
|
III |
|
|
|
IV |
|
|
Оксипролин – бесцветные кристаллы; для L-О. (I) т. пл. 274°С (с разл.),
-76,5° (2,5 г в 100 мл воды), для алло-L-О. (II) т.пл. 245°С (разл.), -59,5° (2%-ный р-р в воде); растворим в воде, ограниченно – в этаноле, не растворим в диэтиловом эфире. При 25 °С для L- О. рKa 1,92 (СООН) и 9,74 (NH2); pI 5,83.
Физико-химические свойства.
Пролин – бесцветные кристаллы; хорошо растворимы в воде (162,3 г в
100мл при 25 °С), ограниченно – в этаноле (1,55 г в 100мл), ацетоне, хлороформе,
не растворим в диэтиловом эфире; селективный осадитель для пролина – роданилат аммония; рКа при 25 °С 1,99 (СООН) и 10,6 (NH); рІ 6,3.
74
L-пролин т.пл. 220-222°С (с разл.); 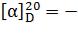 85° (вода); D-(синтетическая)
85° (вода); D-(синтетическая)
форма пролин, т. пл. 215-220°С (с разл.), 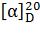 = +81,9° (вода); рацемат D, L –
= +81,9° (вода); рацемат D, L –
пролин т. пл. 205°С (с разл.) [1]. Пролин образует ряд производных; D- и L-
формы образуют растворимые в спирте медные соли; соли D, L-пролина нерастворимы [2]. Эфиры пролина легко образуют производные дикетопиперазина, при метилировании пролина получают стахидрин – бетаин
N,N-диметилпролина (алкалоид).
Пролин и оксипролин относятся к аминокислотам пиррольного ряда и единственные природные аминокислоты, у которых аминогруппа является частью пирролидинового кольца. Оксипролин окисляется и декарбоксилируется до пиррола при помощи NaOCl. Пиррол конденсируют с изатином или л-
диметиламинобензальдегидом в окрашенное соединение.
Пролин и оксипролин, в отличие от других аминокислот, дают желтую, а не
фиолетовую нингидриновую реакцию. С изатином дает синее окрашивание
(характерная реакция на пролин). Реакцию с нингидрином используют для колориметрического количественного определения аминокислот, в том числе в автоматических аминокислотных анализаторах. В реакции с азотистой кислотой пролин и оксипролин не дают азота.
Пролин единственная из кодируемых аминокислот, у которой б-
аминогруппа – фрагмент гетероцикла. При биохимическом окислении пролина
в организме животных образуются 3- и 4-гидроксипролины, остатки которых в больших количествах, особенно 4-гидроксипролина, содержатся в коллагене.
Гидролиз пептидных связей, образованных пролином, осуществляется двумя ферментами – пролиназой (пептидная связь с участием СО-группы) и пролидазой
(пептидная с участием NH-группы). Реакции по атому N пространственно
затруднены. Включение остатков пролина в пептидную цепь обусловливает ее изгибы и потому его присутствие в белках препятствует образованию
75