Материал: Сыровая А.О. и др Аминокислоты глазами химиков, фармацевтов, биологов. Т. 2
нарушении памяти. При помощи пролина, можно значительно повысить эффективность обучения.
Пролин – это одна из главных аминокислот, которую организм использует для выработки коллагена. Из коллагена же производятся прочные, эластичные ткани на поверхности шрамов; он является главным строительным материалом организма – кости, сухожилия, связки и кожа содержат коллаген. Поэтому многокомпонентные смеси аминокислот, предназначенные для восстановления
поврежденных тканей, обычно содержат пролин.
Метаболизм пролина. Пролин содержит атом азота («в связанном виде»),
соединенный с предыдущим аминокислотным остатком, аминокислотным радикалом, и группой СН. Он очень резко изгибает пептидную цепь.
Чередующиеся остатки пролина и оксипролина способствуют созданию стабильной трѐх-спиральной структуры коллагена, придающей молекуле
прочность.
Пептидная связь, образуемая иминогруппой пролина, отличается от других пептидных связей, так как атом азота пептидной группы связан не с водородом, а
с радикалом. Пептиды различаются по аминокислотному составу, количеству и
порядку соединения аминокислот (рис. 4)
H2N |
|
CH |
|
COOH + H2N |
|
CH |
|
COOH |
-H2O |
H2N |
|
CH |
|
CO |
|
NH |
|
CH |
|
COOH |
||||
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R2 |
|||
|
|
R1 |
|
|
|
R2 |
|
|
|
R1 |
|
|
|
|
||||||||||
|
|
|
|
|
|
Образование дипептида |
|
|
|
|
Пептидная связь |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Серилглицилпролилаланин
Радикалы аминокислот (боковая цепь)
|
|
R1 |
|
|
|
R2 |
|
|
|
|
|
|
R3 |
|
|
|
Rn |
||||||||||||
H N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CO . . . . |
|
|
|
|
|
|
COО - |
- пептидный |
|
|
CH |
|
CO |
|
NH |
|
CH |
|
CO |
|
|
NH |
|
CH |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
NH |
|
CH |
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
остов |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
N-конец |
|
|
|
|
|
|
Аминокислотный остаток |
|
|
|
|
|
C-конец |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Рис. 4. Образование дипептида
81

H N |
|
|
CH |
|
CO |
|
NH |
|
|
CH |
|
CO |
|
N |
|
CH |
|
CO |
|
NH |
|
CH |
|
COО |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
H |
|
|
H2С |
|
CH2 |
|
|
CH3 |
||||||||||||
|
ОH |
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Рис. 5. Строение пептидов Сер-Гис-Про-Ала и Ала-Про-Гис-Сер – два разных пептида, несмотря на то,
что они имеют одинаковые количественный и качественный составы аминокислот
[8].
Вследствие мезомерии получаются две устойчивые плоские конформации,
транс (I) и цис (II), при затрудненном свободном вращении около связи С−N:
В 2,5-дикетопиперазинах, простейших циклических пептидах, построенных из двух аминокислот, имеются дос-пептидные связи. Циклические трипептиды могут существовать без напряжения также только с тремя цис-пептидными связями. Поскольку пролил и саркозин не обладают возможностью стабилизации транс-пептидной связи, то можно легко синтезировать циклический трипептид − циклотрипролил. В нативных пептидах и белках преобладает транс-пептидная связь. В некоторых белках были найдены также и цис-пептидные связи, при этом в образовании пептидной связи всегда участвовал пролин.
По стерическим и энергетически соображения не каждую произвольно взятую пептидную последовательность можно перевести в соответствующий циклопептид. Для циклотрипептида требуется, чтобы все три пептидные связи были в энергетически богатой цис-форме. Исходя из энергетических соображений, можно понять низкую тенденцию к образованию 9-членных циклотрипептидов, ибо в их модели имеется сильное напряжение кольца, которое может быть объяснено стерическим взаимодействием направленных внутрь трех
α-Н-атомов (напряжение Прелога). Циклодимеризации, без сомнения,
способствует антипараллельное взаимное расположение двух молекул трипептида с образованием водородных мостиков. Димеризация с образованием водородных связей невозможна, если в трипептид встроен пролин; кроме того, в этом случае
82
цис- и транс-конфигурации пептидных связей практически равноценны энергетически. Роте и сотр. [10] описали в 1965 г. синтез циклотрипролила,
единственного возможного циклотрипептида.
Небольшие циклические пептиды особенно годятся для изучения конформаций, поскольку ограниченная молекулярная подвижность позволяет существовать только некоторым конформациям. Циклотрипептиды в кристаллах обладают только конформацией короны. В растворе же дополнительно появляется асимметричная конформация ванны в том случае, если в трипептиде присутствует хотя бы одна нехиральная аминокислота (саркозин, N-
бензилглицин) [5, 11]
Метаболизм оксипролина Уникальной особенностью метаболизма оксипролина является то
обстоятельство, что эта аминокислота, входящиая в состав белков пищи, не включаются в коллаген. Не существует тРНК, которая могла бы акцептировать оксипролин и далее включать его в растущую полипептидную цепь. В то же время пищевой пролин является предшественником оксипролина в составе коллагена. Гидроксилирование пролина катализируется пролилгидроксилазой – ферментами, находящимися в микросомальной фракции многих тканей (кожи,
печени, легких, сердца, скелетной мышцы, гранулирующих раневых поверхностей). Эти ферменты являются пептидилгидроксилазами, поскольку гидроксилирование происходит только после включения пролина в полипептидную цепь.
Обе гидроксилазы являются оксигеназами со смешанной функцией и функционируют при участии молекулярного кислорода, аскорбат а, ионов Fe+2 и
альфа-кетоглутарата. Пролилгидроксилаза изучена более подробно; есть основания полагать, что лизилгидроксилаза действует аналогичным образом. На каждый моль гидроксилированного пролина декарбоксилируется 1 моль альфа-
кетоглутарата с образованием сукцинат а. В ходе этого процесса один атом
83
кислорода молекулы O2 включается в состав пролина, а другой – в сукцинат
(Биосинтез аминокислот: метаболическая карта ).
В молекуле оксипролина конфигурация при С2 такая же, как и у пролина и других природных аминокислот, а гидроксильная группа находится в транс-
положении по отношению к карбоксильной группе. Окисление пролина в оксипролин происходит, по-видимому, после включения пролина в пептид.
В кристалле отдельные молекулы оксипролина связаны друг с другом трехмерной сеткой водородных связей. В кристалле встречается также несколько довольно коротких С...О расстояний, которые, возможно, являются слабыми водородными связями и играют определенную роль при упаковке молекул.
Во всех случаях, когда оксипролин применяли для синтеза пептидов, его гидроксильная группа была свободной. Исходными веществами в этих синтезах чаще всего служили карбо-бензоксиоксипролин [88, 850, 1694], а также метиловый [996, 2148] и бензиловый [1116, 1756, 2148] эфиры оксипролина.
Производные пиррола: пролин и оксипролин.
У некоторых псевдомонад осуществляется окисление оксипролина по другую сторону от азота кольца с последующим образованием а-кето-глутарата.
Аспарагиновая кислота, глутаминовая кислота, оксипролин.
Следовательно, оксипролин и пролин кодируются одинаково.
Во-первых, кислородный атом гидроксильной группы оксипролина происходит из атмосферного кислорода, как это показано в опытах с изотопной меткой. Во-вторых, предшественником оксипролина, входящего в состав коллагена, служит пролин.
Корреляция между температурой перехода и содержанием оксипролина объясняет связь между Tt и изменением 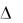 t (обусловленным водородными связями или взаимодействием какого-либо другого характера). В то же время чем больше иминокислотных остатков (пролина или оксипролина) содержится в цепочке, тем больше ограничений накладывается на свободные вращения в
t (обусловленным водородными связями или взаимодействием какого-либо другого характера). В то же время чем больше иминокислотных остатков (пролина или оксипролина) содержится в цепочке, тем больше ограничений накладывается на свободные вращения в
84
цепочке и тем меньше число конформаций, в которых может находиться молекула. Это уменьшение числа возможных состояний, приводящее к уменьшению энтропии перехода, должно увеличить температуру перехода, если энтальпия перехода остается постоянной.
Одна АК также несколько усиливала превращение оксипролина, но не достоверно. При терапевтическом применении чистая АК и в сочетании с витамином Р (кверцетином) достоверно усиливала превращение оксипролина в печени морских свинок. Подобная интенсивность превращения оксипролина была отмечена нами и в печени животных, оставленных на рационе вивария.
Известны методы разделения пролинов и оксипролинов методом газовой хроматографии.
Содержание оксипролина можно определить или классическим спектральным методом (после получения производного соединения с нингидрином), или с помощью высокоэффективной жидкостной хроматографии.
При использовании жидкостных хроматографов фирмы Хьюлетт-Паккард серии
Aminoquant, многие,входящие в состав белка, аминокислоты могут быть идентифицированы и количественно определены за одну хроматографическую разгонку. Возможно обнаружение как спектрофотометрическик детектором, так и флуориметрическим.
По возрастанию содержания оксипролина в легких судили об активности кремнезема, который накапливается одновременно с развитием фиброза. Другое объяснение заключается в том, что в процессе влажного помола кварцевая поверхность покрывается адсорбированным слоем аморфного кремнезема и таким образом становится менее активной.
Эти данные указывают на прямое превращение пролина в оксипролин, но не исключают возможности существования других путей биосинтеза оксипролина. Эти результаты согласуются с малой скоростью обновления коллагена ( стр. Меченый азот оксипролина, введенный с пищей, переходил во
85