Материал: спектр и фотометр
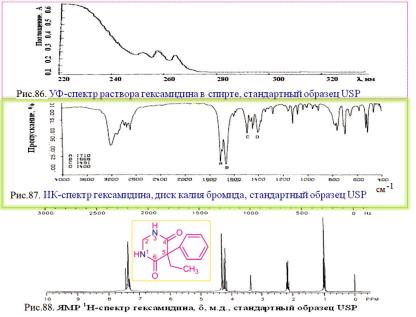
мума – при 250, 255 и 262 нм. Полученные данные полностью согласуются с результатами анализа ПМР-спектра (см. рис. 88) примидона (гексамидина).
Посторонние примеси (не более 2%) в примидоне определяют методом ТСХ, а остаточные растворители (изопропиловый спирт) – методом ГЖХ на хроматографе с детектором ионизации в пламени.
Для количественного определения примидона ФС рекомендует
УФ-спектрофотометрию растворов в этаноле. Оптическую плотность измеряют при 255, 258 и 262 нм. В тех же условиях измеряют УФ-спек- тры стандартного образца и рассчитывают содержание примидона.
Применение. Примидон применяют подобно бензоналу в качестве противосудорожрожного средства. Выраженным снотворным действием не обладает. Выпускают в таблетках по 0,125 и 0,25 г.
ПРОИЗВОДНЫЕ ПИРИМИДИН-2,4-ДИОНА (УРАЦИЛА)
Урацил и его гомолог тимин являются нуклеиновыми основаниями, входящими в состав нуклеиновых кислот в виде нуклеозидов и нуклеотидов. На основе урацила и тимина путем модификации их структуры синтезирован ряд лекарственных веществ, являющихся метаболи-тами (метилурацил) и антиметаболитами (фторурацил, фторафур, цитарабин)
116
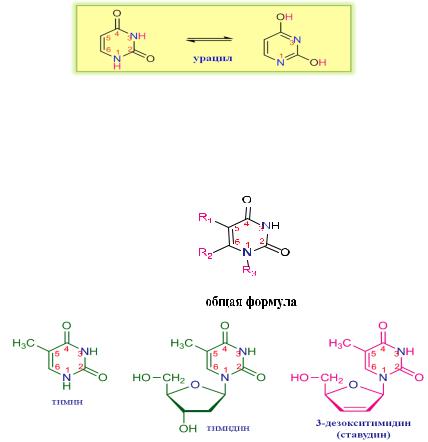
нуклеиновых оснований. Препараты-антиметаболиты ингибируют синтез ДНК и применяются как противоопухолевые средства.
Урацил (1,2,3,4-тетрагидропиримидиндион) подобно барбитуратам может существовать в виде двух таутомерных форм (лактам-лактимная таутомерия):
Лекарственные вещества, производные урацила, могут содержать в молекуле атом фтора (R1), метильный радикал (R1 или R2). Некоторые из них представляют собой пиримидиновые нуклеозиды – синтетические аналоги входящих в состав нуклеиновых кислот производных пиримидинового основания – тимина. Они содержат в молекуле остаток моносахаридов (R3) и являются производными 3-дезокситимидина:
Наиболее широко применяют в медицинской практике производные урацила: фтор-урацил, метилурацил и нуклеозиды: тегафур (фторафур), зидовудин (азидотимидин), ставудин (3-дезокси-тимидин).
Синтез производных урацила основан на циклизации алифатических соединений. Исходные продукты получения фторурацила – натрийформилфторуксусный эфир и 5-метилизо-тиомочевина. Образующийся при их конденсации 2-метилтио-5-фторурацил превращается в 5-фто-
117
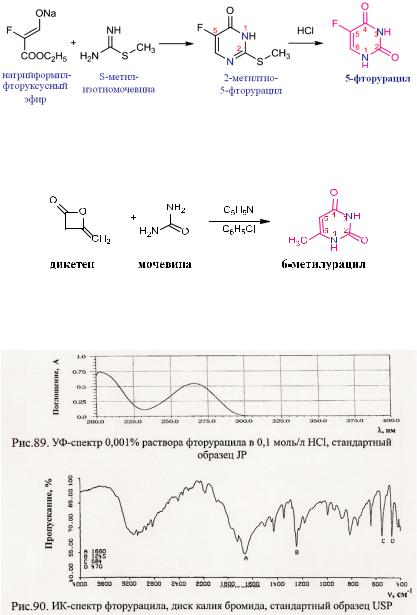
рурацил в результате гидролиза в растворе хлороводородной кислоты (см. схемы 5):
Схема 5. Синтез 5-фторурацила
6-Метилурацил с хорошим выходом (64-65%) можно получить при нагревании смеси эквимолекулярных количеств мочевины и дикетена в хлорбензоле в присутствии пиридина (см. схемы 6):
Схема синтеза 6-метилурацила
Химическое строение 5-фторурацила установлено данными УФ-, ИК- и ПМР-спектров (см. рис. 89-91).
118
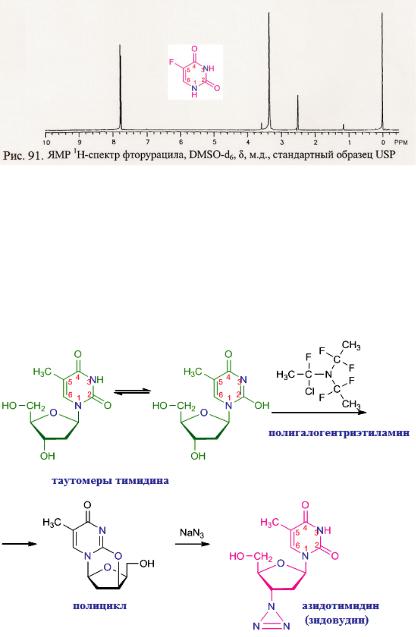
Азидотимидин (зидовудин) – первый противовирусный препарат из группы нуклеозидов. Он был синтезирован в 1964 г (см. схемы 7) при поиске противоопухолевых средств, но оказался эффективным при лечении СПИДа.
Тимидин в присутствии полигалогентриэтиламина подвергают внутримолекулярной этерификации – циклизации. В ней участвует гидроксил иминольного таутомера и гидроксильная группа дезоксирибозы. На образовавшийся полицикл действуют азидом натрия. Внутримолекулярная эфирная группа раскрывается и азидная группа оказывается в прежнем стереохимическом положении:
Схема 7. Синтез азидотимидина
119
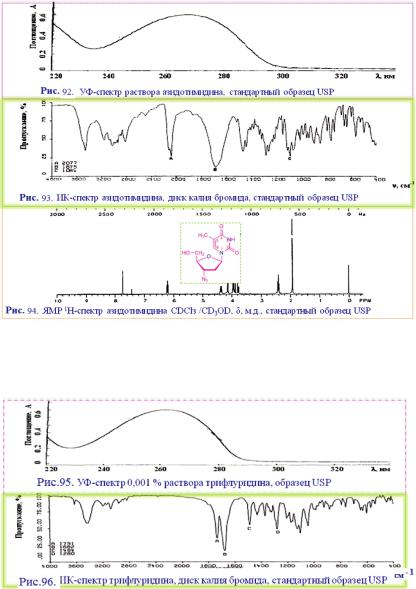
Строение азидотимидина (зидовудина) и его физико-химические свойства подтверждены данными УФ-, ИК- и ЯМРспектров (см. рис. 92-94).
Строения и физико-химические свойства некоторых других лекарственных веществ данного ряда установлены аналогичными спектральными методами (см. рис. 95-106).
120