Материал: спектр и фотометр
ЛВ – лекарственные вещества ЛС – лекарственные средства СО – стандартный образец
РСО – рабочий стандартный образец ГСО – государственный стандартный образец ЛФ – лекарственные формы ТСХ – тонкослойная хроматография
ГЖХ – газожидкостная хроматография ВЭЖХ – высокоэффективная жидкостная хроматография
6
ЧАСТЬ I. ПРИМЕНЕНИЕ СПЕКТРАЛЬНЫХ МЕТОДОВ
ВФАРМАЦЕВТИЧЕСКОМ АНАЛИЗЕ
1.1.ОСНОВНЫЕ ПОНЯТИЯ И ОПРЕДЕЛЕНИЯ
Каждое вещество поглощает электромагнитное излучение, колебания которого имеют строго определенные частоты. Электромагнитное излучение имеет двойственную природу – оно обладает волновыми и корпускулярными свойствами. Излучение и поглощение энергии происходит квантами, энергия которых описывается уравнением
∆E = hν = h (с/λ),
где h – постоянная Планка (6,5·10-27 эрг. с); v – частота колебаний; с – скорость света в пустоте (3·1010 см/с); λ – длина волны.
Из уравнения следует, что энергия кванта пропорциональна частоте колебания и обратно пропорциональна длине волны. Частота колебаний имеет размерность с-1 или Гц (герц), длина волны – размерность длины и выражается в долях метра: см, мкм (10-6 м), нм (10-9 м), иногда в ангстремах
(1 А = 10-10 м).
Для характеристики излучения часто используется волновое число ν: ν' = l/λ = (1/с) v
т. е. число волн, приходящихся на 1 см длины светового луча. Размерность ν – см-1. Волновое число прямо пропорционально ча-
стоте; шкала волновых чисел прямо пропорциональна энергии квантов излучения. С помощью специальных устройств может быть получено излучение, имеющее определенную длину волны и, соответственно, одинаковую энергию квантов. Такое излучение называется монохрома-
тическим.
Другой характеристикой электромагнитного излучения является его интенсивность, связанная с количеством квантов, проходящих в единицу времени через единицу площади. Интенсивность поглощения монохроматического излучения, проходящего через вещество, определяется законом Бугера – Ламберта – Бера:
Ig (Io/I) = kn
где Io – интенсивность падающего света; I – интенсивность прошедшего света; n – число молей поглощающего вещества на пути све - тового потока; k – постоянная, определяемая природой поглощающего вещества.
7
Для растворов вещества в прозрачном в данном интервале частот растворителе то же уравнение имеет вид
lg (Io/I) = εCl
где l – толщина слоя раствора, или длина светового пути, см; С – кон-
центрация вещества, моль/л; ε – мольный коэффициент: поглощения,или коэффициент экстинкции, л/ (моль/см).
Мольный коэффициент поглощения характеризует поглощение раствора, концентрация которого равна 1 моль/л, в кювете с длиной светового пути 1 см. В спектроскопии этот коэффициент принят как мера интенсивности поглощения данным веществом монохроматического света. Величина ε зависит от природы вещества и длины волны поглощаемого света. Иногда в качестве меры интенсивности поглощения используется процент пропускания, или (I/I0)*100.
От закона Бугера – Ламберта – Бера возможны отклонения, если а) молекула может существовать в различных таутомерных формах (например, в случае кето-енольной таутомерии); б) молекулы вещества могут взаимодействовать друг с другом или с молекулами растворителя, например, с образованием водородной связи.
Электромагнитные колебания охватывают большой интервал длин волн – от километров (для радиоволн) до 10-8 см (для жёсткого рентгеновского излучения).
Поглощение электромагнитного излучения связано с определенными изменениями в молекуле вещества, точнее, с ее переходом на более высокий энергетический уровень. Внутренняя энергия молекулы квантована. В связи с этим количество поглощаемой энергии может иметь только строго определенные значения, т. е. поглощается излучение только определенной частоты. Поглощение излучения, а следовательно, и энергии происходит в том случае, если квант излучения соответствует разности между двумя энергетическими уровнями облучаемого вещества.
Область интенсивного поглощения излучения называется полосой, а совокупность полос представляет собой спектр поглощения.
Каждый тип изменений энергетических уровней молекулы происходит в определенной области частот колебаний. Например, в органической химии для исследования строения молекул чаще всего используются следующие области, различающиеся энергией квантов:
а) наибольшая энергия требуется для возбуждения электронов, эта энергия соответствует излучению в ультрафиолетовой и видимой обла-
сти (электронная спектроскопия);
б) меньшие затраты энергии необходимы для изменения колебательных уровней молекулы, связанных с изменением длин связей и углов
8
между атомами; такие изменения вызывают поглощение в инфракрасной области (колебательная спектроскопия);
в) ещё меньшая энергия необходима для переориентации спинов ядер, которая может вызываться квантами радиочастотного излучения
(спектроскоnия ядерного магнитного резонанса).
С точки зрения энергии переходов в молекуле принципиальной разницы между ультрафиолетовой и видимой областью нет. Выделение видимой части спектра в самостоятельную область обусловлено субъективными причинами – границами восприятия электромагнитного излучения человеческим глазом.
Поглощение называется характеристическим, если оно вызывается определенной группой атомов, причем характер поглощения относительно мало изменяется с изменением остальной части молекулы.
Наличие в спектрах характеристических полос поглощения позво-
ляет обнаружить в веществе определенные структурные элементы. Таким образом, наиболее широко используемыми в фармацевтиче-
ской химии и технологии спектральными методами являются УФ-спек- троскопия, ИК-спектроскопия и спектроскопия ЯМР. В настоящее время эти физические методы включены в Фармакопеи России XII издания. Для установления строения органических веществ большое значение имеет также масс-спектрометрия (этот метод основан на принципах, отличающихся от описанных выше). В дальнейшем будут рассмотрены основы каждого из вышеназванных методов.
1.2. ЭЛЕКТРОННАЯ (УЛЬТРАФИОЛЕТОВАЯ) СПЕКТРОСКОПИЯ
Поглощение органическими веществами электромагнитных колебаний в ультрафиолетовой (200-400 нм) и видимой (400-800 нм) области обусловлено переходом электронов со связывающих орбиталей на разрыхляющие орбитали. Такое состояние молекулы называется возбуждённым. При взаимодействии с квантом света, поглощая энергию, электрон может переходить с высшей заполненной орбитали на низшую вакантную орбиталь. Электроны достаточно прочно удерживаются ядром, поэтому для их возбуждения требуются большие энергии и, следовательно, электромагнитное излучение, имеющее малые длины волн (120-800 нм). В УФ-области поглощают все органические вещества. Длины волн менее 190 нм (дальняя, или вакуумная, область УФ-спектра) малопригодны для работы, так как в этой области поглощают компоненты воздуха – кислород и азот. Приборы для исследований в интервале длин волн 120 – 190 нм с вакуумными камерами существуют, однако они сложны и редко
9
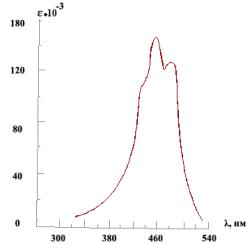
используются в обычной лабораторной практике. Для волн длиной более 200 нм воздух прозрачен, что делает ближнюю ультрафиолетовую и видимую области спектра (200-800 нм) удобными для измерений. В том же интервале прозрачен кварц, который в УФ-спектроскопии применяется как оптический материал для изготовления призм и кювет. Приборы для получения спектров поглощения в этой области просты и доступны. Необходимые для исследования количества вещества невелики – около 0,1 мг. В связи с этим УФ-спектроскопия в настоящее время является одним из наиболее распространенных физических методов исследования органических соединений. Обычно спектр поглощения записывается в виде зависимости интенсивности поглощения ε (или её логарифма) от длины волны λ (см. рис. 1).
Рис. 1. УФ-спектр транс-β-каротина
Электроны в атомах и молекулах занимают орбитали со строго определенной энергией. Уровень энергии атомных орбиталей определяется соответствующим набором квантовых чисел. Молекулярные орбитали (МО) могут рассматриваться как линейные комбинации атомных. Упрощённо это можно представить как перемещение электронов со связывающих σ- и π- и несвязывающих n-МО на разрыхляющие σ* – и π*-MO.
Возможны четыре типа электронных переходов: σ→σ*,n→σ*,n→π* и π → π* (см. рис. 2). Электроны на несвязывающей МО не участвуют в образовании связей, поэтому соответствующих им разрыхляющих орбиталей не существует. Переход n-электрона при поглощении света может происходить на σ*- и π*-MO.
10