Материал: спектр и фотометр
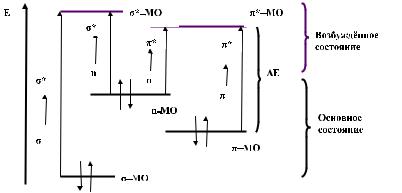
Поглощение света молекулой осуществляется избирательно: поглощаются те кванты света, энергия которых равна разности энергий (∆E) между орбиталями основного и возбуждённого состояний (см. рис. 2). Чем меньше эта разность, тем больших длин волн поглощается свет. Наибольшая энергия требуется для осуществления σ→ σ* электронного перехода. Поэтому соединения, у которых имеются только σ-связи, например алканы и циклоалканы, не поглощают свет в рабочем интервале серийных УФ-спектрофотометров (200-800 нм). В связи с этим они могут использоваться в качестве растворителей при снятии УФ-спектров других соединений. Аналогичное применение находят насыщенные соединения, содержащие гетероатомы с неподеленными парами электронов (О, N, S, галогены). Хотя в их спектрах возможно проявление n-σ* перехода, максимум поглощения в таких соединениях, как спирты, простые эфиры, хлоралканы все же не превышает 200 нм.
Рис. 2. Типы электронных переходов при поглощения света
Способность поглощать свет представляет собой суммарное свойство всех связей молекулы в целом. Однако некоторые полосы поглощения в УФ-спектре можно отнести к электронным переходам в отдельных структурных фрагментах молекулы, называемых хромофорами (табл. 1). К ним относятся многие функциональные группы, в которых атом с неподелённой парой электронов связан с соседним атомом кратной связью. В таких группах, кроме σ→ σ*, возможны еще два электронных перехода: π → π* и n→ π*. Если π → π* переход в изолированных хромофорах всегда находится в дальней УФ-области (<200 нм), то n→ π* переход уже проявляется, в ближней УФ-области и может быть использован в практических целях. Например, очень важно значение переходов π → π* и n→ π*, поскольку только им соответствуют длины волн, попадающие
11
в рабочий диапазон прибора. Исключение составляют переходы π → π* изолированных двойных связей С = С и C=N, а также тройных связей
С≡С и C≡N (λmax 160-180 нм). Для изолированных кратных связей в используемом для измерений интервале проявляется только переход
карбонильной группы C=O (λmax ~ 270 им).
Основными хромофорами, дающими максимум поглощения в области 200-800 нм, являются системы сопряженных двойных связей (см. табл. 1). С ростом числа сопряженных двойных связей энергия, необходимая для возбуждения электронов, будет уменьшаться, и поглощение света будет наблюдаться при больших длинах волн. В ароматических системах переход электрона в возбужденное состояние осуществляется также при меньшей затрате энергии, чем в случае изолированной двойной связи. Таким образом, основными хромофорами в УФ-спектроскопии являются сопряженные С=С-связи, карбонильная группа С=О, системы С=С – С =О, ароматическое ядро.
|
|
|
|
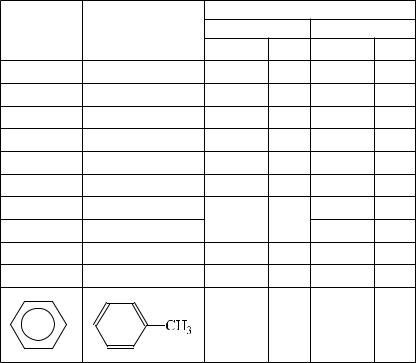
Таблица 1 |
|
Электронные переходы в изолированных и сопряженных хромофорах |
|||||
|
|
|
Тип переходов |
|
|
Хромофор |
Соединение |
π → π* |
|
π → π* |
|
|
|
λ макс, нм |
ε макс |
λ макс, нм |
ε макс |
С=С |
H2C=CH2 |
165 |
15000 |
|
|
C≡C |
HC≡CH |
173 |
6000 |
|
|
C=O |
CH3-CO-CH3 |
187 |
1000 |
271 |
16 |
=C=N- |
CH3-CH=N-OH |
190 |
8000 |
279 |
15 |
-NO2 |
CH3-NO2 |
210 |
15000 |
271 |
19 |
C=C-C=C |
H2C=CH-CH=CH2 |
217 |
20900 |
|
|
C=C-C= |
H2C=CH- |
256 |
22400 |
|
|
=C-C=C- |
-HC=CH-CH=CH2 |
|
|
||
|
|
|
|
||
C=C-C=O |
H2C=CH-CHO |
230 |
12600 |
327 |
40 |
|
|
207 |
7000 |
|
|
|
|
261 |
225 |
|
|
|
|
12 |
|
|
|
УФ-спектр органического вещества характеристичен, так как поглощение определяется только собственно хромофором и его ближайшим окружением, т. е. один и тот же хромофор проявляется практически одинаково как в исключительно простых, так и самых сложных молекулах. В зависимости от непосредственного окружения одной и той же хромофорной группировки положение максимума поглощения в УФ-спектрах различных соединений может несколько изменяться. Сдвиг максимума в сторону более длинных волн принято называть батохромным сдвигом, а сдвиг сторону более коротких волн – гипсохромным.
Интенсивность поглощения в спектре связана с вероятностью данного типа электронного перехода. Однако далеко не все переходы, формально кажущиеся возможными, осуществляются в действительности. Существуют так называемые правила отбора, определяющие разрешенные и запрещенные переходы. Эти правила учитывают в основном симметрию молекулы, а также электронную симметрию основного и возбужденного состояний; запрещены переходы, при которых происходит изменение спина электрона. Интенсивность поглощения, соответствующего разрешенным переходам, обычно высока, мольный коэффициент погашения достигает тысяч, а иногда и сотен тысяч единиц, тогда как для запрещенных переходов значение ε составляет десятки, реже – сотни единиц. Спектрометры для получения УФ-спектров имеют следующее устройство (см. рис. 3 и 4).
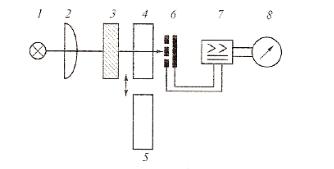
Рис. 3. Схема фотометрического однолучевого прибора с прямым способом измерения:
1 – источник света; 2 – линза; 3 – светофильтр или монохроматор; 4 – кювета с раствором сравнения; 5 – кювета с фотометрируемым раствором;
6 – фотоэлемент; 7 – усилитель; 8 – регистрирующий прибор
На рисунках 5-7 представлены некоторые спектрофотометры, отвечающие требованиям современной науки и практики.
13
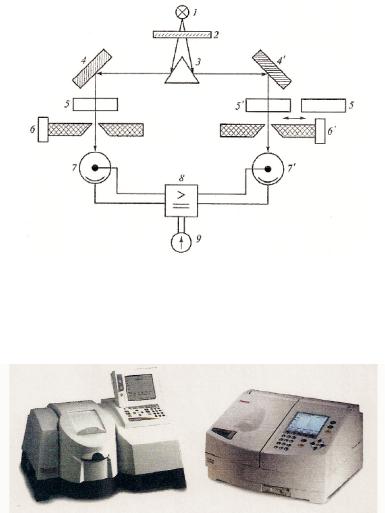
Рис. 4. Схема фотометрического двулучевого прибора с компенсационным способом измерения:
1 – источник света; 2 – светофильтр; 3 – призма; 4, 4’ – зеркала; 5, 5’ – кюветы с раствором сравнения и фотометрируемым раствором
соответственно; 6, 6’ – щелевые диафрагмы; 7, 7’ – фотоэлементы; 8 – усилитель; 9 – нуль-индикатор
Рис. 5. УФ/Вид. |
Рис. 6. УФ/Вид. |
спектрофотометры Evolution |
спектрофотометры Helios |
• Исследовательского класса, |
• Опыт производства (Unicam) |
точные и простые в использовании |
спектрофотометров более 50 лет |
спектрофотометры |
• Надежные и недорогие |
с широким набором приставок |
для использования в учебных |
• Идентификация и количественный |
и заводских лабораториях |
анализ химических |
|
и биологических веществ |
|
14

Рис. 7. UV-Vis спектрофотометр
•Совершенная конструкция, отвечающая требованиям фармакопеи США и европейских стран.
•Минимальное количество движущихся частей (только вентилятор и шторка для проверки настройки длин волн и темного тока)
•Широкодиапазонная диодная матрица
диапазон длин волн: 190-1100 нм; разрешающая способность: 1 нм; скорость сканирования 0,1 сек;
•Удобство и надежность эксплуатации.
•Обеспечение быстрых измерений, обработки данных и распечатки результатов.
•Программное обеспечение для автоматической метрологической аттестации всей системы.
•Универсальное программное обеспечение для качественного и количественного анализа.
•Возможность обработки спектров с использованием 17 математических функций.
•Расширение возможностей для биохимического анализа.
•Стандартная проверка чистоты нуклеиновых кислот; количественное определение содержания нуклеиновых кислот и белков в смесях.
•Различные варианты кинетических исследований.
•Возможность проведения исследований денатурации под тепловым воздействием (определение точки плавления ДНК или конформационных изменений белков).
15