Материал: спектр и фотометр
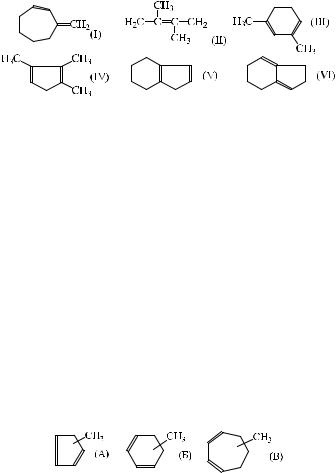
фигурацией системы двойных связей УФ-спектр может быть вычислен с использованием поправок для λmax ±18 и для ε ±12 000. Ниже приведены структуры диенов к примерам 3-8:
Пример 3. Рассчитайте предполагаемые параметры УФ-спектра для 3-метиленцикло-гептена-1 (диен 1).
Решение. В таблице 2 находим данные для изомерного 1-метилцикло-
гептадиена-1,3: λmax 257 нм (ε 7600). Для диена (1)λmax = 257-18 = 239 ± 2 нм; ε= 7600 + 12000 = 20 000 ±1000.
Определенное влияние на положение максимума поглощения в УФ-спектре сопряжённых диенов оказывают алкильные заместители, находящиеся при системе двойных связей, что легко объясняется эффектом сверхсопряжения. Характер этого влияния определяется правилом Вудворда: введение дополнительной алкильной группы вне системы двойных связей практически не отражается на положении максимума поглощения; наличие дополнительной алкильной группы в положении 1 (или 4) диеновой системы вызывает батохромный сдвиг максимума поглощения на 7-10 нм, а в положении 2 (3) – на 3-4 нм (см. табл. 3).
Таблица 3
Положение максимума поглощения (λmax , нм) в УФ-спектрах метилзамещенных циклических диенов (А–В)*
Положение заместителя |
А λ макс, нм |
Б λ макс, нм |
В λ макс, нм |
|
|
|
|
5- |
241 |
259 |
249 |
|
|
|
|
1- |
249 |
265 |
257 |
|
|
|
|
2- |
243 |
261 |
252 |
* Значения ε макс для незамещённых диенов приведены в табл. 2
21
На этом основании положение максимума поглощения для многих сопряженных диенов может быть рассчитано с достаточной степенью точности (до ± 5 нм). Такой расчёт производится следующим образом: в таблице 2 выбирают УФ-спектр незамещённого диена данного типа (основного хромофора) и на каждый алкильный заместитель в положении 1
(4) добавляют по 8 нм, а на каждый заместитель в положении 2 (3) – по 4 нм. Пяти- и шестичленное кольцо, примыкающее к диеновой системе, рассматривается как два алкильных заместителя (с введением тех же поправок). Ниже приводятся примеры таких вычислений.
Пример 4. Вычислите λmax для диена (II).
Решение. Соответствующий хромофор – бутадиен-1,3 (табл. 2): λmax
217 нм. Для диена (II): λmax = 217 +(4·2)= 225 нм (найдено: 226 нм).
Пример 5. Вычислите λmax для диена (III).
Решение. Соответствующий хромофор – циклогексадиен-l,3 [табл. 2, (6)]: λmax 258 нм. Для диена (Ш): λmax = 258 + 8 + 4 = 270 нм (найдено: 265 нм).
Пример 6. Вычислите λmax для диена (IV).
Решение. Соответствующий хромофор – циклопентадиен-l,3 [табл. 2, (3)]: λmax 240 нм. Для диена (lV):λmax = 240 + 8 +(2.4) = 256 нм (найдено: 253 нм).
Пример 7. Вычислите λmax для диена (V).
Решение. Соответствующий хромофор – циклопентадиен-1,3 [ табл. 2, (3)]: λmax 240 нм. Для диена (V):λmax = 240 + 8 + 4= 253 нм (найдено: 251 нм).
Пример 8. Вычислите λmax для диена (VI).
Решение. Соответствующий хромофор – 3-метиленциклопентен-l
[табл.2 (2)]: λmax = 234 нм. Для диена (VI): λmax = 234 + 8 + 4 = 246 нм
(найдено: 245 нм).
Отклонения вычисленных значений от найденных значительны для полизамещенных диенов. В подобных случаях, особенно в диенах, содержащих громоздкие заместители, возможны искажения стереохимии молекулы: выход диеновой системы из одной плоскости (нарушение копланарности) и ослабление взаимодействия двойных связей, вызывающее гипсохромовый сдвиг максимума поглощения. Нарушение копланарности особенно характерно для ациклических диенов ввиду свободного вращения вокруг связи С2–С3 диеновой системы.
Прочие заместители, в том числе и содержащие гетероатомы с неподелёнными парами электронов, оказывают на положение максимума в УФ-спектре диена меньшее и менее характерное влияние, чем алкиль-
22
ные группы. Например, в случае бутадиена-l,3 батохромный сдвиг максимума составляет (в нм): 9 (СН3), 5 (CI), 6 (ОСНз), 0 (СНзСОО) и 1 [N(СН3)2] при наличии указанного заместителя в положении 1 диеновой системы.
Таким образом, УФ-спектр позволяет обнаружить в исследуемом веществе диеновую систему и сделать определенные выводы о ее конфигурации и степени замещённости, однако эти выводы являются скорее предположениями, чем доказательствами.
Сопряжённые двойная и тройная связь образуют хромофор, УФспектр которого близок к спектру соответствующего диена.
1.3.2. Полиеноные системы.
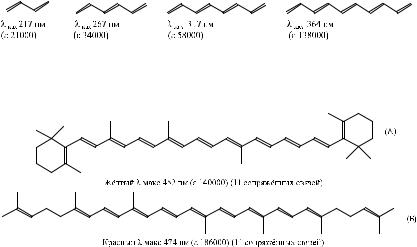
Увеличение длины цепи сопряжения приводит к батохромному сдвигу максимума поглощения в УФ-спектре и значительному возрастанию мольного коэффициента погашения. При последовательном удлинении цепи сопряжения λmax смещается примерно на 50, 40, 30, 25 и далее на 20 нм для каждой дополнительной двойной связи, например:
При большом числе сопряженных двойных связей максимум поглощения попадает в видимую область и вещество становится окрашенным как, например, β-каротин (А), ликопин (Б) и им подобные структуры:
Для полиенов, содержащих четыре и более двойных связей удаётся различить тонкую структуру максимума. Расстояние между отдельными полосами, образующими этот максимум, составляет 9-15 нм и соответствует частоте валентных колебаний системы двойных связей в ИК-спектре.
Интерпретация УФ-спектров полиенов, как правило, более сложна, чем в случае диеновых систем. Для замещенных полиенов изменение
23
конфигурации хотя бы одной двойной связи (в частности, за счет явления цис-транс-изомерии) может вызвать в спектре значительно большие изменения, чем поправка на введение дополнительных заместителей.
Таким образом, по данным УФ-спектра в исследуемом веществе удается надежно установить присутствие полиеновой системы и ориентировочно определить число двойных связей, находящихся в сопряжении.
1.3.3. Карбонильная группа.
Для УФ-спектров предельных альдегидов и кетонов характерна полоса λmax 275-290 нм, соответствующая π→π*-переходу. Переход является запрещенным по симметрии, поэтому максимум очень слабый (ε 15-20). Для ациклических альдегидов [λmax (в гексане) 290 нм] и ациклических кетонов [λmax (в гексане) 279 нм] характер замещения практически не сказывается на положении полосы. Для циклических кетонов положение максимума в значительной степени зависит от размера цикла (λmax, в гексане):
циклобутанон 280 нм циклопентанон 300 нм
циклогексанон, циклогептанон 292 нм.
Для альдегидов и кетонов на положение полосы поглощения существенно влияет природа растворителя. В полярных растворителях и особенно в растворителях, способных образовывать с карбонильной группой водородную связь, наблюдается гипсохромный сдвиг максимума поглощения, так как водородная связь понижает энергетический уровень n-орбитали. Средние поправки для определения положения λmax при использовании разных растворителей составляют (в нм): этанол (О), вода (-7), углеводороды (+ 11), диоксан (+5). В кислой среде полоса поглощения в УФ-спектрах альдегидов и кетонов полностью исчезает, так как неподелённая пара атома кислорода присоединяет протон. Это убедительно доказывает, что данная полоса относится именно к n→π*-переходу.
Вследствие исключительно малых значений ε для предельных альдегидов и кетонов возникают определенные трудности при идентификации карбонильной группы в исследуемых веществах и в проведении количественного анализа этих соединений методом УФ-спектроскопии.
В УФ-спектрах α,β-непредельных альдегидов и кетонов наблюдается интенсивная полоса перехода π→π* и слабая полоса запрещенного перехода n→π* карбонильной группы. По сравнению со спектрами предельных альдегидов и кетонов последняя полоса сильно смещена в длинноволновую область. Введение каждого следующего алкильного за-
24
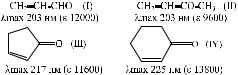
местителя к двойной связи α,β-непредельного альдегида или кетона как в α-, так и в β-положение вызывает батохромный сдвиг максимума поглощения основного (π→π*) перехода на ~ 10 нм. Это дает возможность в простейших случаях рассчитать положение основной полосы, учитывая данные для основных хромофоров (I) – (IV):
УФ-спектры α,β-непредельных кетонов столь же чувствительны к изменению растворителя, как и спектры предельных кетонов. Характер смещения полосы перехода n→π* одинаков с описанным выше для предельных карбонильных соединений. Полоса перехода: π→π* в более полярном растворителе смещается в сторону более длинных волн (до 10 нм) вследствие того, что в полярном растворителе в большей степени проявляется разделение зарядов и, соответственно, облегчается переход π-электронов в возбужденное состояние. Таким образом, с ростом полярности растворителя две полосы поглощения α,β-непредельных альдегидов и кетонов смещаются в разные стороны – происходит их сближение. Примером могут служить УФ-спектры 4-метилпентен-3-она-2 (окиси мезитила), полученные в разных растворителях:
(СНЗ)2С=СН-СО-СНЗ
λmax (в этаноле) 236 нм (ε 10 600), 310 нм (ε 52) λmax (в изооктане) 231 нм (ε 11 900), 321 нм (ε 38)
Простые альдегиды и кетоны очень слабо поглощают в УФ-области около 280 нм. В этом поглощении участвуют электроны не двойной связи, а не связывающие электроны карбонильного кислорода; поскольку этих электронов нет в двойной углерод-углеродной связи, алкены не проявляют такого поглощения. Карбонильные группы, сопряженные с двойной связью или ароматическим кольцом, поглощают значительно сильнее в УФ-области. Несопряженные альдегиды и кетоны дают только слабую полосу поглощения, но при наличии сопряжения с бензольным кольцом поглощение сильно возрастает (см. рис. 10).
Таким образом, наличие группировки α,β-непредельного альдегида или кетона отно-сительно легко определяется по данным УФ-спектра соединения, при этом определенные предположения могут быть высказаны о наличии заместителей при двойной связи.
25