Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
аминокислоты |
Аминокислоты |
|
|
ВВЕДЕНИЕ. Аминокислоты стали получать в промыш- |
|||
|
|||
|
ленности около 50 лет назад, после того как были |
||
|
изучены важнейшие этапы обмена веществ. |
||
|
После этого некоторые аминокислоты стали исполь- |
||
и |
зоваться в медицине, например для приготовления |
||
инфузионных растворов, другие (L-метионин, L-лизин |
|||
кислоты |
|||
и L-треонин) – в качестве кормовых добавок. Объем |
|||
|
|||
|
производства аминокислот значительно увеличился с |
||
|
тех пор, как было обнаружено, что L-глутамат может |
||
Спирты, |
усиливать вкус, а дипептид аспартам обладает выра- |
||
организме, а должны поступать вместе с пищей (не- |
|||
|
женным сладким вкусом. Молекулы всех белков по- |
||
|
строены из 20 протеиногенных аминокислот. Некото- |
||
|
рые аминокислоты не могут синтезироваться в |
||
|
заменимые аминокислоты). Для человека и многих |
||
|
сельскохозяйственных животных |
незаменимыми |
|
|
аминокислотами являются L-метионин, L-лизин, аро- |
||
|
матические аминокислоты (L-фенилаланин, L-тиро- |
||
|
зин, L-триптофан) и гидрофобные аминокислоты |
||
|
(L-валин, L-лейцин и L-изолейцин). В природе также |
||
|
встречаются «небелковые» аминокислоты, например |
||
|
D-изомеры аминокислот. Их используют в синтетиче- |
||
|
ской химии, в том числе при производстве полусинте- |
||
|
тических антибиотиков. |
|
|
|
ЭКОНОМИЧЕСКИЙ АСПЕКТ. Производство амино- |
||
|
кислот составляет более 2 000 000 т/год, что оце- |
||
|
нивается в сумму более 4 млрд долларов США. |
||
|
Значительная часть предприятий, |
производящих |
|
|
аминокислоты, расположена в азиатском регио- |
||
|
не. Лидирует производство L-глутамата натрия |
||
|
(более 1 500 000 т/год), за ним следуют производ- |
||
|
ства L-лизина (700 000 т/год) и L-метионина |
||
|
(600 000 т/год). L-Аспарагиновая кислота и L-фени- |
||
|
лаланин – сырье для получения подсластителя ас- |
||
|
партама – производятся в количествах 10 000 т/год. |
||
|
Около 65% производимых аминокислот использу- |
||
|
ются в пищевой промышленности, 30% – как кормо- |
||
|
вые добавки для скота и лишь 5% аминокислот по- |
||
|
сле дополнительной очистки применяют в |
||
|
медицинских целях, прежде всего для инфузионных |
||
|
растворов, а также в производстве косметических |
||
|
препаратов. |
|
|
|
ПОЛУЧЕНИЕ. Существует четыре |
промышленных |
|
|
метода получения аминокислот: 1) экстракция из |
||
|
гидролизата белка; 2) химический синтез; 3) био- |
||
|
трансформация соединений-предшественников в |
||
|
ферментере или клеточном реакторе; 4) микробная |
||
|
ферментация. |
|
|
|
Экстракцией из белкого гидролизата в промыш- |
||
|
ленности получают прежде всего L-цистеин, L-цис- |
||
|
тин, L-лейцин, L-аспарагин, L-аргинин и L-тирозин. |
||
|
В качестве сырья используют растительные белки |
||
30 |
или отходы мясной промышленности, которые под- |
||
вергают кислотному гидролизу, после чего путем |
|||
кристаллизации или экстракции спиртом отделяют гидрофобные аминокислоты L-фенилаланин, L-лей- цин и L-изолейцин. Затем проводят ионообменную хроматографию, разделяя растворимые аминокислоты на основную, кислую и нейтральную фракции, которые далее перекристаллизовывают и подвергают хроматографической очистке. Химический синтез аминокислот всегда приводит к образованию рацемата (смеси L- и D-изомеров аминокислот), который также находит применение. Например, L,D-метионин применяется в качестве кормовой добавки, L,D-ала- нин добавляют во фруктовые соки для смягчения вкуса. Для разделения рацематов аминокислот на L- и D-изомеры в молекулу аминокислоты вводят еще один хиральный центр при Сα-атоме. Такие реакции биотрансформации осуществляют в ферментере или клеточном реакторе. Биокатализатором могут служить очищенные ферменты или целые клетки, содержащие необходимый фермент. Экономически выгодно использовать иммобилизованные биокатализаторы, которые позволяют проводить реакцию непрерывно в течение длительного срока. Успех промышленного получения аминокислот объясняется тем, что химический синтез соединений-предшест- венников относительно дешев. Кроме того, для производства практически всех протеиногенных аминокислот разработаны методы ферментации, и имеются штаммы, позволяющие получать большие количества продукта. Во многих случаях такой подход экономически оправдан. Широко используются штаммы, усовершенствованные методами генетической инженерии. К настоящему времени закончено секвенирование генома Corynebacterium glutamicum. Полученная генетическая информация поможет ускорить создание новых высокопродуктивных штаммов. Во многих случаях уже клонированы целые опероны, ответственные за биосинтез аминокислот. Изучаются возможности управления обменом веществ клетки методами так называемой метаболической инженерии.
Аминокислоты, получаемые промышленным путем
Аминокислота |
|
Объем |
Цена, |
Метод получения |
Основные применения |
|
|
произ- |
доллар |
|
|
|
|
водства, |
США/кг |
|
|
|
|
т/год |
|
|
|
Протеиногенные аминокислоты |
|
|
|
||
L-Глутамат |
> 1 500 000 |
1 |
Ферментация |
Усилитель вкуса |
|
L-Лизин |
|
700 000 |
2 |
Ферментация, |
Кормовая добавка |
|
|
|
|
ферментный реактор |
|
L-Метионин |
|
600 000 |
2 |
Химический синтез |
Кормовая добавка |
L-Треонин |
|
55 000 |
5 |
Ферментация |
Кормовая добавка |
L-Аспартат |
|
15 000 |
10 |
Хиральный пул, биореактор |
Аспартам™ |
L-Глицин |
|
15 000 |
10 |
Химический синтез |
Подсластитель |
L-Фенилаланин |
|
10 000 |
10 |
Ферментация, |
Аспартам™, медицина |
|
|
|
|
ферментный реактор |
|
L-Аргинин |
|
1 000 |
20 |
Ферментация, хиральный пул |
Медицина, косметика |
L-Триптофан |
|
1 400 |
20 |
Ферментация, |
Кормовая добавка |
|
|
|
|
ферментный реактор |
|
Другие аминокислоты |
5 000 |
|
Хиральный пул, ферментация, |
Медицина и др. |
|
|
|
|
|
ферментный или биореактор |
|
Небелковые аминокислоты |
|
|
|
||
D-Фенилглицин, D- гидроксифенилглицин |
Химический синтез |
Предшественники ампи- |
|||
|
|
|
|
|
циллина и амоксициллина |
Гидрокситриптофан |
|
|
|
Химический синтез |
Антидепрессант |
|
|
|
|
|
Окситриптан™ |
|
|
|
|
|
|
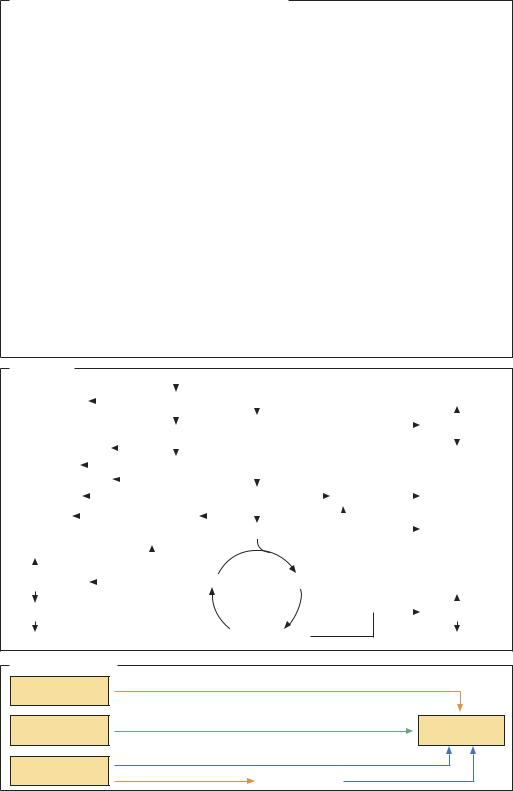
Биосинтез
Гистидин (C6N3) |
|
|
|
|
|
|
|
|
|
Глюкоза (C6) – источник углерода |
|
Глицин (C2N) |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
Пентоза (C5) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Фенилаланин (C9N) |
|
|
Тетроза (C4) |
|
|
Триоза (C3) |
|
|
|
|
|
|
|
|
|
Серин (C3N) |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Цистеин (C3NS) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Тирозин (C9N) |
|
|
|
|
|
|
Шикимовая кислота (C7) |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
Триптофан (C11N2) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
Пируват (C3) |
|
|
|
|
(C5) |
|
|
|
|
|
|
|||||||||||
Аланин (C3N) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Валин (C5N) |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
Лизин (C6N2) |
|
|
|
|
|
Диаминопимели- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Метионин (C5NS) |
новая кислота (C7N2) |
|
Ацетил-КоА (C2) |
|
|
|
|
|
|
|
Лейцин (C5N) |
|||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Аспарагиновая |
|
|
|
|
|
|
|
Оксалоацетат (C4) |
Цитрат (C6) |
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
кислота (C4N) |
|
|
|
|
|
|
|
|
|
|
|
Пролин (C5N) |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Треонин (C4N) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Глутамат (C5N) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Изолейцин (C6N) |
2-Оксоглутарат (C5) |
Аргинин (C6N4) |
|
Методы получения |
|
|
|
Белки |
Гидролиз, разделение |
|
|
(хиральный пул) |
|
|
|
Глюкоза и другие |
Ферментация |
|
L-Аминокислоты |
источники углерода |
|
|
|
|
|
|
|
Химическое |
Ферментный или биореактор |
|
|
Химический синтез |
|
Ферментный реактор |
|
сырье |
L,D-Аминокислоты |
||
|
|
31 |
|
|
|
|
|
Спирты, кислоты и аминокислоты
32
L-Глутаминовая кислота
ВВЕДЕНИЕ. В 1908 г. японские ученые установили, что L-глутаминовая кислота, содержащаяся в водорослях Konbu, может усиливать вкус. Промышленное производство L-глутаминовой кислоты из кислотного гидролизата клейковины пшеницы и соевого белка было начато уже в 1909 г. на фирме Ajinоmoto. В 1957 г. сотрудник фирмы Киова Хакко обнаружил, что при выращивании Corynebacterium glutamicum в
сахаросодержащей среде накапливается L-глутами- новая кислота. В настоящее время в результате усовершенствования штамма и оптимизации технологии ферментации удается получать до 150 г глутамата из 1 л культуры.
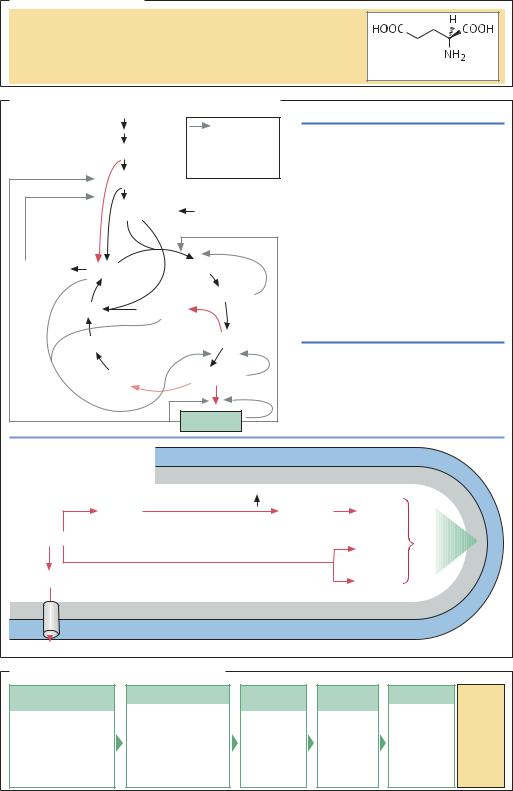
МИКРООРГАНИЗМЫ И БИОСИНТЕЗ. В клетках C. glutamicum L-глутаминовая кислота образуется при трансаминировании 2-оксоглутаровой кислоты, которая получается при окислении изолимонной кислоты в цикле Кребса. В диком штамме окисление дикарбоновых продуктов цикла Кребса строго регулируется. Изучение генома C. glutamicum и способов регуляции активности ферментов привело к созданию нового штамма, в котором: 1) возросла секреция глутамата в среду роста; 2) изменены пути регуляции активности некоторых ферментов, участвующих в биосинтезе L-глута- миновой кислоты; 3) активированы некоторые побочные пути обмена веществ.
Приведем разъяснения.
1.Количество глутамата в культуральной жидкости в большой степени зависит от скорости секреции, и, следовательно, от проницаемости цитоплазматической мембраны. Проницаемость мембран может изменяться. Например, для увеличения проницаемости ограничивают доступ биотина, жирных кислот или глицерина (для ауксотрофов по жирным кислотам или по глицерину соответственно). Добавление в среду пенициллина также приводит к повышению проницаемости клеточной стенки, так как пенициллин препятствует ее образованию.
2.В промышленных штаммах C. glutamicum активность 2-оксоглутаратдегидрогеназы значитель-
но ниже активности L-глутаматдегидрогеназы (KМ различаются примерно в 70 раз, Vmax – примерно в 150 раз).
3.К наиболее важным анаплеротическим реакциям относятся карбоксилирование фосфоенолпирувата и активация глиоксилатного цикла (в растениях
ибактериях). Обе реакции приводят к образованию оксалоацетата, предшественника цитрата, кроме того, в результате этих реакций происходит включение
дикарбоновых (С2) продуктов гликолиза в цикл лимонной кислоты. Фосфоенолпируваткарбоксилаза использует в качестве кофактора биотин, следовательно, изменяя количество биотина, можно регулировать активность фермента. Активность многих
ферментов, участвующих в глиоксилатном цикле, зависит от концентрации метаболитов, конечных продуктов, а также NH+4 и NAD+/ NADH, поэтому можно «искусственно» менять их активность. Выход продукта
вштаммах-продуцентах глутамата можно повысить методами генетической инженерии. В настоящее время геном C. glutamicum полностью расшифрован и активно изучается. В частности, исследуют зависимость выхода продукта от введения в геном мультикопийных кассет, несущих ген глутаматдегидрогеназы.
ФЕРМЕНТАЦИЯ И ПЕРВИЧНАЯ ПЕРЕРАБОТКА. В качестве сырья для производства глутамата используют мелассу или гидролизат крахмала. В оптимальных условиях культивирования высокопродуктивные штаммы C. glutamicum перерабатывают до 60–70% исходного сырья. Источником азота служат соли аммония и аммиак. При выборе условий роста необходимо оптимизировать концентрацию биотина в среде,
арН среды поддерживать в диапазоне 7,0–8,0. Для синтеза глутамата очень важна аэрация клеточной
культуры: оптимальное значение kd составляет 3,5 10–6 моль кислорода/(атм мин мл). Ферментацию в промышленных масштабах проводят в реакторах с рабочим объемом до 500 м3. Как правило, сначала проводят предферментацию, а затем ферментацию воздушно-проточным способом. Чтобы избежать ингибирования катаболитами, после образования достаточного количества клеток (14 ч роста)
всреде поддерживают постоянный уровень глюкозы, не превышающий 0,5%. После удаления клеток ультрафильтрацией глутамат выделяют из культуральной жидкости методами ионообменной или абсорбционной хроматографии (150 г/л через 60 ч роста).
ЭКОНОМИЧЕСКИЕ АСПЕКТЫ. L-Глутамат используется в основном в пищевой промышленности как усилитель вкуса, чаще всего в комбинации с нуклеозидами. В 2004 г. путем ферментации было получено 1 500 000 т L-глутамата. Рыночная стоимость L-глу- тамата составляет 1000 долларов США за тонну,
аобъем рынка достигает 1,5 млрд долларов США. Основные производства расположены в странах азиатского региона.
Copyright ОАО «ЦКБ «БИБКОМ» & ООО «Aгентство Kнига-Cервис»
L-Глутаминовая кислота |
|
|
|
|
|
|
|
|
|
|
|
|
||
С5Н9NO4 |
|
|
|
|
Код СAS 56-86-0 (L)-форма |
|
|
|
|
|||||
MR |
|
147,13 |
|
|
|
|
|
|
|
|
|
|
|
|
Тпл |
|
247–249°С |
|
|
|
|
|
|
|
|
|
|
|
|
Растворимость |
600 г/л воды |
|
|
|
|
|
(2 S)-форма, L-форма |
|
||||||
Биосинтез и штаммы-суперпродуценты глутамата |
|
|
|
|
|
|
|
|
||||||
|
Глюкоза |
|
|
|
|
|
Ферменты |
|
|
|
|
Ген |
||
|
|
|
|
Регуляция |
|
|
1 Фосфоенолпируват- |
|
|
ppc |
||||
|
|
|
|
по принципу |
|
|
|
|
||||||
|
|
|
|
|
|
карбоксилаза (PEPC) |
|
|
||||||
|
Фосфоенолпируват |
обратной |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
||||||
|
|
2 |
|
связи или |
|
|
2 Пируваткиназа |
|
|
|
pyk |
|||
|
1 |
|
репрессия |
|
|
3 Пируваткарбоксилаза |
|
pyk |
||||||
|
Пируват |
|
|
|
|
|
|
|||||||
|
|
4 |
|
|
|
|
|
|
4 Пируватдегидрогеназа |
|
pdh |
|||
|
Ацетил-КоА |
Ацетат |
|
|
|
5 Цитратсинтаза |
|
|
|
gltA |
||||
|
3 |
|
|
|
|
|
|
|
6 Aконитаза |
|
|
|
citB |
|
|
|
|
5 |
|
|
|
|
7 Изоцитратдегидрогеназа |
|
icd |
||||
|
|
|
|
|
|
|
|
|
||||||
L-Аспартат |
Оксалоацетат |
Цитрат |
6 |
|
|
|
8 L-Глутаматдегидрогеназа (GDH) |
gdh |
||||||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
9 α-Кетоглутарат- |
|
|
aceE |
|||
|
|
|
|
|
|
|
|
|
|
|
||||
|
11 |
|
цис-Аконитат |
|
|
дегидрогеназа (KDH) |
|
|
||||||
|
Малат |
Глиоксилат |
|
|
|
|
10 Изоцитратлиаза (ICL) |
|
aceE |
|||||
|
|
|
|
10 |
|
|
|
|
11 Малатсинтетаза (MS) |
|
aceB |
|||
|
|
|
|
|
|
|
|
|
|
|||||
|
Фумарат |
|
|
Изоцитрат |
|
Штаммы-суперпродуценты: |
|
|
||||||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
7 |
|
|
|
|
|||||
|
|
|
|
|
|
|
1. Повышенная активность PEPC, GDH, ICL, MS |
|||||||
|
|
|
2-Оксоглутарат |
|
|
|||||||||
|
Сукцинат |
|
|
2. Сниженная активность или инактивация |
||||||||||
|
9 |
|
8 |
|
|
|||||||||
|
|
|
|
|
|
|
KDH |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
3. Нарушение регуляции активности PEPC |
||||||
|
|
|
|
L-Глутамат |
|
|
|
по механизму обратной связи посредством |
||||||
|
|
|
|
|
|
|
L-глутамата |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Усиление секреции |
|
Клеточная стенка |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
Клеточная мембрана |
|
|
|
|
|
|
|
|
|||
|
|
|
После добавления |
|
|
|
|
|
|
|
|
|||
|
Ацетил- |
|
|
биотина |
Малонил- |
Жирные |
|
|
|
|||||
|
|
|
|
|
|
|
|
|||||||
|
КоА |
|
Ограничение доступа |
|
|
KоА |
кислоты |
|
|
|
||||
Глюкоза |
|
ненасыщенных жирных кислот |
|
|
|
|
|
Фосфо- |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
Глицерин |
липиды |
|
|
|
L-Глутамат |
|
|
|
|
|
|
|
|
|
Инозит |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Изменение интенсивности транспорта через мембрану |
|
|
|
|
|
|
||||||||
Нарушение синтеза клеточной стенки под действием пенициллина |
|
|
|
|
|
|||||||||
L-Глутамат |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ферментация и первичная переработка |
|
|
|
|
|
|
|
|
|
|||||
Посевной материал, |
|
Ферментация |
|
Удаление |
|
Концентри- |
Обработка |
|
|
|||||
предферментация |
Биореактор до 500 м3, |
клеток |
|
рование |
Высушивание |
|
|
|||||||
Постепенное |
|
Пресс-фильтр |
Ультра- |
|
Выход |
|||||||||
увеличение объема |
источник углерода – |
или ультра- |
|
фильтрация |
распылением |
продукта: |
||||||||
меласса или |
|
|
|
или кристал- |
||||||||||
культуры в реакторе |
|
|
фильтрация |
|
|
|
~150 г/л |
|||||||
гидролизат крахмала, |
|
|
|
лизация |
||||||||||
|
|
|
|
|
|
|
через |
|||||||
|
|
источник азота – |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
40–60 ч |
||||
|
|
аммиак, наличие |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
биотина |
|
|
|
|
|
|
|
|
|
|
33 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
аминокислоты |
D,L-Метионин, L-лизин и L-треонин |
||||||
ВВЕДЕНИЕ. Основное |
применение D,L-метионин, |
cum в качестве источника углерода добавляют рас- |
|||||
|
|||||||
|
L-лизин и L-треонин находят в составе пищевых и |
творы сахаров. Уровень биотина в среде поддержива- |
|||||
|
кормовых добавок. Это незаменимые аминокислоты |
ют на постоянном уровне – около 30 мкг/л. После |
|||||
|
для человека и многих сельскохозяйственных живот- |
окончания синтеза и удаления клеток L-лизин выделя- |
|||||
и |
ных, т. е. они не образуются в организме и должны |
ют на ионообменной колонке или путем распылитель- |
|||||
поступать вместе с пищей. D,L-Метионин, L-лизин и |
ной сушки. Еще одна технология получения L-лизина |
||||||
кислоты |
|||||||
L-треонин содержатся в белках кукурузы, сои, овса, |
основана на использовании клеток Cryptococcus lau- |
||||||
|
|||||||
|
ячменя, ржи и риса, однако их содержание недоста- |
rentii. В настоящее время эта технология практиче- |
|||||
|
точно для полноценного питания. Поэтому вегетари- |
ски не реализуется, так как не может конкурировать |
|||||
Спирты, |
анцам рекомендуется дополнительно принимать пре- |
с технологией с использованием C. glutamicum. Тех- |
|||||
рожь, |
прибавка |
в |
весе достигается |
только |
coccus laurentii. Дешевым сырьем в данном случае |
||
|
параты L-метионина, L-лизина и L-треонина. При |
нология заключается в производстве L-лизина из |
|||||
|
откорме скота эти аминокислоты особенно важны: |
D,L-α-амино-ε-капролактама в биореакторе, в кото- |
|||||
|
когда основой питания животных являются рис и |
рый добавлены высушенные ацетоном клетки Crypto- |
|||||
|
в том случае, если в корм добавляют L-лизин и |
являются отходы производства нейлона, селектив- |
|||||
|
L-треонин, а когда животных кормят в основном куку- |
ный гидролиз которых приводит к образованию |
|||||
|
рузой, в их рацион необходимо добавлять D,L-метио- |
D,L-α-амино-ε-капролактама, который в свою оче- |
|||||
|
нин, L-лизин и L-треонин. В промышленности эти |
редь подвергается рацемизации ферментом D-ами- |
|||||
|
аминокислоты получают ферментацией или химиче- |
нокапролактамрацемазой, выделенной из штамма |
|||||
|
ским синтезом. |
|
|
|
Achromobacter obae. |
||
|
D,L-МЕТИОНИН. Химический синтез D,L-метионина, |
L-ТРЕОНИН. Мутантные штаммы Escherichia coli с из- |
|||||
|
L-лизина и L-треонина включает пять стадий. В каче- |
мененным путем регуляции биосинтеза являются ос- |
|||||
|
стве исходных веществ используют акролеин, метан- |
новными промышленными продуцентами L-треонина. |
|||||
|
тиол и синильную кислоту. Одним из промежуточных |
Максимальный выход продукта составляет 80 г/л че- |
|||||
|
продуктов синтеза является гидантоин – консервант, |
рез 30 ч роста. Уже клонированы гены оперона, от- |
|||||
|
использующийся при производстве шампуней и мою- |
вечающего за биосинтез треонина, и в настоящее |
|||||
|
щих средств. В процессе химического синтеза обра- |
время ведутся работы, направленные на получение |
|||||
|
зуется рацемат, в разделении которого нет необходи- |
штаммов с еще более высоким выходом продукта. |
|||||
|
мости, поскольку в организме высших животных |
После отделения клеток проводят ультрафильтрацию |
|||||
|
D-метионин превращается в L-метионин. |
|
культуральной жидкости, а затем L-треонин очищают |
||||
|
L-ЛИЗИН. В промышленом производстве L-лизина |
кристаллизацией. |
|||||
|
используются штаммы Corynebacterium glutamicum. |
ЭКОНОМИЧЕСКИЕ АСПЕКТЫ. В 2004 г. было произ- |
|||||
|
L-Лизин образуется из диаминопимелиновой кисло- |
ведено 600 000 т D,L-метионина, 700 000 т L-лизи- |
|||||
|
ты, которая в свою очередь получается из оксалоаце- |
на и 55 000 т L-треонина. Метионин получают преи- |
|||||
|
тата в результате многоступенчатой реакции конде- |
мущественно путем химического синтеза, а L-лизин и |
|||||
|
нсации аспарагиновой кислоты и пирувата. В диких |
L-треонин – ферментацией. Стоимость этих амино- |
|||||
|
штаммах в качестве побочных продуктов этой много- |
кислот 1000–2000 долл. США/т, а объем продаж до- |
|||||
|
стадийной реакции |
образуются предшественники |
стигает 500 млн долл. В последнее время наряду с |
||||
|
L-треонина и L-метионина, что снижает выход L-лизи- |
традиционным производством аминокислот для кор- |
|||||
|
на. В штаммах-суперпродуцентах этот побочный путь |
мовых добавок развивается новая технология – |
|||||
|
блокирован благодаря мутациям в генах соответству- |
выращивание трансгенных растений с измененным |
|||||
|
ющих ферментов (используют также ауксотрофные |
аминокислотным составом. Такие растения в перспе- |
|||||
|
мутантные штаммы, для метаболизма которых необ- |
ктиве могут использоваться непосредственно для от- |
|||||
|
ходимо присутствие специфических веществ, напри- |
корма скота. |
|||||
|
мер гомосерина). В настоящее время клонированы |
|
|||||
|
гены почти всех ферментов, участвующих в биосин- |
|
|||||
|
тезе L-лизина и его регуляции, поэтому методы гене- |
|
|||||
|
тической инженерии играют решающую роль в полу- |
|
|||||
|
чении |
штаммов, |
характеризующихся |
высоким |
|
||
|
уровнем синтеза L-лизина. В современном производ- |
|
|||||
|
стве используются штаммы, в которых выход проду- |
|
|||||
|
кта достигает 120 г/л через 60 ч роста. Как правило, |
|
|||||
34 |
применяют воздушно-проточную ферментацию в реа- |
|
|||||
кторах объемом до 500 м3. В среду роста C. glutami- |
|
||||||