Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
аминокислоты |
Этиловый спирт |
|
ВВЕДЕНИЕ. Этиловый спирт (этанол) используется как |
||
|
||
|
сырье в химическом производстве, как растворитель, а |
|
|
также как топливо. В 2004 г. мировое производство эта- |
|
|
нола составило 45 млрд л (34,6 млн т), из которых |
|
и |
лишь 2,3 млрд л были получены из этилена – продукта |
|
переработки нефти и природного газа. Более двух |
||
кислоты |
||
третей этанола, поступающего на рынок, получают из |
||
|
||
|
глюкозы биотехнологическими методами с помощью |
|
|
анаэробных дрожжей и бактерий. Традиционная техно- |
|
Спирты, |
логия производства этанола использовалась во многих |
|
нефть все чаще обращают вниимание на биотехнологи- |
||
|
странах, затем стало экономически выгоднее получать |
|
|
этанол из продуктов переработки нефти. В последние |
|
|
годы в связи со значительным ростом мировых цен на |
|
|
ческие подходы как резервную стратегию. Брожение мо- |
|
|
жет снова стать основным способом промышленного по- |
|
|
лучения этанола лишь при условии очень низких цен на |
|
|
биомассу или слишком высоких цен на энергоносители. |
|
|
С 1975 г. в Бразилии и США этанол используют в каче- |
|
|
стве топлива для двигателей внутренного сгорания. |
|
|
МИКРООРГАНИЗМЫ И БИОСИНТЕЗ. Для получения |
|
|
этанола путем спиртового брожения самое важное |
|
|
значение имеют пекарские дрожжи Saccharomyces |
|
|
cerevisiae. При гликолизе 1 моль D-глюкозы дает |
|
|
2 моль этанола. В бактериях Zymomonas mobilis, |
|
|
выделенных из сока агавы, этанол образуется в кето- |
|
|
дезоксифосфоглюконатном пути (пути Энтнера–Дудо- |
|
|
рова). Оба этих микроорганизма не имеют ферментов |
|
|
для расщепления полисахаридов, поэтому перед тем, |
|
|
как добавлять в питательную среду углеводы, их рас- |
|
|
щепляют до моносахаридов подходящими фермен- |
|
|
тами. Другой биотехнологический метод получения |
|
|
этанола основан на применении рекомбинантных |
|
|
штаммов-суперпродуцентов, которые в результате |
|
|
клонирования новых генов приобретают способность |
|
|
перерабатывать такие дешевые виды сырья, как крах- |
|
|
мал, целлюлоза или гемицеллюлоза. Особый интерес |
|
|
представляют термофильные анаэробные бактерии |
|
|
Thermoanaerobacter ethanolicus, которые могут рас- |
|
|
щеплять многие углеводы. Оптимальные условия для |
|
|
роста этого микроорганизма – температура 69 °С, |
|
|
рН среды 4,5–9,5. |
|
|
ПЕРЕРАБОТКА С ИСПОЛЬЗОВАНИЕМ ФЕРМЕНТАЦИИ. |
|
|
В основе промышленной технологии получения этанола |
|
|
лежит процесс брожения, который осуществляется в |
|
|
биореакторах объемом до 500 м3 в периодическом ре- |
|
|
жиме. В стандартных асептических условиях клетки |
|
|
дрожжей Saccharomyces cerevisiae менее подвержены |
|
|
заражению молочнокислыми бактериями, чем Zymomo- |
|
|
nas mobilis. В качестве бактериальной культуры исполь- |
|
|
зуют дрожжи, выращенные на обогащенной сахарами |
|
|
среде. Через 14–20 ч выход этанола достигает макси- |
|
20 |
мума (~90% теоретического значения). Процесс обра- |
|
зования этанола замедляется из-за подавления роста |
клеток дрожжей катаболитами. При концентрации глюкозы >0,1%, поэтому в промышленном процессе этанола применяют специальные методы контроля концентрации глюкозы в среде («fed-batch»). Другой причиной замедления роста дрожжей может быть высокая концентрация этанола, поэтому из культуральной среды следует непрерывно удалять этанол (через 72 ч его концентрация достигает ≥8% об.) путем азеотропной перегонки. При этом получают 95%-й этанол, который годится в качестве топлива. Абсолютный (100%) этанол получают путем специальных методов дистилляции, фильтрации через молекулярные или мембранные фильтры. При повторном использовании культуры время ферментации сокращается, например, по методу Мелле-Войно дрожжевые клетки концентрируют центрифугированием, полученной суспензией засевают другой биореактор. Промышленная технология может быть усовершенствована, если будет разработана непрерывная технология брожения. Теоретически такой процесс возможен, однако его практическое воплощение связано с преодолением больших технических проблем. Перспективно использование иммобилизованных дрожжевых и бактериальных клеток.
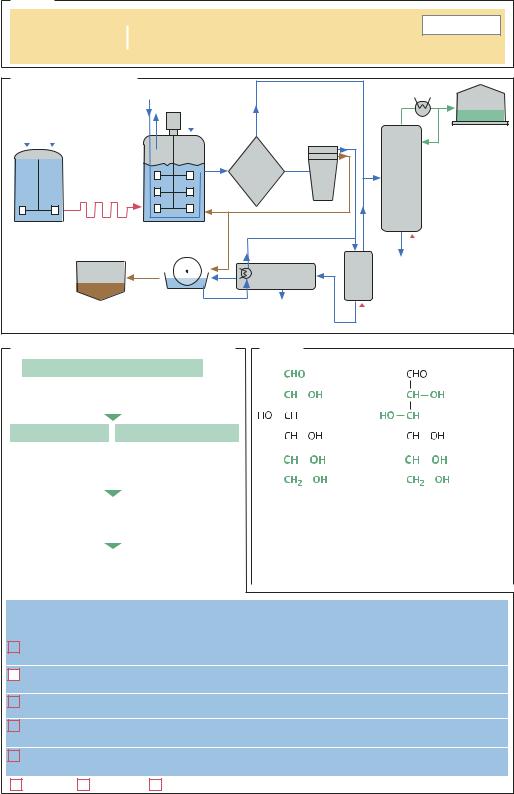
ЭКОНОМИЧЕСКИЕ АСПЕКТЫ. Основным сырьем для производства этанола являются меласса из сахарной свеклы (Бразилия) или кукурузный крахмал (США). В мире насчитывается более 700 крупных фирм, производящих этанол путем ферментации в периодическом режиме. С 1975 г. в Бразилии осуществляется масштабное производство этилового спирта из мелассы по простой технологии (периодическая ферментация, дистилляция). Эту технологию применяют более 100 крупных производителей этанола; в настоящее время производство этилового спирта в Бразилии достигло 12 млрд л в год. В США с 1975 г. на некоторых автозаправочных станциях продают автомобильное топливо – смесь этанола (9:1; так называемый «газохол»). В США производство этанола с использованием осахаренного кукурузного крахмала в качестве питательной среды для роста дрожжей осуществляется с применением более сложных технологий (ферментация в периодическом режиме, мембранная очистка) и достигло 10,6 млрд л в год (2003). В Бразилии и в США отходы промышленного получения этанола используются как кормовые добавки. В Японии разработана экономичная технология с несколькими вариантами непрерывного технологического процесса, где применяются иммобилизованные клетки дрожжей. В экспериментальной установке, работающей в непрерывном режиме, за 200 суток был получен 10%-й этанол, который очищали на мембранных фильтрах.
Этанол |
|
|
|
|
||
С2Н6О |
|
|
|
Н3С—СН2—ОН |
||
MR |
46,07 |
Ткип |
78,32 °С |
Промышленное получение: |
||
|
||||||
D. |
0,79367 (15 °С) |
Код CAS* |
64-17-5 |
в основном гидратацией этилена |
||
* Регистрационный номер Chemical Abstract Service. – Прим. ред. |
|
|||||
Получение из мелассы |
|
|
Охлаждение |
|||
|
|
Воздух* |
|
|
||
|
|
СО2 + воздух |
|
|
||
|
Питательные |
|
S. cerevisiae |
Резервуар |
||
|
вещества, |
|
|
Центрифуга |
||
Меласса вода |
|
|
для этанола |
|||
|
|
|
|
|
||
|
|
|
|
Сепара- |
Вакуумная |
|
|
|
|
|
дистилляционная |
||
|
|
|
|
тор** |
||
|
|
|
|
колонна |
||
|
Стерилизация |
|
|
|||
|
|
|
(ректификация |
|||
|
|
|
|
|
в вакууме) |
|
|
|
|
|
Возврат клеток |
|
|
|
|
|
|
в производственный цикл |
|
|
|
|
|
|
|
Пар |
|
|
Отходы: |
|
|
|
Вода |
|
|
кормовые |
|
|
Испаритель |
Стриппинг- |
|
|
добавки |
|
|
|
||
|
|
|
|
|
колонна |
|
* Только во время роста |
|
|
Вода |
Пар |
||
|
|
|
||||
** Экстрактор/установка для дистилляции/мембраны |
|
|
||||
Ферментация и дальнейшая переработка |
Этанол |
|
||||
Питательные вещества |
|
|
|
|
|
|
|
|
|
|
1 |
|
2 |
||||||
Сахарный тростник, меласса |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
из сахарной свеклы или осахаренный |
|
|
|
|
|
|
|
|
|
кукурузный крахмал, соли |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Клеточный реактор |
|
Биореактор |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
Иммобилизованные |
|
Объем до 500 м3, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
клетки, ферментация |
|
ферментация в непрерыв- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
в непрерывном |
|
|
ном или периодическом |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
режиме |
|
|
режиме |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
Происхождение атомов углерода в молекуле этанола |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
Удаление этанола |
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
при сбраживании глюкозы |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
Дистилляция или первапорация |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
Saccharomyces cerevisiae |
|
|
|
|
|
Гликолиз |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Переработка отходов |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
2 |
|
Zymomonas mobilis |
|
путь Энтнера–Дудорова |
|
|
|
||||||||||||||||||
|
|
|
|
|
Кормовые добавки для скота |
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Организм |
Система |
Содержание |
Скорость |
Содержание Концентрация Максимальный |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
глюкозы, |
истощения, |
|
|
|
|
клеток, |
этанола, |
|
|
|
выход |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
г/л |
|
|
ч–1 |
|
|
|
|
|
|
г/л |
г/л |
|
|
|
продукта, г/л |
||||||
|
|
|
|
Saccharomyces Без возврата |
100 |
0,17 |
|
12 |
41 |
|
7,0 |
|
|
|
||||||||||||||||||||
1 |
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
cerevisiae |
клеток в цикл |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
1 |
|
S. cerevisiae |
С возвратом |
100 |
0,08 |
|
50 |
43 |
|
29 |
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
клеток в цикл |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
S. cerevisiae |
С возвратом |
150 |
0,53 |
|
48 |
60,5 |
|
32 |
|
|
|
||||||||||||||||||||
|
2 |
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
клеток в цикл |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
1 |
|
S. cerevisiae |
С возвратом клеток |
334 |
0,23 |
|
124 |
110–160 |
82 |
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
в цикл, вакуум (6,7 кПа) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
Zymomonas |
С возвратом |
100 |
2,7 |
|
|
38 |
44,5 |
|
120 |
|
|
|
||||||||||||||||||
3 |
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
mobilis |
клеток в цикл |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
21 |
||||||||||||
|
|
|
|
ATCC 4126; |
|
NRLL Y-132; |
|
ATCC 10988 – штаммы микроорганизмов |
|
|
|
|||||||||||||||||||||||
1 |
|
|
2 |
3 |
|
|
|
|||||||||||||||||||||||||||
аминокислоты |
1-Бутанол, ацетон |
|
ВВЕДЕНИЕ. 1-Бутанол имеет очень важное значение |
||
|
||
|
как растворитель лаков, используемых при покраске |
|
|
автомобилей, а также как сырье в промышленном син- |
|
|
тезе (в реакциях этерификации). Объем мирового |
|
и |
производства бутанола составляет 1,2 млн т в год. Ра- |
|
ньше бутанол служил сырьем при получении синтети- |
||
кислоты |
||
ческого каучука из бутадиена. Ацетон также очень |
||
|
||
|
важный растворитель. В мире за год производится |
|
|
около 3 млн т ацетона. В современном производстве |
|
Спирты, |
основным источником сырья для синтеза этих соеди- |
|
нений служат продукты нефтехимической промышлен- |
||
ности. До 1950 г. ацетон и 1-бутанол получали в ос- |
||
новном при сбраживании мелассы или крахмала с |
||
помощью анаэробных бактерий рода Clostridium. |
||
|
В связи с новыми возможностями, которые открыва- |
|
|
ются в эпоху развития биотехнологии, ферментатив- |
|
|
ных методов получения ацетона и 1-бутанола вновь |
|
|
приобрели значение после их оптимизации и рассмат- |
|
|
риваются в качестве «резервных» технологий. |
|
|
МИКРООРГАНИЗМЫ И БИОСИНТЕЗ. Среди немного- |
|
|
численных бактерий-продуцентов ацетона и 1-бута- |
|
|
нола наиболее важное значение в производственных |
|
|
технологиях имеют анаэробные бактерии рода Clo- |
|
|
stridium. В ацетоно-бутиловом брожении можно вы- |
|
|
делить две фазы: первая – бактерии активно размно- |
|
|
жаются, и в среде накапливаются ацетат и бутират, |
|
|
что приводит к понижению рН до 5,0. При таком низ- |
|
|
ком рН размножение бактерий практически заканчи- |
|
|
вается, и брожение переходит во вторую фазу – на- |
|
|
копление 1-бутанола и ацетона, образующихся из |
|
|
имеющихся в среде углеводов и накопленных в пер- |
|
|
вой фазе кислот. Состав конечного продукта зависит |
|
|
от используемого бактериального штамма. Наиболее |
|
|
хорошо изучена физиология Clostridium acetobutyli- |
|
|
сum, который обладает самой высокой продуктив- |
|
|
ностью, а также достаточно устойчив к токсичному |
|
|
действию 1-бутанола. При сбраживании 100 г глюко- |
|
|
зы с помощью Clostridium acetobutyliсum образуется |
|
|
38 г смеси бутанола и ацетона в соотношении 3:1. |
|
|
Многие представители рода Clostridium содержат |
|
|
амилазы, амилоглюкозидазы и другие внеклеточные |
|
|
деполимеразы, поэтому для их культивирования |
|
|
можно использовать такое дешевое питательное ве- |
|
|
щество, как крахмал. Перспективным признано при- |
|
|
менение лактозы (в виде молочной сыворотки). К на- |
|
|
стоящему времени изучены механизмы действия и |
|
|
регуляции практически всех ферментов, участвую- |
|
|
щих в биосинтезе ацетона и 1-бутанола, гены боль- |
|
|
шинства этих ферментов уже клонированы. При гли- |
|
|
колизе из глюкозы образуется пируват, который под |
|
|
действием фермента пируват:ферредоксин-оксидо- |
|
|
редуктазы декарбоксилируется с образованием аце- |
|
22 |
тил-КоА. Продуцируемые в процессе гликолиза вос- |
|
становительные эквиваленты (прежде всего NADH) |
обеспечивают дальнейшие превращения ацетил-КоА в С2-, С3- или С4-соединения. В реакции, катализируемой гидрогеназой, молекулярный водород служит донором электронов. Знание механизмов регуляции активности этого фермента может позволить осуществлять контроль за составом конечного продукта (metabolic engineering), поэтому в настоящее время ведутся активные исследования, посвященные изучению гидрогеназы. Геном C. acetobutyliсum полностью прочитан, и с этим микроорганизмом возможны генетические манипуляции. Так, разработаны челночные векторы для C. acetobutyliсum и Escherichia coli и Bacillus subtilis, а также системы с использованием транспозонов и специфических фагов. Методами генетической инженерии на основе диких и мутантных штаммов удалось значительно повысить выход ацетона и 1-бутанола.
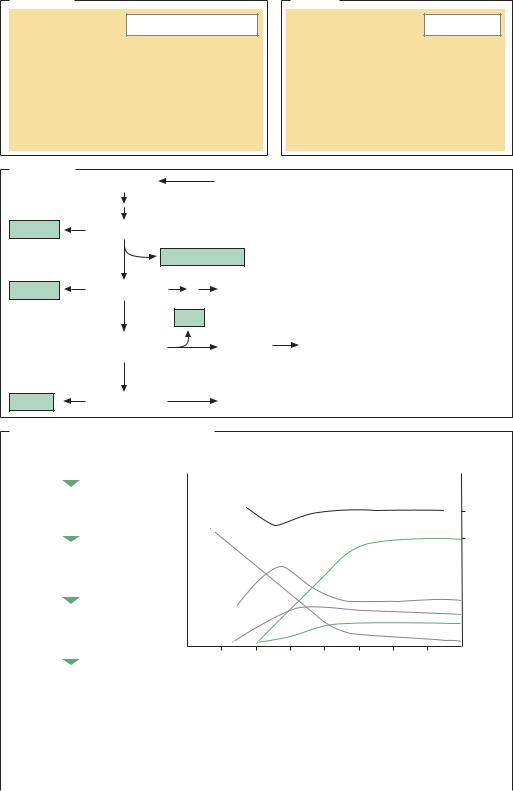
ФЕРМЕНТАТИВНЫЙ ПРОЦЕСС И ПЕРВИЧНАЯ ОБРАБОТКА. В течение более 40 лет ферментативное получение ацетона и 1-бутанола с помощью C. acetobutyliсum в промышленных масштабах осуществляли в ферментерах с рабочим объемом более 100 м3. При этом около 60% производственных затрат приходилось на закупку сырья, а примерно 12% – на энергетические расходы при дистилляции. В современном производстве используются двустадийные технологии с возвратом клеток в производственный цикл, непрерывная ферментация, технологии с иммобилизацией клеток, а также усовершенствованные технологии выделения продуктов ферментации (первапорация, обратный осмос). Традиционные технологии, которые применялись в Северной Америке и ЮАР, с периодическим режимом культивирования клеток на кукурузном крахмале или мелассе в качестве сырья менее выгоден по сравнению с получением ацетона и 1-бутанола из продуктов нефтехимии. Экономическая целесообразность использования той или иной технологии определяется расходом сырья (кг продукта/кг сахара) и продуктивность (кг продукта/(час литр культуры)). Технология совершенствуется по двум направлениям. Во-первых, генно-инженерными методами удалось получить штаммы, устойчивые к токсичному действию ацетона и 1-бутанола, а изучение биохимических и физиологических особенностей жизнедеятельности микроорганизмов привело к созданию новых штаммов-суперпродуцентов. Во-вторых, можно повысить эффективность производства путем совершенствования самого технологического процесса, в том числе условий ферментации и выделения продуктов. На фоне постоянно растущих цен на нефть метод ферментативного получения ацетона и 1-бутанола, вероятно, вновь приобретет важное значение.
1-Бутанол |
|
|
|
Ацетон |
|
|
|
С4Н10О |
Н3С—СН2—СН2—СН2—ОН |
|
С3Н6О |
|
Н3С—СО—СН3 |
||
MR |
74,12 |
|
|
|
MR |
58,08 |
|
d |
0,81 |
|
|
|
d |
0,7908 |
|
Ткип |
117–118 °С |
|
|
|
Ткип |
56 °С |
|
Код CAS |
71-36-3 |
|
|
|
Код CAS |
67-64-1 |
|
Химический синтез: |
|
|
|
Каталитическое дегидрирование 2-пропанола |
|||
гидроформилирование пропилена |
|
|
|
Прямое окисление пропилена |
|||
с последующим гидрированием |
|
|
|
Расщепление кумолгидропероксида |
|||
Биосинтез |
|
|
|
|
|
|
|
|
Глюкоза |
|
Крахмал, сыворотка и т. д. |
|
|
||
|
|
|
|
|
|
1 |
Пируват: ферредоксин- |
|
|
|
|
|
|
|
оксидоредуктаза |
2 лактат |
2 пируват |
|
|
|
|
2 |
Гидрогеназа |
|
|
|
|
3 |
Тиолаза |
||
|
2 |
|
|
|
|
||
|
|
|
|
|
4 |
КоА-трансфераза/ |
|
|
1 |
2 Н2 + 2 СО2 |
|
|
|||
|
|
|
|
ацетацетат-декарбоксилаза |
|||
|
|
|
|
|
|
5 |
Альдегид/ |
2 ацетат |
2-ацетил-КоА |
|
2 этанол |
|
|
|
алкогольдегидрогеназа |
|
|
|
6 |
Две гидрогеназы, |
|||
|
|
|
|
|
|
||
|
3 |
СО2 |
|
|
|
7 |
кротоназа |
|
|
|
|
|
Бутиральдегиддегидрогеназа |
||
|
ацетоацетил- |
|
|
|
|
|
и бутанолдегидрогеназа |
|
|
ацетон |
|
2-пропанол |
|
||
|
КоА |
4 |
5 |
|
|||
|
|
|
|
Гены всех указанных |
|||
|
6 |
|
|
|
|
|
|
|
|
|
|
|
|
ферментов клонированы |
|
|
|
|
|
|
|
|
|
бутират |
бутирил-КоА |
7 |
1-бутанол |
|
|
|
|
|
|
|
|
|
|||
Ферментация и первичная обработка |
|
|
|
|
|
||
|
Споры |
|
Сбраживание глюкозы под действием |
|
|
|
|
|
|
|
|
|
|||||||
|
|
Clostridium acetobutylicum |
|
|
|
|
|
|
|
|
|
|
|
||||||
|
Суспензия в образце почвы |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
% |
|
|
Фаза |
|
|
Фаза образования |
|
|
|
|
|
|
|
|
|||
|
|
|
|
образования |
|
растворителей |
|
|
|
|
|
|
|
|
|
||||
|
Жидкая культура |
|
глюкозыКонцентрацияв среде, |
100 |
|
кислот |
|
|
|
|
рН |
|
|
5,0 |
|
|
|||
|
|
|
|
|
|
|
рН |
|
|
||||||||||
|
Анаэробные условия, |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
24 ч при 37 °С |
|
|
|
|
|
|
|
|
|
Бутанол |
|
|
|
культурыпродукта/млмг |
|
|||
|
|
|
|
80 |
|
|
|
|
|
|
|
|
|
|
4,0 |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
Биореактор |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
объемом 15 м3 |
|
|
60 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
Пропускание СО2, |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
18 ч при 37 °С |
|
|
40 |
|
|
|
|
|
|
|
|
Бутират |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Ацетат |
|
|
|
|||
|
Биореактор |
|
|
20 |
|
|
|
|
|
Ацетон |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
объемом 700 м3 |
|
|
|
|
|
|
|
|
Глюкоза |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
6% меласса, |
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
50–60 ч при 37 °С |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
0 |
8 |
16 |
24 |
32 |
40 |
48 |
Время, ч |
|
|
|
|||||
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Непрерывная |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Микроорганизм |
|
|
|
Выход продукта, % |
|
|
|
||||||||||
|
дистилляция |
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Затем фракционная |
|
|
|
|
|
|
|
|
1-Бутанол |
Ацетон |
2-Пропанол |
Этанол |
|
|
||||
|
перегонка |
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
Clostridium acetobutylicum |
|
30,2 |
|
14,0 |
– |
5,0 |
|
|
|||||||||
|
|
|
|
|
|
|
|||||||||||||
|
|
|
C. beijerinckii |
|
|
|
67,9 |
|
6,0 |
– |
– |
|
|
||||||
|
Около 38 кг |
|
C. puniceum |
|
|
|
75,6 |
|
16,8 |
– |
– |
|
|
||||||
|
смеси 1-бутанол : ацетон |
|
C. tetanomorphum |
|
|
47,1 |
|
– |
– |
42,7 |
|
|
|||||||
|
(3 : 1) из 100 кг глюкозы |
|
|
|
|
|
|
||||||||||||
|
|
C. butyricum |
|
|
|
17,0 |
|
– |
7,0 |
|
|
|
– |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
23 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
аминокислоты |
Уксусная кислота |
|
ВВЕДЕНИЕ. Уксус в качестве вкусовой добавки или |
||
|
||
|
консерванта использовался в Европе еще в античные |
|
|
времена. Он также находит широкое применение и в |
|
|
классической кухне народов Азии. По традиционной |
|
и |
технологии уксус получали из вина. Один из знаме- |
|
нитых примеров – бальзамический уксус, который |
||
кислоты |
||
является своеобразной «кулинарной достопримеча- |
||
|
||
|
тельностью» города Модена (Италия). Во Франции в |
|
|
XVIII в., когда еще трудно было говорить о развитии |
|
Спирты, |
промышленности, существовал так называемый |
|
«стружечный» способ получения уксуса – разведен- |
||
ное вино наливали в бочки с древесной стружкой, |
||
вымоченной в уксусе. В 1856 г. Луи Пастер обнару- |
||
жил микроорганизмы, осуществляющие уксуснокис- |
||
|
лое брожение – уксуснокислые бактерии. К 1868 г., |
|
|
изучая различные среды роста, он получил чистую |
|
|
культуру этих бактерий и таким образом заложил ос- |
|
|
новы технологического метода получения винного ук- |
|
|
суса (содержание уксусной кислоты около 6%). Сто- |
|
|
ловый уксус – 5%-й раствор уксусной кислоты, как |
|
|
правило, получают ферментацией ректификата (эта- |
|
|
нола). Мировое производство уксусной кислоты со- |
|
|
ставляет несколько млрд литров в год. В США в |
|
|
больших количествах используется ацетат кальция- |
|
|
магния (температура плавления –7,7 °С), получен- |
|
|
ный биотехнологическим методом, как реагент для |
|
|
борьбы с обледенением на автотрассах (Cryotech |
|
|
CMAТМ). Химический реактив «ледяная уксусная кис- |
|
|
лота» (99,7%, рКа 5,6) производят из этилена или |
|
|
метанола. |
|
|
МИКРООРГАНИЗМЫ В БИОСИНТЕЗЕ. Способностью |
|
|
осуществлять неполное окисление этанола с образо- |
|
|
ванием уксусной кислоты обладают лишь немногие |
|
|
микроорганизмы, в частности, некоторые штаммы |
|
|
Gluconobacter и Acetobacter. Принадлежность бакте- |
|
|
рий к тому или иному штамму определить очень |
|
|
сложно из-за быстро меняющегося фенотипа, поэто- |
|
|
му с этой целью используют анализ последователь- |
|
|
ностей 16S-рРНК или плазмид. Окисление этанола |
|
|
происходит в реакциях, катализируемых мембранос- |
|
|
вязанными ферментами алкогольдегидрогеназой |
|
|
и альдегиддегидрогеназой. В клетках Acetobacter |
|
|
альдегиддегидрогеназа несет в качестве простетиче- |
|
|
ской группы пирроллхинолинхинон (ПХХ), а альдегид- |
|
|
дегидрогеназа наряду с пирроллхинолинхиноном |
|
|
содержит еще гем. Перенос электронов на терми- |
|
|
нальную оксидазу происходит через образование |
|
|
убихинона. Уксуснокислые бактерии осуществляют |
|
|
гликолиз, образующиеся молекулы пирувата посту- |
|
|
пают в цикл лимонной кислоты. Уксуснокислые бак- |
|
|
терии чрезвычайно требовательны к высокой концен- |
|
|
трации кислорода в среде роста: прерывание аэрации |
|
24 |
всего на несколько минут приводит к значительному |
|
снижению эффективности окисления этанола. В от- |
сутствие этанола бактерии рода Acetobacter окисляют уксусную кислоту до углекислого газа.
ФЕРМЕНТАЦИЯ И ПЕРЕРАБОТКА. Для получения стартовой культуры Acetobacter sp. в пилотном ферментере клетки культивируют на сусле (вино или спирт, 1%-ная уксусная кислота, питательные вещества). После начала образования кислоты устанавливают повторяющийся цикл: когда концентрация спирта снижается до 0,2% (воздух в ферментере встроен датчик), более половины культуральной жидкости удаляют, и добавляют новое сусло. Для интенсивной аэрации без вспенивания жидкости (воздух в ферментер подают со скоростью, равной 1/10 объема ферментера в минуту) служат специальные мешалки, сконструированные Фрингсом. Тепло, выделяемое бактериями в результате метаболизма, отводится системой охлаждения. Средняя эффективность процесса в ферментере объемом 100 м3 составляет 1,6 г/л. Раствор уксусной кислоты из ферментера пропускают через мембранные фильтры, пастеризуют и разводят до концентрации столового уксуса. При использовании специальных штаммов и регулировании условий ферментации образуется 17,5%-й уксус, а более концентрированный уксус для производства консервов получают двухступенчатой ферментацией. Около 70% всего производимого в мире столового уксуса получают в ферментерах, изобретенных Фрингсом (способ Фрингса). Их количество в мире превышает 700. Альтернативой биореактору Фрингса является эрлифтный реактор с иммобилизованными уксуснокислыми бактериями: этот метод позволяет получать высокий выход продукта (свыше 100 г/л), однако пока редко используется в промышленных масштабах.