Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
Уксусная кислота |
|
|
|
|
|
С2Н4О2 |
|
|
|
Н3С—СОOН |
|
MR |
60,05 |
|
Химический синтез: |
||
|
|
|
|||
Ткип |
117,9 °С |
|
|
|
|
pKa |
4,76 (25 °С) |
|
окисление этилена |
|
|
Код CAS |
67-19-7 |
|
или реакция СО с метанолом |
|
|
Биосинтез с участием Acetobacter sp. |
|
|
|||
Алкогольдегидрогеназа |
|
Альдегиддегидрогеназа |
|
||
С2Н5ОН |
Н3С—СНО |
|
Н3С—СОOН |
|
|
|
(ацетальдегид) |
(уксусная кислота) |
|
|
|
|
Н2О + СО2 |
|
|
|
|
|
«полное окисление» |
|
|
||
Мембраносвязанные ПХХ-зависимые дегидрогеназы передают на убихинон |
|
||||
высвобождаемые при окислении электроны, которые затем поступают |
|
||||
на терминальную оксидазу – также мембраносвязанный фермент. |
Пирроллхинолинхинон (ПХХ) |
||||
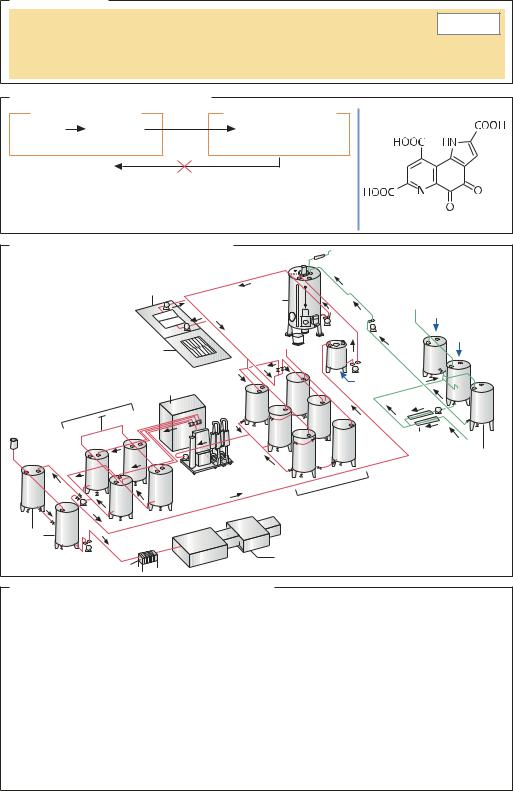
Ферментация и дальнейшая переработка |
|
|
|||
|
Система охлаждения |
|
|
||
|
|
|
Аппарат Фрингса |
Вино |
|
|
|
|
|
|
|
|
|
|
|
|
94% этанол |
Аварийный блок питания |
|
|
|||
Резервуары |
Мембранный фильтр |
Питательные |
|
||
для разбавления |
вещества |
|
|||
уксусной кислоты |
|
|
|
|
|
|
|
|
|
Смеши- |
|
|
|
|
|
вание |
Сусло |
|
|
|
|
с водой |
|
|
|
|
|
|
|
|
|
|
|
Резервуары |
|
|
|
|
|
для хранения |
|
|
|
|
|
уксусной кислоты |
|
Розлив |
|
|
|
|
|
уксуса |
|
|
Розлив пастеризованного уксуса |
|
|
|
Пастеризация |
|
|
||
|
|
|
|
|
|
Другие технологии получения уксусной кислоты
|
Максимальное |
Продуктивность |
Особенности |
|
|
содержание |
процесса, |
|
|
|
уксусной кислоты, % |
л/м3 в сут. |
|
|
Стандартный метод |
15 |
35–50 |
Простой технологический процесс |
|
(с периодическим режимом) |
|
|
|
|
Одностадийный процесс |
18,5 |
30–50 |
Высокая концентрация конечного |
|
с высоким выходом |
|
|
продукта, низкие затраты на хранение |
|
уксусной кислоты |
|
|
и транспортировку |
|
Двухстадийный процесс |
Более 20 |
30–50 |
Высокая концентрация конечного |
|
с высоким выходом |
|
|
продукта, низкие затраты на хранение |
|
уксусной кислоты |
|
|
и транспортировку |
|
Непрерывный |
Более 10 |
До 60 |
Высокая концентрация конечного |
|
ферментативный |
|
|
продукта, более низкие затраты |
|
процесс |
|
|
на хранение и транспортировку |
|
Иммобилизованные |
Менее 9 |
– |
Эрлифтные реакторы; |
|
уксуснокислые бактерии |
|
|
работают на протяжении 460 сут. |
|
(стадия испытаний) |
|
|
|
25 |
|
|
|
|
|
Спирты, кислоты и аминокислоты
Лимонная кислота
ВВЕДЕНИЕ. В 1822 г. Карл Вильгельм Шееле впер- |
ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ИЗ САХАРОВ. Для |
вые выделил D-лимонную кислоту из лимонного со- |
промышленного производства лимонной кислоты ис- |
ка и изучил ее свойства. Значительные количества |
пользуют твердофазную ферментацию сахаров под |
этой кислоты содержатся во многих фруктовых со- |
действием A. niger. В открытые металлические ре- |
ках. Хансу Кребсу принадлежит одно из самых заме- |
зервуары, устойчивые к кислой среде, помещают |
чательных открытий в биохимии: в 1937 г. он пока- |
раствор сахаров и споры гриба. Для дополнительной |
зал, что лимонная кислота является ключевым |
аэрации и отведения тепла в суспензию пропускают |
соединением аэробного обмена веществ (цикл три- |
воздух с интенсивностью до 10 объемов ферментера |
карбоновых кислот, цикл Кребса). За сутки в орга- |
в минуту. Через пять суток образуется хорошо разви- |
низме взрослого человека образуется около 1,5 кг |
тый мицелий, в котором активируется синтез лимон- |
лимонной кислоты, которая затем подвергается |
ной кислоты (продолжительность всего процесса |
дальнейшим превращениям. Лимонная кислота – |
8 сут.). После удаления мицелия проводят экстрак- |
сильная кислота с трехступенчатой диссоциацией: |
цию горячей водой и осаждение цитрата. Выход про- |
рКа при 25 °С составляют 3,13, 4,78 и 6,43 соот- |
дукта достигает 50 г/кг сахара. В современной |
ветственно. В 1%-м растворе лимонной кислоты |
промышленности цитрат получают в башенных био- |
рН 2,2. Наличие трех карбоксильных и одной гидро- |
реакторах или реакторах с механическим перемеши- |
ксильной группы определяет способность лимонной |
ванием в стерильных условиях. Объем таких реакто- |
кислоты к образованию комплексов с двух- и трехва- |
ров от 100 до 500 м3. рН продукта на выходе ~2,0, |
лентными катионами. Промышленное получение ли- |
поэтому ферментеры должны быть выполнены из ус- |
монной кислоты основано на ферментативном про- |
тойчивой к агрессивной среде высококачественной |
цессе. Мировое производство лимонной кислоты |
стали. В качестве экономически выгодного сырья ис- |
составляет 1 200 000 т в год (2005), объем рын- |
пользуют гидролизат крахмала или дешевые источ- |
ка – около 1 200 млрд долларов США. Лимонная |
ники сахарозы. Эффективность образования цитрата |
кислота используется как подкислитель и консерви- |
зависит от содержания ионов марганца в среде: |
рующий агент в пищевой промышленности, компле- |
в среде с низким содержанием марганца (менее |
ксообразователь в металлургии, средство для смяг- |
2 мкг/л) синтезируется большое количество продук- |
чения воды при производстве стиральных порошков |
та. Наращивание клеточной массы завершается че- |
и для неотложной помощи при тяжелых отравлениях |
рез 48 ч роста при рН 5. Последующее искусствен- |
солями металлов. |
ное закисление среды до рН 2,5, добавление сахаров |
МИКРООРГАНИЗМЫ И БИОСИНТЕЗ. Некоторые плес- |
при непрерывной ферментации и интенсификация |
невые грибы, в частности Aspergillus niger, в услови- |
аэрации способствуют образованию лимонной кисло- |
ях избытка глюкозы и интенсивной аэрации во время |
ты. Продукт выделяется клетками во внеклеточную |
экспоненциальной фазы роста и после ее окончания |
среду. В расчете на потребленную глюкозу выход ли- |
выделяют в среду значительное количество лимон- |
монной кислоты более 80%. По завершении фер- |
ной кислоты. Несмотря на то что многие промежу- |
ментации мицелий отфильтровывают, в раствор цит- |
точные продукты цикла Кребса оказывают регулятор- |
рата добавляют Ca(OH)2, далее цитрат кальция |
ное влияние на другие процессы обмена веществ, |
переводят в кислоту серной кислотой. Сырой продукт |
возможно создание штаммов A. niger – суперпроду- |
обрабатывают активированным углем и пропускают |
центов лимонной кислоты. Во-первых, запас оксало- |
через ионообменную колонку. В растворе кристалли- |
ацетата постоянно растет за счет активности находя- |
зуется очень чистая лимонная кислота. Расход гипса |
щиейся в цитоплазме пируваткарбоксилазы, которая |
более 1 т/т лимонной кислоты. В настоящее время |
катализирует присоединение молекулы СО2 к пиру- |
большое распространение получает другой более |
вату с образованием оксалоацетата (анаплеротиче- |
экономичный способ очистки лимонной кислоты: по- |
ская, т. е. возмещающая реакция). Во-вторых, ли- |
сле реакции цитрата с трилауриламином продукт эк- |
монная кислота синтезируется в митохондриях, |
страгируют с помощью алканов и 1-октанола. Раство- |
секретируется в цитоплазму, а затем выводится из |
рители и трилауриламин можно вновь использовать |
клетки. Причина существования такого направленно- |
после соответствующей обработки. В последние годы |
го транспорта в том, что цитоплазматическая малат- |
был разработан метод получения D-лимонной кисло- |
дегидрогеназа катализирует превращение оксалоаце- |
ты из фракций нефти с помощью особого штамма |
тата в яблочную кислоту, молекулы которой |
дрожжей. Проект был доведен до этапа создания пи- |
проникают в митохондрии, заменяя молекулы лимон- |
лотной установки, однако в связи с резким повыше- |
ной кислоты (принцип антипорта). |
нием цен на нефть пока отложен. |
26
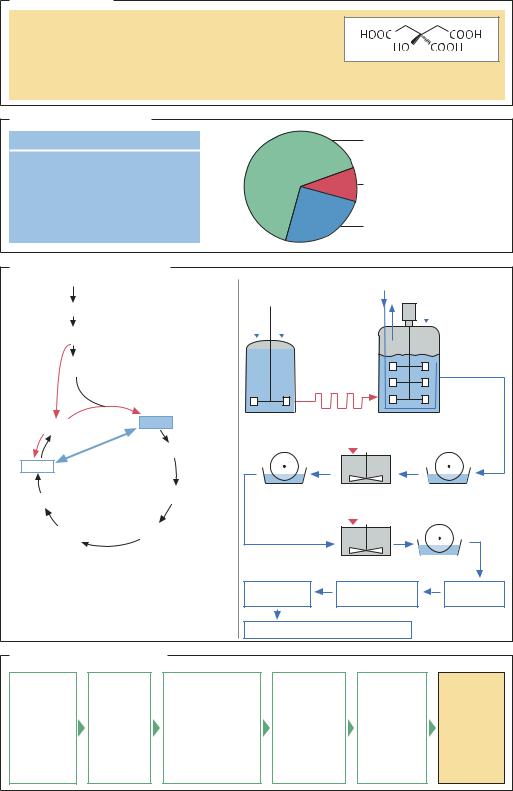
Лимонная кислота |
|
|
|
|
|
|
|
С6Н8О7 |
|
|
Код СAS 77-92-9 |
|
|
|
|
MR |
|
192,12 |
|
|
|
|
|
Растворимость |
|
600 г/л воды (20 °С) |
|
|
|
|
|
Кислотные свойства |
рKa1 = 3,128 (25 °С); в 1%-м водном растворе лимонной кислоты рН 2,2 |
|
|||||
Комплексообразование (lgK): Fe3+ 12,5, Ca2+ 4,68, Cu2+ 3,98 (при 20 °С) |
|
|
|
||||
Источники и применение |
|
|
|
|
|
||
Источники |
|
г/кг |
|
|
Пищевая и косметическая |
||
|
|
|
|
|
промышленность |
|
|
Лимоны |
|
40–80 |
|
|
65% |
|
|
Грейпфруты |
|
12–21 |
|
|
Медицина 10% |
|
|
Малина |
|
10–13 |
|
|
|
||
|
|
|
|
|
|
||
Черная смородина |
15-30 |
|
|
|
|
|
|
Клубника |
|
6–8 |
|
|
|
|
|
Томаты |
|
2,5 |
|
|
Техника 25% |
|
|
Биосинтез в Aspergillus niger |
|
|
|
|
|
||
Глюкоза |
|
Промышленное |
Воздух |
|
|
||
|
|
|
получение цитрата: |
СО2 + воздух |
|
||
Фосфоенолпируват |
|
|
|
||||
Ме- |
Питательные |
|
Aspergillus niger |
||||
|
|
|
|
||||
|
|
|
|
|
|
||
Пируват |
|
|
ласса |
вещества, вода |
|
|
|
|
|
|
|
|
|
|
|
Ацетил-КоА |
|
|
|
|
|
||
|
|
|
|
Стерилизация |
|
|
|
1 |
|
3 |
|
|
|
|
|
Оксалоацетат |
|
Цитрат |
|
|
Ферментер |
Клеточная |
|
|
|
|
|
|
|||
2 |
4 |
|
Известь |
Са(ОН)2 |
|
масса |
|
|
|
|
|||||
|
цис-Аконитат |
|
|
||||
|
|
|
|
|
|
|
|
Малат |
|
|
|
|
|
|
|
Фумарат |
|
Изоцитрат |
фильтрация |
осаждение |
Фильтры |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
H2SO4 |
CaSO4 |
|
Сукцинат |
|
2-Оксоглутарат |
|
|
|
|
|
|
|
|
|
|
|
|
|
Анаплеротические реакции |
|
|
осаждение |
фильтрация |
|||
цикла трикабоновых кислот: |
|
|
|||||
|
|
|
|
|
|||
1 Пируваткарбоксилаза (в цитоплазме) |
Центрифуги- |
Кристаллизация |
|
Концентри- |
|||
2 Малатдегидрогеназа (в цитоплазме) |
|
||||||
рование |
|
рование |
|||||
3 Цитратсинтаза (в митохондриях) |
|
|
|||||
|
|
|
|
|
|||
4 Цитрат/малат-антипортер |
|
|
|
|
|
||
(мембрана митохондрий) |
Кристаллическая лимонная кислота |
|
|
||||
Ферментация и переработка |
|
|
|
|
|
||
Инокулят, |
|
Предфер- |
|
Основная |
|
Удаление |
|
|
Очистка |
|
питательная |
|
ментация |
|
ферментация |
|
мицелия |
|
|
|
|
|
|
Осаждение: |
Выход |
|||||||
среда |
|
|
|
|
|
|
|
|||
|
Биореактор |
Биореактор объемом |
|
Вращающиеся |
1. |
Са(ОН)2 |
||||
|
|
|
лимонной |
|||||||
Крахмал, |
объемом |
400 м3 из кислото- |
|
фильтры |
2. |
Н2SO4 |
кислоты – |
|||
меласса, |
40 м3 |
устойчивого мате- |
|
|
3. |
пере- |
более 200 г/л |
|||
источник |
|
|
риала, 8 сут. при |
|
|
|
|
кристал- |
||
|
|
|
|
|
|
через 150 ч |
||||
азота, соли |
|
|
32 °С; после завер- |
|
|
|
|
лизация |
||
|
|
|
|
|
|
ферментации |
||||
|
|
|
|
шения фазы роста |
|
|
|
|
|
|
|
|
|
|
закисление среды |
|
|
|
|
|
|
|
|
|
|
от pH 5,0 до 2,0 |
|
|
|
|
|
|
27
аминокислоты |
Молочная и глюконовая кислоты |
|
ВВЕДЕНИЕ. Объем мирового производства молочной |
||
|
||
|
кислоты за 2001 г. составил 860 000 т, из которых |
|
|
30 000 т получены путем ферментации. Благодаря |
|
|
умеренно кислому вкусу и консервирующим свойст- |
|
и |
вам молочная кислота находит широкое применение |
|
в пищевой промышленности (до 85% всего произве- |
||
кислоты |
||
денного объема). Молочная кислота технической чи- |
||
|
||
|
стоты используется в кожевенном и текстильном |
|
|
производствах, а также служит сырьем для синтеза |
|
Спирты, |
полимеров, поддающихся биологической деградации, |
|
WorksТМ), которое разлагается под действием микро- |
||
|
например полилактидов. Ежегодно в мире произво- |
|
|
дится более 100 000 т L-молочной кислоты, которая |
|
|
идет на производство полиэфирного волокна (Nature |
|
|
организмов. Производство D-глюконовой кислоты, ее |
|
|
натриевой соли и δ-лактона – изомера D-глюконовой |
|
|
кислоты составляет 60 000 т в год. δ-Лактон также |
|
|
применяется в пищевой промышленности в качестве |
|
|
мягкого подкислителя. При лечении болезней, свя- |
|
|
занных с недостатком Ca2+ и Fe3+ в организме, в |
|
|
растворы для инфузии добавляют глюконаты кальция |
|
|
и железа, так как эти соли не токсичны и очень хоро- |
|
|
шо растворимы в воде. Глюконовая кислота – силь- |
|
|
ный комплексообразователь в щелочных условиях, |
|
|
поэтому значительная часть (около 50%) глюконо- |
|
|
вой кислоты в виде натриевой соли используется в |
|
|
технических целях – как средство для очистки сте- |
|
|
кол, удаления ржавчины и разрыхления цемента, а |
|
|
также в текстильной промышленности для предот- |
|
|
вращения загрязнения тканей солями металлов. рКа |
|
|
D-глюконовой кислоты 3,7. |
|
|
МИКРООРГАНИЗМЫ И БИОСИНТЕЗ. Для промышлен- |
|
|
ного прозводства молочной кислоты используют |
|
|
штаммы Lactobacillus. Выбор того или иного штамма |
|
|
зависит от наиболее доступного источника углерода. |
|
|
Полное превращение субстрата происходит только в |
|
|
случае гомоферментативного молочнокислого бро- |
|
|
жения – из 1 моль D-глюкозы образуется 2 моль |
|
|
L-молочной кислоты. Процесс неполного окисления |
|
|
D-глюкозы – образование D-глюконовой кислоты – |
|
|
описан для некоторых грибов (Aspergillus niger, неко- |
|
|
торых представителей рода Penicillium), а также |
|
|
для уксуснокислых бактерий рода Gluconobacter. |
|
|
У грибов реакцию катализирует глюкозооксидаза – |
|
|
флавинсодержащий фермент, локализованный в |
|
|
клеточной стенке. В условиях промышленной фер- |
|
|
ментации глюкозооксидаза обнаруживается и в сре- |
|
|
де роста гриба. Штаммы Gluconobacter осуществля- |
|
|
ют неполное окисление D-глюкозы с помощью |
|
|
мембраносвязанного фермента D-глюкозодегидроге- |
|
|
назы. Так же, как алкоголь- и альдегиддегидрогеназы |
|
|
уксуснокислых бактерий, D-глюкозодегидрогеназа в |
|
28 |
клетках Gluconobacter является ПХХ-зависимым |
|
ферментом. |
ФЕРМЕНТАЦИЯ И ПЕРЕРАБОТКА. В последнее время метод ферментативного получения молочной кислоты составляет конкуренцию химическому синтезу (путем гидратирования акриловой кислоты или присоединения HCN к ацетальдегиду). В зависимости от доступного источника углерода выбирают различные штаммы Lactobacillus: если в питательную среду добавляют декстрозу или раствор других сахаров, используют штаммы L. delbrueckii или L. leichmannii, а в случае роста на сыворотке – L. bulgaricus. Наряду с сахарами (12–18%) питательная среда должна содержать источник азота, фосфаты и витамины группы В. Ферментацию проводят в условиях ограниченного доступа кислорода при температуре 45–50 °С в течение 2–6 сут. в зависимости от начальной концентрации субстрата. Добавление CaCO3, нейтрализующего кислоту, обеспечивает постоянство рН 5,5–6,0. После отделения клеточной массы лактат кальция переводят в молочную кислоту серной кислотой. Далее молочную кислоту подвергают очистке с применением одной из двух методик – пропускают через ионообменную колонку или перегоняют метиллактат (эфир молочной кислоты и метанола). В стадии разработки находятся другие методики получения чистой молочной кислоты: экстракция растворителями, мембранное фильтрование и хроматографическая очистка самой молочной кислоты без стадии образования кальциевой соли. D-Глюконовую кислоту получают из D-глюкозы в ферментерах большого объема с использованием Aspergillus niger. При рН >3 в клетках грибных гиф образуется фермент клеточной стенки глюкозооксидаза, которая окисляет D-глюкозу до D-глюконо-5-лактона. Этот лактон гидролизуется самопроизвольно или под действием лактоназы до D- глюконовой кислоты. Ферментацию с целью получения натриевых и кальциевых солей глюконовой кислоты проводят при интенсивной аэрации на среде, содержащей 11–25% глюкозы. рН среды поддерживается в интервале 4,5–6,5 путем добавления раскислителей (Na2CO3/NaOH или CaCO3). По окончании ферментации, чтобы выделить соль, среду концентрируют, продукт сушат; в случае же свободной кислоты и лактона используют ионообменники для очистки продукта.
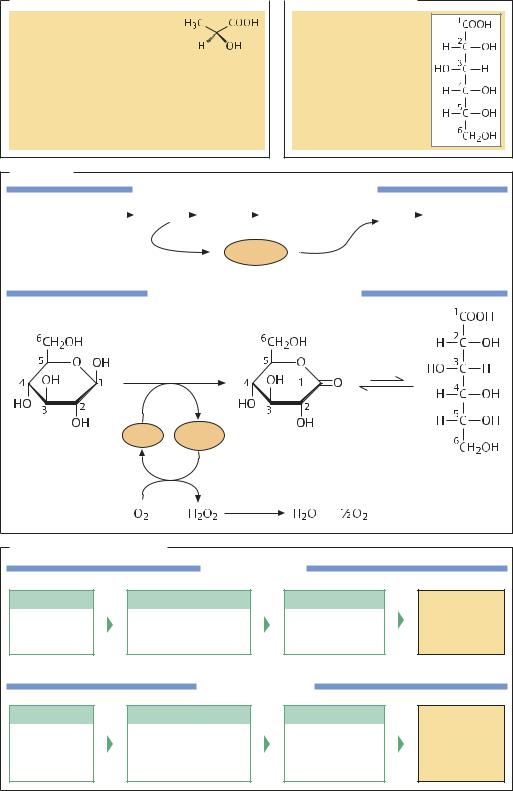
D-молочная кислота, L-молочная кислота |
|
|
|
|
D-глюконовая кислота |
|||
|
|
|
|
|||||
С3Н6О3 |
90,08 |
|
|
|
|
|
С6Н12О7 |
196,16 |
|
|
|
|
|
||||
MR |
|
|
|
|
|
MR |
||
pKa |
3,80 (25 °С) |
(S)-форма |
|
|
|
pKa |
3,7 (25 °С) |
|
Код CAS |
50-21-5 |
|
|
|
Код CAS |
526-95-4 |
||
|
|
|
|
|
||||
|
|
|
|
|
||||
|
10326-41-7 (R)-форма |
|
|
|
|
|||
|
79-33-4 (S)-форма |
|
|
|
|
|||
Химический синтез(реакция HCN с ацетальдегидом) приводит к образованию рацемата
Биосинтез
L-молочная кислота (Lactobacillus delbrueckii)
D-глюкоза |
|
|
|
|
|
2 Пируват |
|
2 L-лактат |
|
|
|
|
|
|
2 NADH
|
D-глюконовая кислота (Aspergillus niger) |
|
||
|
Глюкозооксидаза |
|
|
|
β-D-Глюкоза |
FAD |
FADH2 |
D-Глюконо-5-лактон |
|
|
|
|
|
D-Глюконовая кислота |
|
|
Каталаза |
|
|
Ферментация и переработка |
|
|
|
|
|
|
L-молочная кислота |
|
|
Инокулят |
|
Биореактор |
Очистка |
|
Lactobacillus |
Объем более 100 м3, |
Осаждение |
Bыход продукта |
|
|
декстроза, раствор |
кальциевой соли, |
2–3 кг/(м3 ч) |
|
|
сахаров, 50 °С, рН 5,5–6,0 |
переосаждение, |
|
|
|
|
|
перекристаллизация |
|
|
|
D-глюконовая кислота |
|
|
Инокулят |
|
Биореактор |
Очистка |
|
Aspergillus niger |
Объем более 100 м3, |
Отделение клеток, |
Выход продукта |
|
|
декстроза, раствор |
концентрирование, |
||
|
сахаров, 33 °С, рН 6,5 |
добавление NaOH, |
более 13 кг/(м3 ч) |
|
|
|
|
высушивание |
|
|
|
|
|
29 |